매괴화와 월계화(장미과)의 화피 미세형태학적 연구
This is an open access article distributed under the terms of the Creative Commons Attribution Non-Commercial License (http://creativecommons.org/licenses/by-nc/3.0/) which permits unrestricted non-commercial use, distribution, and reproduction in any medium, provided the original work is properly cited.
Abstract
Rosa rugosa Thunb. (Rosae Rugosae Flos) and R. chinensis Jacq. (Rosae Chinensis Flos) are medicinal shrubs widely used in East Asia, where dried flower buds are traded as herbal drugs. Because the two species exhibit similar floral morphology but differ in their pharmacopeia status, accurate identification is essential to ensure authenticity and quality control. Moreover, confirming the taxonomic position of the white-flowered R. rugosa is necessary to evaluate the origins of Rosae Rugosae Flos.
Fresh R. rugosa and its white variants were collected, and herbal samples of R. rugosa and R. chinensis were examined using light and scanning electron microscopy. The petals of all taxa had papillate epidermis with cuticular striations, indicating functional stability. The white-flowered R. rugosa shared identical traits, confirming intraspecific variation within the same species. The sepals of R. rugosa bore secretory and simple trichomes, whereas those of R. chinensis were glabrous, providing a key diagnostic marker.
These results indicate that sepal trichome distribution is a reliable diagnostic marker for distinguishing R. rugosa from R. chinensis. The findings also confirm that the white-flowered R. rugosa should be regarded as an intraspecific variation. This study provides essential micromorphological criteria for authenticating Rosa-derived herbal medicines, thereby contributing to their safe and effective pharmacological use.
Keywords:
Rosa rugosa Thunb., Rosa chinensis Jacq., Rosae Rugosae Flos, Rosae Chinensis Flos, Scanning Electron Microscope서 언
장미과 (Rosaceae Juss.)는 90 — 100여개 속, 2,890 — 3,300여 종으로 구성된 쌍자엽식물군으로, 주로 북반구의 온대 및 아열대 지역에 다양한 분류군이 분포하는 것으로 보고되어 있다 (Kalkman, 2004; Potter et al., 2007; Hummer and Janick, 2009). 한반도에는 37속, 146종의 장미과 분류군이 분포하며 (Lee, 2018), 다양한 재배식물도 함께 서식하고 있는 것으로 보고되어 있다 (Korea National Arboretum, 2016). 장미과 식물은 원예 및 작물적 가치뿐만 아니라 천연물, 생약 소재 및 한약재로 활용되고 있으며, 다수의 식물이 각국의 약전 및 공정서에 기원종으로 수재되어 있다 (Song et al., 2020a).
이들 중 장미속 (Rosa L.)은 장미아과 (Rosoideae Juss. ex Arn.)에 속하며, 전 세계적으로 약 200종이 북반구 온대 및 한대지역에 서식하고 있고, 한반도 내에는 10종이 분포하는 것으로 보고된 바 있다 (Gu and Robertson, 2003; Lee, 2018).
장미속에 속하는 분류군 중 해당화 (R. rugosa Thunb.)는 동북아시아의 해안지역과 국내 동해안과 서해안에 자생하는 다년생 관목으로, 홍자색 또는 자주색의 양성화가 달린다 (Ohba, 2001; Gu and Robertson, 2003; Lee, 2018). 일부 흰색의 꽃을 지닌 분류군을 흰해당화로 기본종과 구별하여 인식하기도 하는데, R. rugosa var. albiflora Koidz. (Ohba, 2001; POWO, 2025), R. rugosa f. albiflora (Ohba, 2001), R. rugosa ‘Alba’ (Korea National Arboretum, 2016), 각각 다른 학명으로 인식하기도 하지만 최근에는 해당화의 이명 (synonym)으로 처리되는 추세이다 (Gu and Robertson, 2003; POWO, 2025). 해당화는 건조 가공 과정을 거친 꽃봉오리를 한약 (생약)재 매괴화 (玫瑰花, 생약명: Rosae Rugosae Flos)의 형태로 유통된다 (Chinese Pharmacopoeia Committee, 2015; Korea Food and Drug Administration, 2021). 매괴화는 전통적으로 월경불순, 통경 지통, 종기 치료에 활용되며 (Yu et al., 2014), 최근에는 항산화, 항염증, 항균, 미백, 주름 개선, 장내 수크레이스 (sucrase) 억제 효과 등 약리 효과가 보고된 바 있고 (Young et al., 1990; Hong et al., 2001; Lee et al., 2003; Thao et al., 2014), 기능성 화장품 및 건강기능식품의 원료로도 주목받고 있는 매우 중요한 자원식물이다 (Yu et al., 2014).
동속 이종인 월계화 (R. chinensis Jacq.)는 중국에 자생하는 식물이지만, 국내에는 재배식물로 보고되어 있다 (Korea National Arboretum, 2016). 월계화의 소엽은 3 — 5개의 넓은 난형 또는 타원형으로, 잎의 양면에 털이 없다. 꽃은 4 — 9월에 개화하며, 가지 끝에 겹꽃의 붉은색 또는 흰색의 양성화가 달린다. 꽃은 지름 4 — 5 cm이고, 향기가 약하거나 없다. 악편 (꽃받침)의 향축면 (상면)에는 털이 밀생하고, 배축면 (하면)은 무모 (glabrous)라는 점에서 해당화와 구분된다 (Gu and Robertson, 2003). 월계화 역시 매괴화와 유사하게 건조된 꽃봉오리를 월계화 (月季花, 생약명: Rosae Chinensis Flos) 약재로 활용한다 (Chinese Pharmacopoeia Committee, 2015). 월계화는 자가면역 억제, 항산화 효과, 향균 효과와 당뇨병 개선에 대한 연구 결과가 보고된 바 있다 (Kim et al., 2011; Zhou et al., 2023).
매괴화와 월계화는 모두 장미속에 속하는 분류군으로 건조된 꽃봉오리를 약재로 사용한다는 공통점이 있다. 다만, 매괴화는 한국과 중국 약전에 모두 기원종으로 수재되어 있는 반면, 월계화는 중국 약전에만 수재되어 있다 (Chinese Pharmacopoeia Committee, 2015; Korea Food and Drug Administration, 2021). 하지만 국내에도 공정서 기원종에 수재되어 있지 않은 월계화가 관상 및 약용의 목적으로 전국에 걸쳐 재배되고 있기 때문에 외형이 유사한 두 약재의 혼입 및 유통이 우려된다. 기원종과 동속 근연종, 유사종의 혼입은 약효의 일관성을 저해하고 품질 저하 및 약용 자원 관리에 혼란을 초래할 수 있기 때문에 명확한 감별 기준이 필요하다.
또한, 해당화 (매괴화)의 약리효과는 주로 화판 (꽃잎)과 악편 조직에서 분비되는 생리활성 물질에 기인한다고 보고되어 있다 (Sulborska et al., 2012; Sulborska and Weryszko, 2014). 선행 연구에 따르면 해당화의 악편에는 분비성 선모가 존재하며, 생리활성 물질의 상당수는 해당 구조에서 생성 및 분비되는 것으로 알려져 있다 (Sulborska and Weryszko, 2014). 또한, 장미속 분류군 꽃의 미세형태학적 형질은 종 동정과 분류군 인식에 매우 유용한 형질로 알려진 바 있다 (Žarković et al., 2022; Seyedipour and Mahdigholi, 2024). 따라서 분비성 선모 등의 미세형태학적 구조는 기원식물 간 차이를 식별할 수 있는 중요한 진단 형질로 활용되어 형태가 유사한 장미속 식물 간의 정확한 동정 및 감별 기준 확립에 유용하게 활용될 수 있다.
한편, 해당화의 화색 (꽃색) 차이는 플라보노이드 (flavonoid) 및 안토시아닌 (anthocyanin) 생합성 경로의 유전자 발현 조절에 의해 결정되며, 특정 유전자의 발현 정도가 붉은색·분홍색·흰색 꽃의 형성에 직접적으로 영향을 미친다는 연구 결과가 보고된 바 있다 (Sheng et al., 2018). 그러나 가공된 약재 상태에서 매괴화와 월계화 및 그 기원식물의 미세형태학적 형질을 직접적으로 비교한 연구는 아직까지 보고된 바 없으며, 특히 화색 변이에 따른 해당화 및 그 종하 분류군의 미세형태학적 차이를 기반으로 한 분류학적 위치를 논의한 연구는 매우 제한적이다.
미세종자 (Song et al., 2018), 화분·포자 (Kim et al., 2020), 화판 표피 (Park et al., 2020), 잎 표피 (Song et al., 2020b) 등 다양한 약재 기원종에서 광학현미경 (light microscope)과 주사전자현미경 (scanning electron microscope) 등 현미경적 검경을 이용한 한약재 미세형태감별의 유용성이 이미 검증된 바 있어, 해당 분류군의 미세형태 감별 기준 마련을 위한 형질 연구가 필요하다.
이에 본 연구에서는 약재로 유통 중인 매괴화와 월계화의 미세형태학적 형질을 관찰 및 비교하고, 특히 붉은색과 흰색 화판을 가진 해당화와 흰해당화 간의 미세형태학적 구조 차이를 비교·분석하였다. 이를 통해 매괴화, 월계화 감별 및 품질 관리를 위한 기초자료를 축적하고, 해당화 화색 변이에 따른 미세형태학적 차이를 확인하여 분류학적으로 고찰하고자 하였다.
재료 및 방법
1. 연구 재료
개화기의 해당화와 흰해당화를 자생지에서 직접 채집하였고, 약재인 매괴화와 월계화는 한국한의학연구원 한약표준자원은행 (KIOM)에 보관된 시료를 연구 대상으로 하였다. 채집된 해당화와 흰해당화는 70% ethanol 용액에 액침표본으로 제작하였고, 해당화의 일부는 석엽표본으로 제작하였다. 사용된 재료 및 표본 정보는 다음과 같다 [R. rugosa: Korea, Chungcheongbuk-do, Cheongju-si, 27. Apr. 2025. Lee 598 (CBU, herbarium acronym); R. rugosa f. albiflora: Korea, Incheon, 02. Jun. 2024. Song 213 (CBU); Rosae Rugosae Flos: China, Sichuan, 10. Mar. 2014. 1403055 (KIOM); Rosae Chinensis Flos: 10. Mar. 2012. 1207078 (KIOM)].
2. 외부 형태
해당 연구에서 사용된 생태사진과 약재사진은 디지털 카메라 (Tough TG-6 digital camera, Olympus, Tokyo, Japan)로 촬영하였다. 악편의 표면을 관찰하기 위해 악편을 차아염소산 나트륨 (NaClO)에 24시간 보관 후, 악편의 표피를 벗겨낸 뒤 슬라이드글라스 위에 올려 실체현미경 (stereo microscope, S9D, Leika, Wetzlar, Germany)으로 관찰하였다.
3. 미세 형태
건조 약재는 연화 및 수화 처리를 위해 연화제 (wetting agent, Agepon: distilled water = 1:200) (Agfa Gevaert, Leverkusen, Germany)에 넣고 37℃에서 하루 동안 수화 (rehydrate) 후 70% ethanol 용액에 보관하였다. 화판과 악편의 미세형태학적 형질을 관찰하기 위해 수화된 건조 약재 시료와 채집된 액침 시료는 에탄올 시리즈를 통해 탈수 과정 (50%, 70%, 90%, 95%, 100%에서 각 1시간)을 진행하였다. 이후 임계점 건조기 (critical point dryer, SPI-13200J-AB, SPI Supplies, West Chester, PA, U.S.A.)를 사용하여 완전 건조시켰으며, 건조 시료는 직경 9.5 ㎜ 알루미늄 스터브 (aluminium stub, 01501-BA, SPI Supplies, West Chester, PA, U.S.A.) 위에 카본테이프로 고정하였다. 또한, 이온 증착기 (ion sputter coater, Q150T ES Plus, Quorum Technologies Ltd., Laughton, U.K.)를 이용해 백금 (platinum, Pt)으로 45초간 이온 증착 하였다. 채집품인 해당화와 흰해당화의 경우, 면밀한 관찰을 통한 분류학적 해석을 위해 화판은 정단부 (apex part)와 중앙부 (middle part)의 시료를 각각 제작하였고, 악편은 정단부 (apical part)와 기저부 (basal part)로 나누어 부위별로 비교·분석하였다. 약재 시료인 매괴화와 월계화의 경우, 화판은 중앙부, 악편은 기저부를 검경하여 비교·분석하였다. 주사전자현미경 (scanning electron microscope, EM30+, COXEM, Daejeon, Korea)을 통해 가속전압 5 kV, 작동거리 5.4 — 6.0 ㎜에서 관찰하였으며, 화판은 1.0k — 5.0k, 악편의 모용은 0.3k — 2.0k 그 외 형질은 0.5k — 5.0k 배율에서 검경하였다.
결 과
1. 화판 표피 미세형태
해당화 (R. rugosa)와 흰해당화 (R. rugosa f. albiflora)의 꽃은 모두 5수성이고, 방사상칭형 (actinomorphic)이며, 이판화 (polypetalous flower)이고, 다수의 수술이 관찰되었다. 해당화는 자홍색의 화판, 흰해당화는 흰색의 화판으로 확인되었다 (Fig. 1A-B). 매괴화의 화판 외면은 노란색이나 화판 내면은 자홍색으로 관찰되었고, 월계화의 화판 외면은 밝은 자홍색이나, 내면은 자주색으로 관찰되었다 (Fig. 1C-D).

Photographs of the Rosa rugosa and medicinal materials.A-B; Habit in natural population, C-D; Herbal medicine, A; R. rugosa, B; R. rugosa f. albiflora, C; Rosae Rugosae Flos, D; Rosae Chinensis Flos.
화판의 외면 표피세포의 모양은 해당화에서는 등방형 (isodiametric), 흰해당화에서는 불규칙형 (irregular), 매괴화에서는 등방형과 불규칙형이 동시에 관찰되었다. 수층벽 (anticlinal wall)은 위의 세 시료에서 모두 직선형 (straight)과 곡선형 (curved)이 동시에 관찰되었고, 월계화는 각피층 (cuticle)이 넓게 퍼져있어 표피세포와 수층벽을 관찰할 수 없었다. 모든 시료에서 병층벽 (periclinal wall)은 평평 (flat)하였으며, 각피층에는 줄무늬 (striations)가 관찰되었고 (Table 1; Fig. 2A, C, G, I, K, M, O), 원형 또는 타원형의 표면 무늬가 관찰되었다 (Fig. 2E).

SEM micrographs of the petal of the Rosa taxa.A-E, I-L; Apex part, F-H, M-P; Middle part, A, C, E, G, I, K, M, O; Outer surface, B, D, F, H, J, L, N, P; Inner surface, A, B, E, F; R. rugosa, C, D, G, H; R. rugosa f. albiflora, I, J, M, N; Rosae Rugosae Flos, K, L, O, P; Rosae Chinensis Flos.
화판의 내면 표피세포의 모양은 모든 시료에서 유두상 세포(papillae)가 관찰되었으며, 수층벽은 곡선형으로 관찰되었고, 병층벽은 볼록 (convex)하였고, 각피층에는 줄무늬가 관찰되었다 (Table 1; Fig. 2B, D, F, H, J, L, N, P). 해당화와 흰해당화의 화판 표면에서는 정유 (essential oil) 성분으로 추정되는 방출된 분비물 (secretory substances)이 관찰되었다 (Fig. 3).
2. 악편 표피 미세형태
악편의 외면 표피세포는 해당화와 흰해당화에서 등방형, 매괴화에서 등방형과 불규칙형이 동시에 관찰되었고, 월계화는 불규칙형으로 관찰되었다. 수층벽은 해당화, 매괴화, 월계화에서 직선형과 곡선형이 동시에 나타났으며, 흰해당화는 곡선형이 관찰되었다. 병층벽은 해당화, 흰해당화, 매괴화에서 평활(smooth)하였고, 월계화는 불규칙한 홈 (irreguraly grooved)이 관찰되었다 (Table 2; Fig. 4A, C, E, G, I, K). 기공복합체는 모든 시료의 외면에 분포하였으며, 기공복합체의 형태는 부재형 (anomocytic type)으로 확인되었다 (Table 2; Fig. 4A, C, E, G, I, K).
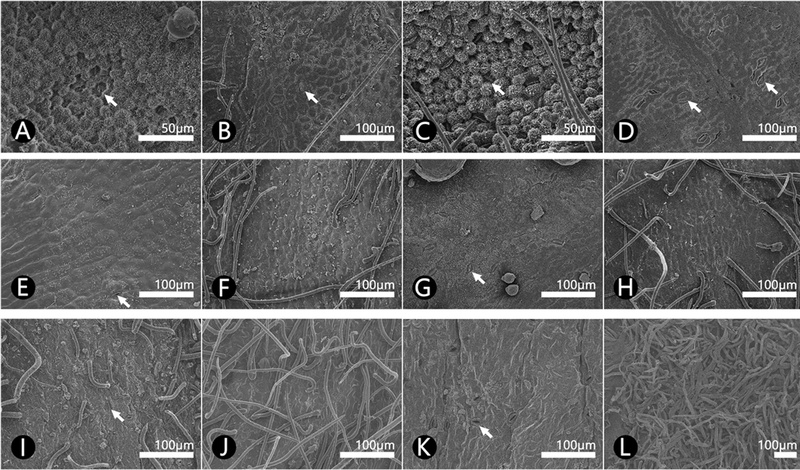
SEM micrographs of the sepal of the Rosa taxa.The arrow indicate stomata complex. A-D; Apical part, E-L; Basal part, A, C, E, G, I, K; Outer surface, B, D, F, H, J, L; Inner surface, A-B, E-F; R. rugosa, C-D, G-H; R. rugosa f. albiflora, I-J; Rosae Rugosae Flos, K-L; Rosae Chinensis Flos.
악편 내면 표피세포는 해당화와 매괴화에서 등방형으로 관찰되었고, 흰해당화에서 등방형과 불규칙형이 동시에 관찰되었다. 수층벽은 해당화와 흰해당화에서 직선형과 곡선형이 동시에 나타났으며, 매괴화에서 곡선형, 병층벽은 해당화와 흰해당화에서 매끈하게 관찰되었고, 매괴화에서 불규칙한 홈이 확인되었다 (Table 2; Fig. 4B, D, F, H, J). 모든 시료의 악편 말단부 내면에서 기공복합체가 관찰되지 않았지만, 해당화와 흰해당화의 정단부에서 기공이 관찰되었으며, 기공복합체의 형태는 모두 부재형으로 확인되었다 (Table 2; Fig. 4B, D).
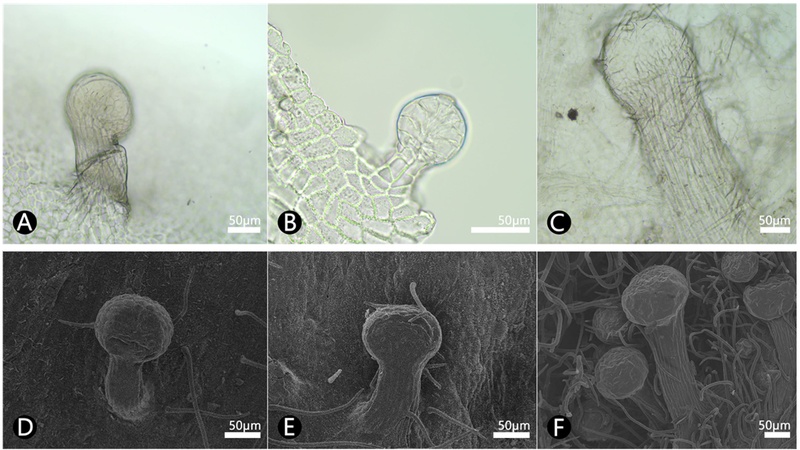
해당화와 흰해당화, 매괴화의 악편 외면에는 모두 단세포 단모 (simple uni-cellular trichome)가 관찰되었고 (Table 2; Fig. 4C, G, I), 자루가 있는 다세포 분비성 두상 선모(stalked multi-cellular secretory capitate)가 산생하는 것으로 관찰되었으나 (Table 2; Fig. 5), 월계화는 무모 (glabrous)로 나타났다 (Table 2; Fig. 4K). 반면, 악편 내면에서는 해당화, 흰해당화, 매괴화, 월계화 모두에서 단세포 단모가 확인되었으며 (Table 2; Fig. 4B, F, H, J), 특히 월계화는 단세포 단모가 밀생하여 분포하였다 (Fig. 4L).
고 찰
본 연구에서는 약재 매괴화와 그 기원종인 식물체 해당화, 근연종 (동속이종)인 약재 월계화의 화판, 악편 표면을 외부형태학적 및 미세형태학적으로 비교·검토하였다. 시료는 자연 서식지에서 채집한 시료와 유통되는 약재 시료를 대상으로 하였으며, 주사전자현미경을 이용하여 면밀한 형태 관찰을 수행하였고, 일부 형질은 광학현미경을 병행하여 정밀하게 분석하였다.
외부형태학적으로 해당화 (R. rugosa)는 식물체 전체에 가시가 밀생하고, 짧은 모용, 분비성 선모가 혼재하는 특징을 지닌다. 또한, 잎은 우상복엽으로 호생하며, 5 — 7개의 타원형 또는 도란형의 소엽으로 구성되고, 꽃은 5 — 7월에 개화, 가지 끝에 1 — 3개씩 홍자색 또는 자주색의 양성화가 달린다. 꽃은 지름 4 — 10 cm이며, 향기가 강하다. 꽃잎은 5장이고, 도란형 또는 아원형으로 끝이 둥글거나 오목하다. 악편은 피침형의 5개의 열편으로 구성되며, 길이는 2 — 3 cm이고, 열편의 끝은 고리처럼 돌출되어 있으며, 향이 강하고, 열매는 장미과(hip)이다 (Ohba, 2001; Sulborska and Weryszko-Chmielewska, 2014; Lee, 2018). 본 종은 엽축에 가시가 없고, 잎 하면에 털이 있으며, 탁엽은 빗살거치연으로 속 내 다른 분류군과 형태적으로 구별된다 (Lee, 2018). 동속 이종인 월계화 (R. chinensis)는 3 — 5개의 넓은 난형 또는 타원형의 소엽을 지니고, 잎은 무모이다. 꽃은 4 — 9월에 개화하며, 가지 끝에 겹꽃의 붉은색 또는 흰색의 양성화가 달린다. 꽃은 지름 4 — 5 cm이고, 향기가 약하거나 없다. 악편의 향축면 (상면)은 털이 빽빽하게 밀집해 있고, 배축면 (하면)이 무모라는 점에서 해당화와 구분된다 (Gu and Robertson, 2003).
미세형태학적 형질 분석 결과, 모든 시료의 화판에서 유두상 표피 세포구조가 확인되었다. 해당 구조는 빛의 집중적 포획을 통해 액포 내 안토시아닌 색소가 빛을 다량으로 흡수하여 화판 색이 강조되도록 하거나, 평평한 표피에 비해 반사각을 줄여 감소된 빛의 반사로 수분매개자를 유인하는 등 수분생물학적 기능을 수행한다고 알려져 있다 (Kay et al., 1981; Gorton and Vogelmann, 1996; Glover and Martin, 1998, 2002; Comba et al., 2000; Dyer et al., 2007; Martin and Glover, 2007). 또한 유두상 세포는 발판의 기능으로 직접 곤충이 표면을 인식함으로써 꿀샘까지 유인, 인도하는 촉각적 신호를 제공한다는 연구 (Kevan and Lane, 1985) 뿐만 아니라 판상의 세포보다 표면적이 넓고 요철이 있어 곤충이 화판에 쉽게 착륙하고 지지하는 등 섭식 효율을 높인다는 결과가 보고된 바 있다 (Whitney et al., 2009). 연구된 모든 시료에서 화판 향축면 (내면, 상면) 표피세포는 유두상 세포로 확인되었으며, 해당화와 흰해당화는 화판과 악편 모두에서 유사한 형질을 지니는 것으로 확인되었다. 이는 두 분류군이 미세형태학적으로 안정적인 형질을 공유하는 것으로 판단하였다.
또한, 해당화의 유두상 세포에서 분비되는 생리활성 물질을 분석하고, 관찰한 연구가 보고된 바 있다 (Sulborska et al., 2012). 본 연구에서 역시 해당화와 흰해당화의 화판 내면 유두상 세포에서 분비물이 관찰되어 선행 연구와 일치하였다. 반면, 매괴화와 월계화에서는 유두상 세포에서 분비물이 관찰되지 않아 연구와 상반되는 결과를 나타냈다. 이는 약재 가공 과정 중 약리 성분의 소실에 따른 결과로 판단되나, 개체 변이, 성장적 변이에 대한 비교가 이루어지지 않아 보다 명확한 후속 연구가 필요한 것으로 판단하였다.
장미속 분류군의 화색이 다양한 이유는 화판 색 변이가 안토시아닌 및 플라보노이드 합성 관련 유전자 발현의 차이에 기인한다는 연구가 보고된 바 있다 (Sheng et al., 2018). 본 연구 결과, 해당화와 흰해당화는 화색의 차이만 나타날 뿐 형태, 미세형태학적으로는 모두 동일하게 확인되어 흰색의 꽃잎은 해당화의 종 내 변이로 판단하였다. 실제 화색은 다양한 조절 및 기능 돌연변이의 조합, 수분매개자의 차이, 토양 성분의 차이, 색소의 차이 등에 기인하며, 동일 종 내에서도 화색의 다형성 (polymorphism)이 나타나 화색만으로 종을 명확히 구분하거나 범주화하기 어렵다고 제안된 바 있다 (Wessinger and Rausher, 2012; Wu et al., 2013; Dafni et al., 2020). 따라서, 화색이 아닌 구조적 특징인 유두상 표피세포가 해당화와 흰해당화 모두에서 안정적으로 관찰됨에 따라 화판의 색과 무관하게 곤충 매개 수분에 적응된 기능적 구조로 이해된다. 반면, 두 분류군 간 화판 색 차이에 따른 수분매개자와의 상호작용은 충분히 연구되지 않았으므로, 화판의 색과 수분매개자의 상호작용에 관한 보다 면밀한 수분 생태적 (pollination ecology) 연구가 필요할 것으로 판단된다.
각피 (큐티클, cuticle)는 식물 표면과 외부 환경 사이의 1차적인 방어막일 뿐만 아니라 증산 및 외부 자극을 막는 기능을 수행하는 것으로 알려진 바 있다 (Riederer and Schreiber, 2001; Evert, 2006; Molina et al., 2023). 또한, 화판 표피에서 향기 및 정유 (essential oil) 성분의 저장 및 방출에 관여하는 기능적 구조로 보고된 바 있다 (Evert, 2006; Molina et al., 2023). 분비 물질의 축적에 따라 각피가 신장되거나, 국소적으로 홈 (groove)을 형성한다는 연구가 보고된 바 있으며 (Esau, 1973), 특히 해당화의 화판 표피세포 내 각피 줄무늬가 활성의 증가에 따라 확장되어 배열이 변화하고, 각피의 파열과 함께 분비물이 외부로 방출되는 것으로 보고된 바 있다 (Sulborska et al., 2012). 실제로 각피에 향기 성분이 저장되고 방출의 기능을 수행한다는 결과가 보고된 바 있다 (Ancensão and Pais, 1998; Evert, 2006; Sulborska et al., 2012). 본 연구에서 모든 시료의 화판 내면 표피에서 각피 줄무늬의 소실과 원형 또는 타원형의 표면이 변화된 영역이 확인되어 기존의 연구 결과와 동일하게 나타난 것으로 확인되었다. 반면, 모든 시료에서 각피의 파열은 관찰되지 않아 선행 연구와는 차이를 나타냈다. 이러한 차이는 성장적 변이에 따라 분비 물질의 양이 달라짐에 기인한 변이로 해석되며, 약재 기원종의 생육 시기 및 채집 시점에 따른 약리적 효과에 대한 후속연구가 필요할 것으로 판단하였다. 특히 약재인 꽃봉오리 상태와 완전 개화 상태의 형질 및 방출 물질의 이화학적 비교 분석을 통해 최적 약재 수확 시기를 확인할 필요가 있겠다.
약재 상태인 매괴화와 월계화에서 화판 외면 표피의 각피가 채집 시료인 해당화에 비해 상대적으로 두껍게 관찰되었다. 각피층의 유무 및 두께 등의 형질은 서식지 온도, 자외선, 습도 등 환경 및 생태적 영향을 많이 받는다고 보고된 바 있다 (Domínguez et al., 2011; Bueno et al., 2021). 두꺼운 각피층은 건조한 환경에서 증산 작용에 의한 수분 손실을 줄이기 위한 전략으로 알려져 있으며 (Rotondi et al., 2003; Oliveira et al., 2003; Agrawal et al., 2009; Molina et al., 2023), 특히 각피가 비기공성 증산 (non-stomatal transpiration)을 억제하는 주요 장벽으로 가뭄 내성 및 수분 결핍과 매우 밀접히 관련된다는 보고가 있다 (Chen et al., 2020). 한편, Rosa roxburghii Tratt 열매 약재의 건조 가공 방법 (열풍건조, 적외선건조, 마이크로파 진공건조, 동결건조)에 따라 다당류의 구조적 특성과 생리활성이 달라진다는 연구가 수행된 바 있다 (Zhang et al., 2024). 약재 가공 과정인 건조 방식과 각피층의 구조 변형과의 관계 혹은 생육 환경의 차이에서 각피층의 구조적 차이가 기인하는지 해부학적 기법 및 다양한 서식지에서 확보한 개체를 대상으로 한 확장된 비교 연구가 수행되어야 하겠다.
분비성 선모 (secretory glands)는 식물체에서 다양한 2차 대사산물을 합성 및 분비하는 기관으로, 외부 환경에 대한 방어뿐만 아니라 수분매개자의 유인, 방향성 물질의 분비 및 저장과 같은 생태적 기능에 중요한 역할을 하는 것으로 알려져 있다 (Ancensão and Pais, 1998; Werker, 2000; Sulborska et al, 2012, Liu et al., 2022). 장미과 내 분류군에서 분비성 선모는 방향성 물질의 분비 및 기능성 물질을 축적하는 것으로 보고된 바 있으며 (Sulborska et al., 2012), 이는 장미과 식물이 약용 및 방향성 (aromatic)을 위한 정유 자원으로 전통적으로 활용되어 온 사실과도 밀접하게 연결된다. 본 연구에서 매괴화와 월계화를 미세형태학적으로 비교한 결과, 매괴화의 악편 외면 표피에서는 분비성 선모와 단세포 단모가 밀생하여 분포하였으나, 월계화는 무모성으로 확인되었다. 매괴화에서 관찰된 분비성 선모는 약리 활성 성분의 생성 및 축적에 직접적으로 관여하는 기능적 형질로 판단하였다. 한편, 모용의 종류와 분포의 차이는 두 분류군이 근연종임에도 불구하고 명확히 구분되는 형질로 확인된다. 특히 장미과 내 일부 분류군에서 화판 내 모용의 유무, 종류, 밀도 등의 형질이 분류학적으로 종을 구분하는 주요 형질로 활용될 수 있음이 확인된 바 있어 (Žarković et al., 2022; Seyedipour and Mahdigholi, 2024), 모용의 유무가 매괴화와 월계화를 약재 상태에서 감별할 수 있는 주요 진단 (감별)형질로 활용될 것으로 판단하였다.
더불어, 조직화학적 분석 (histochemical analysis)에 따르면 분비성 선모는 플라보노이드, 페놀 (phenol), 탄닌 (tannin) 등의 주요 생리활성 성분의 주된 생성 및 축적 부위이며 (Sulborska et al., 2012; Sulborska and Weryszko, 2014; Liu et al., 2022), 비분비성 선모 (non-secretory glands)나 일반 표피세포에 비해 생리활성 물질을 고농도로 축적하는 것으로 보고된 바 있다 (Sulborska et al., 2020). 분비성 선모의 유무와 밀도는 단순한 형태학적 구분을 넘어 약리효과의 차이를 설명할 수 있는 중요한 미세형태학적 근거로 해석될 수 있다. 실제로 꿀풀과 (Lamiaceae)의 배초향 (Agastache rugosa Kuntze)에서 동일한 종이지만, 내륙과 해안으로 구분되는 서식지 차이에 기인한 분비성 선모의 빈도 차이 (생태적 변이)가 특정 정유 성분 (pulegone)의 함량 차이로 나타난다는 보고가 있다 (Song et al., 2024). 본 연구에서 확인된 분비성 선모의 유무에 따른 매괴화, 월계화의 차이는 두 분류군 간 약리 활성 물질의 함량 및 품질의 차이가 있을 가능성을 시사한다. 따라서, 이를 검증하기 위한 생리학적, 약리학적 후속 연구가 필요할 것으로 판단된다.
또한 해당화와 월계화의 미세형태학적 비교 결과, 화판은 동일한 세포 구조로 확인된 반면, 해당화의 악편 외면에서는 분비성 선모와 단세포 단모가 모두 관찰되었으나, 월계화에서는 단세포 단모만이 관찰되었다. 악편 내면에서 해당화는 단세포 단모가 산생하는 반면, 월계화는 밀생하여 분포하였다. 해당 형질 차이를 통해 악편 내 모용의 종류와 분포, 밀도가 해당화와 월계화를 구분하는 주요 감별 형질로 확인되었고, 현장에서 육안 또는 루페 등을 통해 악편을 확인하는 것만으로 두 약재를 감별할 수 있을 것으로 판단하였다.
기공은 식물의 증산과 기체교환을 통해 수분 스트레스와 온도를 조절하는 기본적인 구조이다 (Pillitteri and Torii, 2012). 이전 연구에서 해당화 악편의 기공은 악편의 외면에만 존재하는 것으로 보고된 바 있다 (Sulborska and Weryszko, 2014). 본 연구 결과, 기저부에서는 기존 결과와 동일하게 외면에서만 기공이 확인되었으나, 정단부에서는 양면 모두에서 기공이 나타났다.
이러한 결과는 악편 내에서도 부위별로 기공 분포가 상이함을 의미하며, 이는 기관의 위치에 따른 생리적 기능의 차이를 보일 수 있다. 장미과 내 분류군에서 악편 내 기공의 위치, 크기, 밀도는 안정적인 분류학적 형질로 활용될 수 있기도 하지만 (Huang et al., 2018), 환경 조건과 생리적 적응 전략에 따라 다양한 변이가 나타날 수도 있다고 알려져 있다 (Hetherington and Woodward, 2003). 추후 장미속 전체 분류군으로의 확장과 악편 표피의 부위별 검경을 통해 기공의 분포와 패턴이 종간 인식 형질로 활용될 수 있을지 면밀한 연구가 필요할 것이다.
본 연구에서 장미속 4가지의 시료 (채집 시료 해당화, 흰해당화 및 약재 시료 매괴화, 월계화) 화판, 악편 표피세포의 형태, 모용의 종류와 분포 양상, 기공의 분포 등의 형질을 상세히 관찰하고, 기술하여 가공된 약재와 채집 시료의 미세형태학적 형질을 제시하였다. 그 결과, 약재의 각피층이 상대적으로 두꺼운 것에 대해 환경적 변이 혹은 약재 공정 과정에서의 차이의 가능성을 고찰하였으며, 그 외 형질의 유사성을 확인하였다. 특히 건조의 가공을 거치더라도 주요 미세 형질이 잘 보존되어 연화 및 수화의 실험 과정을 통해 미세형태를 관찰할 수 있음을 확인하였다. 또한, 해당화와 흰해당화의 미세형태학적 형질이 매우 유사하게 나타남에 따라 흰해당화를 종하 분류군이 아닌 화판 색 변이에 따른 종 내 변이로 판단하였다. 또한, 악편에서의 모용의 유무가 매괴화와 월계화의 주요 감별 기준임을 제시하였다.
추후 두 약재 기원종의 성장적, 생태적 변이, 재배 특성, 약효 차이, 추가적인 활용 방안에 대한 연구가 수행되어야 할 것으로 생각된다.
Acknowledgments
본 연구는 한국연구재단 중견연구자지원사업(Grant No. RS-2023-00208589)과 산림청(한국임업진흥원) 산림과학기술 연구개발사업(RS-2021-KF001796)의 지원으로 수행되었습니다.
References
-
Agrawal AA, Fishbein M, Jetter R, Salminen JP, Goldstein JB, Freitag AE and Sparks JP. (2009). Phylogenetic ecology of leaf surface traits in the milkweeds(Asclepias spp.): Chemistry, ecophysiology, and insect behavior. New Phytologist. 183:848-867.
[https://doi.org/10.1111/j.1469-8137.2009.02897.x]

-
Ancensão L and Pais MS. (1998). The leaf capitate trichomes of Leonotis leonurus: Histochemistry, ultrastructure, and secretion. Annals of Botany. 81:263-271.
[https://doi.org/10.1006/anbo.1997.0550]

-
Bueno A, Alonso-Forn D, Peguero-Pina JJ, Xavier de Souza A, Ferrio JP, Sancho-Knapik D and Gil-Pelegrín E. (2021). Minimum leaf conductance(gmin) is higher in the treeline of Pinus uncinata Ram. in the Pyrenees: Michaelis’ hypothesis revisited. Frontiers in Plant Science. 12:786933. (cited by 2025 Oct 15).
[https://doi.org/10.3389/fpls.2021.786933]

-
Chen M, Zhu X, Zhang Y, Du Z, Chen X, Kong X, Sun W and Chen C. (2020). Drought stress modify cuticle of tender tea leaf and mature leaf for transpiration barrier enhancement through common and distinct modes. Scientific Reports. 10:6696. (cited by 2025 Oct 15).
[https://doi.org/10.1038/s41598-020-63683-4]

- Chinese Pharmacopoeia Committee. (2015). Pharmacopoeia of the People’s Republic of China. 2015 edition. Part I. China Medical Science and Technology Press. Beijing, China.
-
Comba L, Corbet SA, Hunt H, Outram S, Parker JS and Glover BJ. (2000). The role of genes influencing the corolla in pollination of Antirrhinum majus. Plant, Cell & Environment. 23:639-647.
[https://doi.org/10.1046/j.1365-3040.2000.00580.x]

-
Dafni A, Tzohari H, Ben-Shlomo R, Vereecken NJ and Ne’eman G. (2020). Flower colour polymorphism, pollination modes, breeding system and gene flow in Anemone coronaria. Plants-Basel. 9:397. (cited by 2025 Oct 15).
[https://doi.org/10.3390/plants9030397]

-
Domínguez E, Heredia-Guerrero JA and Heredia A. (2011). The biophysical design of plant cuticles: An overview. New Phytologist. 189:938-949. (cited by 2025 Oct 15).
[https://doi.org/10.1111/j.1469-8137.2010.03553.x]

-
Dyer AG, Whitney HM, Arnold SE, Glover BJ and Chittka L. (2007). Mutations perturbing petal cell shape and anthocyanin synthesis influence bumblebee perception of Antirrhinum majus flower colour. Arthropod-Plant Interactions. 1:45-55.
[https://doi.org/10.1007/s11829-007-9002-7]

- Esau K. (1973). Anatomia roślin. Państwowe Wydawnictwo Rolnicze i Leśne, Warszawa.
-
Evert RF. (2006). Esau’s Plant Anatomy: Meristems, Cells, and Tissues of the Plant Body – Their Structure, Function, and Development. John Wiley & Sons, Inc., Hoboken, New Jersey.
[https://doi.org/10.1002/0470047380]

-
Glover BJ and Martin C. (1998). The role of petal cell shape and pigmentation in pollination success in Antirrhinum majus. Heredity. 80:778-784.
[https://doi.org/10.1038/sj.hdy.6883450]

-
Glover BJ and Martin C. (2002). Evolution of adaptive petal cell morphology. In Cronk QCB, Bateman RM and Hawkins JA (eds.). Developmental Genetics and Plant Evolution. Taylor & Francis, London, UK. pp. 160-172.
[https://doi.org/10.1201/9781420024982.ch8]

-
Gorton HL and Vogelmann TC. (1996). Effects of epidermal cell shape and pigmentation on optical properties of Antirrhinum petals at visible and ultraviolet wavelengths. Plant Physiology. 112:879-888.
[https://doi.org/10.1104/pp.112.3.879]

- Gu C and Robertson KR. (2003). Rosa In Wu ZY and Raven PM (eds.). Flora of China 9. Science Press & Missouri Botanic Garden Press. Beijing & St. Louis, China & USA. p.368-369.
-
Hetherington AM and Woodward FI. (2003). The role of stomata in sensing and driving environmental change. Nature. 424:901-908.
[https://doi.org/10.1038/nature01843]

- Hong KP, Na CS, Jang KS, Kim HC, Park MH and Kim JS. (2001). Effects of Saengjinyanghyutang-gamibang and Rosa rugosa on the streptozotocin treated mice for induction of diabetes. Journal of Korean Oriental Medicine. 22:79-89.
-
Huang X, Lin S, He S, Lin X, Liu J, Chen R and Li H. (2018). Characterization of stomata on floral organs and scapes of cut ‘Real’ gerberas and their involvement in postharvest water loss. Postharvest Biology and Technology. 141:1-9.
[https://doi.org/10.1016/j.postharvbio.2018.04.001]

-
Hummer KE and Janick J. (2009). Rosaceae: taxonomy, economic importance, genomics. In Folta KM and Gardiner SE. (eds.). Genetics and genomics of Rosaceae. Springer. New York, USA. p.1-17.
[https://doi.org/10.1007/978-0-387-77491-6_1]

-
Kalkman C. (2004). Rosaceae. In Kubitzki K. (ed.). Flowering Plants· Dicotyledons: Celastrales, Oxalidales, Rosales, Cornales, Ericales. Springer Berlin Heidelberg. Berlin, Germany. p.343-386.
[https://doi.org/10.1007/978-3-662-07257-8_39]

-
Kay QON, Daoud HS and Stirton CH. (1981). Pigment distribution, light reflection and cell structure in petals. Botanical Journal of the Linnean Society. 83:57-83.
[https://doi.org/10.1111/j.1095-8339.1981.tb00129.x]

-
Kevan PG and Lane MA. (1985). Flower petal microtexture is a tactile cue for bees. Proceedings of the National Academy of Sciences of the United States of America (PNAS). 82:4750-4752.
[https://doi.org/10.1073/pnas.82.14.4750]

- Kim KS, Park JW, Chae SK, Kang JS and Kim BS. (2011). Study on immunosuppressive effects of Rosa chinensis Jacq. extract. Korean Journal of Oriental Physiology and Pathology. 25:459-465.
- Kim YS, Song JH, Choi GY, Lee GS and Ju YS. (2020). Comparative study on the external micro-morphology of 3 kinds of minute pollen and spore herbs(Pini Pollen, Typhae Pollen, Lygodii Spora) utilizing scanning electron microscope. Korean Journal of Herbology. 35:9-18.
- Korea Food and Drug Administration. (2021). The Korean Herbal Pharmacopoeia. 4th ed. KFDA Notification No. 2021-64. July 29 2021.
- Korea National Arboretum. (2016). Standard checklist of cultivated plants in Korea. Korea National Arboretum. Pocheon, Korea. p.1-498.
- Lee MK, Lee SH, Choi GP, Yu CY, Lee JH and Lee HY. (2003). Screening of immune enhancement activities of the extracts from Rosa rugosa Radix. Korean Journal of Medicinal Crop Science 11:13-18.
- Lee ST. (2018). Rosaceae Juss. In Flora of Korea Editorial Committee (eds.). The Genera of Vascular Plants of Korea. Hongreung Publishing Co. Seoul, Korea. p.702-746.
-
Liu R, Wang Y, Zhang Y, Liang C, Liu H, Zheng Z, Du X and Cui Z. (2022). Morphology and mass spectrometry-based chemical profiling of peltate glandular trichomes on Mentha haplocalyx Briq leaves. Food Research International. 164:112323. (cited by 2025 Oct 14).
[https://doi.org/10.1016/j.foodres.2022.112323]

-
Martin C and Glover BJ. (2007). Functional aspects of cell patterning in aerial epidermis. Current Opinion in Plant Biology. 10:70-82.
[https://doi.org/10.1016/j.pbi.2006.11.004]

-
Molina I, Bueno A, Heredia A and Domínguez E. (2023). Editorial: Plant cuticle: From biosynthesis to ecological functions. Frontiers in Plant Science 14:1154255. (cited by 2025 Oct 14).
[https://doi.org/10.3389/fpls.2023.1154255]

- Ohba H. (2001). Rosa L. In Iwatsuki K, Boufford DE and Ohba H. (eds.). Flora of Japan IIb. Kodansha Ltd. Tokyo, Japan. p.169-177.
-
Oliveira AFM, Meirelles ST and Salatino A. (2003). Epicuticular waxes from caatinga and cerrado species and their efficiency against water loss. Anais da Academia Brasileira de Ciências. 75:431-439.
[https://doi.org/10.1590/S0001-37652003000400003]

-
Park I, Yang S, Song JH and Moon BC. (2020). Dissection for floral micromorphology and plastid genome of valuable medicinal borages Arnebia and Lithospermum(Boraginaceae). Frontiers in Plant Science. 11:606463. (cited by 2025 Sep 9).
[https://doi.org/10.3389/fpls.2020.606463]

-
Pillitteri LJ and Torii KU. (2012). Mechanisms of stomatal development. Annual Review of Plant Biology. 63:591-614.
[https://doi.org/10.1146/annurev-arplant-042811-105451]

-
Potter D, Eriksson T, Evans RC, Oh S, Smedmark JEE, Morgan DR, Kerr M, Robertson KR, Arsenault M, Dickinson TA and Campbell CS. (2007). Phylogeny and classification of Rosaceae. Plant Systematics and Evolution. 266:5-43.
[https://doi.org/10.1007/s00606-007-0539-9]

- POWO. (2025). Plants of the World Online. Royal Botanic Gardens, Kew and Missouri Botanical Garden. Available online: https://powo.science.kew.org/, (accessed on 21 Aug 2025).
-
Riederer M and Schreiber L. (2001). Protecting against water loss: Analysis of the barrier properties of plant cuticles. Journal of Experimental Botany. 52:2023-2032.
[https://doi.org/10.1093/jexbot/52.363.2023]

- Rotondi A, Rossi F, Asunis C and Cesaraccio C. (2003). Leaf xeromorphic adaptations of some plants of a coastal Mediterranean macchia ecosystem. Journal of Mediterranean Ecology. 4:25-35.
- Seyedipour S and Mahdigholi K. (2024). Petal micromorphology of some Rosa species in Iran. Rostaniha. 25:123-138.
-
Sheng L, Xia W, Zang S, Zeng Y, Yuan X, Ning G, Zhang S and Feng L. (2018). Transcriptome-sequencing analyses reveal putative genes related to flower color variation in Chinese Rosa rugosa. Acta Physiologiae Plantarum. 40:62. (cited by 2025 Sep 9).
[https://doi.org/10.1007/s11738-018-2635-6]

-
Song JH, Moon BC, Choi G and Yang S. (2018). Morphological identification of Lepidii seu Descurainiae Semen and adulterant seeds using microscopic analysis. Applied Sciences-Basel. 8:2134. (cited by 2025 Sep 9).
[https://doi.org/10.3390/app8112134]

-
Song JH, Nam HH, Park I, Yang S, Chun JM, Seo YS, Kim HY, Moon B, Kang S. Moon C. Song J and Kim JS. (2024). Comparative morphology of island and inland Agastache rugosa and their gastroprotective effects in EtOH/HCl-induced gastric mucosal gastritis. Planta Medica. 90:4-12.
[https://doi.org/10.1055/a-2189-7272]

- Song JH, Yang S and Choi G. (2020a). A comparative study about the origins of Rosaceae taxa in the Pharmacopoeias of five Northeast-Asian countries. Korean Herbal Medicine Informatics. 8:97-108.
-
Song JH, Yang S and Choi G. (2020b). Taxonomic implication of leaf micromorphology using microscopic analysis: A tool for identification and authentication of Korean Piperales. Plants-Basel. 9:566. (cited by 2025 Sep 30).
[https://doi.org/10.3390/plants9050566]

-
Sulborska A, Konarska A, Matysik-Woźniak A, Dmitruk M, Weryszko-Chmielewska E, Skalska-Kamińska A and Rejdak R. (2020). Phenolic constituents of Lamium album L. subsp. album flowers: Anatomical, histochemical, and phytochemical study. Molecules. 25:6025. (cited by 2025 Oct 14).
[https://doi.org/10.3390/molecules25246025]

-
Sulborska A and Weryszko-Chmielewska E. (2014). Characteristics of the secretory structures in the flowers of Rosa rugosa Thunb. Acta Agrobotanica. 67:13-24.
[https://doi.org/10.5586/aa.2014.056]

-
Sulborska A, Weryszko-Chmielewska E and Chwil M. (2012). Micromorphology of Rosa rugosa Thunb. petal epidermis secreting fragrant substances. Acta Agrobotanica. 65:21-28.
[https://doi.org/10.5586/aa.2012.018]

-
Thao NP, Luyen BT, Tai BH, Yang SY, Cuong NX and Nam NH. (2014). Rat intestinal sucrase inhibition of constituents from the roots of Rosa rugosa Thunb. Bioorganic & Medicinal Chemistry Letters. 24:1192-1196.
[https://doi.org/10.1016/j.bmcl.2013.12.098]

-
Werker E. (2000). Trichome diversity and development. Advances in Botanical Research. 31:1-35.
[https://doi.org/10.1016/S0065-2296(00)31005-9]

-
Wessinger CA and Rausher MD. (2012). Lessons from flower colour evolution on targets of selection. Journal of Experimental Botany. 63:5741-5749.
[https://doi.org/10.1093/jxb/ers267]

-
Whitney HM, Chittka L, Bruce TJA and Glover BJ. (2009). Conical epidermal cells allow bees to grip flowers and increase foraging efficiency. Current Biology. 19:948-953.
[https://doi.org/10.1016/j.cub.2009.04.051]

-
Wu CA, Streisfeld MA, Nutter LI and Cross KA. (2013). The genetic basis of a rare flower color polymorphism in Mimulus lewisii provides insight into the repeatability of evolution. PLoS One. 8:e81173. (cited by 2025 Oct 15).
[https://doi.org/10.1371/journal.pone.0081173]

- Young HS, Park JC, Choi JS and Suh SS. (1990). Antihypertensive activity and triterpene from the underground parts of Rosa rugosa. Journal of Oriental Botanical Research. 3:83-89.
-
Yu HS, Choi JE, Woo WH and Mun YJ. (2014). The study on pharmacological activation as cosmetic material of Rosa rugosa Thunb. flowers extract. Korean Journal of Acupuncture. 31:188-194.
[https://doi.org/10.14406/acu.2014.032]

-
Žarković LD, Stanković SS, Veljić MM, Marin PD and Džamić AM. (2022). Flower micromorphology of eight wild-growing Rosa species(Rosaceae) from Serbia. Biologia. 77:351-359.
[https://doi.org/10.1007/s11756-021-00948-x]

-
Zhang Q, Wu S, Dai Q, Hu P and Chen G. (2024). Effects of different drying methods on the structural characteristics and multiple bioactivities of Rosa roxburghii Tratt fruit polysaccharides. Foods 13:2417. (cited by 2025 Oct 14).
[https://doi.org/10.3390/foods13152417]

-
Zhou H, Liu M, Yuan Y, Shalapy NM and Cui L. (2023). Rosa chinensis as edible flowers: Phytochemicals and biological effects. Journal of Future Foods. 3:357-363.
[https://doi.org/10.1016/j.jfutfo.2023.03.006]