
방사선에 의한 조혈계 장애 동물모델에서 은시호의 보호효과
Correspondence to: #Bo Kyung Jeong and Sueun Lee are contributed equally to this paper.
This is an open access article distributed under the terms of the Creative Commons Attribution Non-Commercial License (http://creativecommons.org/licenses/by-nc/3.0/) which permits unrestricted non-commercial use, distribution, and reproduction in any medium, provided the original work is properly cited.
Abstract
We evaluated the effects of Stellaria dichotoma extract (SDE) on bone marrow injury following radiation exposure in mice.
SDE improved the survival rate after lethal dose irradiation. Mice were irradiated with a sublethal dose of 5 Gy to induce severe myelosuppression. The treatments were administered ten times from 9 d before irradiation until the day of exposure. SDE administration resulted in a significant decrease in the duration of neutropenia compared to that in vehicle-treated animals. SDE significantly ameliorated the decrease in peripheral neutrophils observed in the irradiated mice experiencing myelosuppression. However, no effect was observed on lymphocyte or red blood cell levels. Notably, SDE treatment ameliorated the hypocellularity and disruption of bone marrow caused by irradiation. Furthermore, SDE reduced the radiation-induced increase in FLT3 ligand levels.
Overall, SDE treatment effectively reduced irradiation-induced myelosuppression.
Keywords:
Stellaria dichotoma Linné var., Bone marrow, Radiation, Hematopoiesis, Mice서 언
방사선 피폭에 의한 가장 일반적인 장애는 조혈계와 면역계의 장애로 알려져 있으며 특히 호중구를 포함한 백혈구의 감소로 인한 감염 위험성 증가와 혈소판 감소로 인한 출혈 소인의 증가는 치사에 이르게 되는 주요한 원인으로 알려져 있다 (Green and Rubin, 2014; Yahyapour et al., 2018; Jiao et al., 2022; Hollingsworth et al., 2023). 현재까지 골수손상에 대해 제시된 표준 치료법은 중성구 수치가 감소하는 경우 과립세포군촉진인자 (granulocyte colony-stimulating factor, G-CSF)를 투여하는 것이다 (Pellmar and Rockwell, 2005). 혈소판의 손상에 대해서는 혈소판의 성분수혈이 제시되고 있다 (Waselenko et al., 2004). 그러나 이러한 기존 치료법은 암환자의 치료 시 동반되는 혈구감소 시의 치료지침을 적용하고 있기 때문에 피폭상황에서의 적정성 여부가 재검토될 필요가 있다. 국제원자력기구 (International Atomic Energy Agency, IAEA) 및 국제적 피폭치료 가이드라인에서 골수회복을 위해 쓰도록 방침이 정해져 있으나 이러한 적용법으로는 심한 손상을 회복할 수는 없어 치료 효과에 있어 한계가 있으며, G-CSF의 효과적인 사용 방법 및 적용기준에 대한 연구가 추가적으로 필요하다 (Berger et al., 2006; Drouet and Hérodin, 2010; Dainiak et al., 2011). 더불어, 대규모 사고 시 고가의 G-CSF의 한계가 예상되므로 이를 대치 보완할 실용적 약제의 발굴이 필요하다.
그러나 이들 생물학적 제제는 고가이고, 특정 조건에서만 적용 가능하다는 한계점이 존재한다. 특히 대규모 방사선 재난 상황에서는 접근성과 실용성의 제약이 존재하기 때문에, 이를 보완할 수 있는 저독성 천연물 기반의 면역조절제 개발에 대한 필요성이 지속적으로 제기되고 있다 (Yu et al., 2022; Gamboa et al., 2024).
이러한 배경에서, 전통 의학에서 활용되어 온 약용 식물들에 대한 재조명이 이루어지고 있으며, 그 중 은시호는 중국 및 러시아에 분포하는 다년생 초본인 Stellaria dichotoma Linné var. lanceolata Bge의 뿌리로 골증열 (骨蒸熱), 허로 (虛勞), 음허발열 (陰虛發熱) 등 체내 면역 저하와 관련된 병태를 치료하는 데 사용되어 왔다 (Liu et al., 2023; Ma et al., 2024).『동의보감』 등 다수의 전통 문헌에 따르면, 은시호는 청허열 (淸虛熱)을 주요 효능으로 하며, 음혈 부족으로 인한 면역 저하 상태의 회복을 돕는 약물로 분류된다 (Heo, 2013). 한국한의학연구원에서 운영하는 전통의학정보 포털 프로그램을 활용하여 다양한 골수 손상 및 뼈 질환의 효과를 기대할 수 있을 것으로 되어있으며 한의학적 관점에서 방사선에 의한 손상은 정기 (正氣)의 손상과 음허로 인한 허열 (虛熱)의 발현으로 해석되며, 이는 은시호의 약리적 적용 가능성과 이론적으로 부합한다.
약리학적으로 은시호에는 사포닌, 플라보노이드, 폴리페놀 등 생리활성 물질이 다량 함유되어 있으며, 선행 연구에 따르면 이들 성분은 항염증, 항산화, apoptosis를 억제 효과를 통해 조직 손상 회복에 관여한다 (Bae et al., 2018; Dong et al., 2021). 특히 사포닌은 Toll-like receptor (TLR) 경로를 매개로 면역세포의 기능을 조절하고, 사이토카인 분비 및 대식세포 활성화를 유도함으로써 선천면역 및 후천면역 반응의 균형 회복에 기여할 수 있는 잠재력을 갖는다 (Wang et al., 2023).
본 연구는 방사선에 의한 골수 손상 모델에서, 은시호의 면역학적 효능과 약리학적 작용기전을 함께 탐색함으로써, 현대 의학과 전통 의학의 융합 기반 면역 회복 전략의 가능성을 평가하고자 한다. 특히 생존율, 혈구 회복, 면역세포 조절 등의 지표를 중심으로 분석함으로써, 면역학적 기전을 바탕으로 한 약리적 치료 접근과 한의학적 처방 원리 간의 상호 보완성을 실험적으로 검증하고자 한다.
재료 및 방법
1. 은시호 추출물의 제조
실험에 사용된 은시호은 광명당제약 (울산)에서 구입 하였으며, 최고야 박사 (한국한의학연구원)의 형태감별을 거쳐 실험에 사용되었다. 표본은 한국한의학연구원에 보관 중이다 (specimen no. 2-16-0191). 은시호 793 g을 잘게 절단하여 증류수 10배를 넣고 100℃에서 3시간 환류추출 후, 얻어진 추출물을 감압농축기를 사용하여 45℃에서 농축 후 동결건조기를 이용하여 추출물 331.95 g을 제조하였다 (수득율 41.86%, w/w).
2. 세포 배양
본 실험에 사용된 세포인 bone marrow-derived mouse stromal cells, OP9 세포는 American Type Culture Collection (ATCC, Manassas, VA, USA)로부터 구입하여 사용하였다. 세포는 항생제 및 항균제로서 100 U/mL의 페니실린과 100 μg/mL의 streptomycin을 첨가하고 20% FBS를 첨가한 α-MEM 배지에서 5% CO2의 습한 대기, 37℃의 온도조건으로 배양하였다.
3. 활성산소종 (Reactive Oxygen Species, ROS) 측정
은시호 추출물의 산화적 스트레스에 대한 보호 효과를 확인하기 위해 과산화수소 처리 후 세포 생존률을 확인하였다. 세포 내 ROS는 2',7'-dichlorodihydrofluorescein diacetate (DCF-DA)를 사용하여 측정하였다. OP9 세포에 은시호 추출물 (5, 10, 50, 100 μg/mL)과 1mM의 과산화수소를 각각 처리하고 24시간 배양한 후 세포를 PBS로 세척하여 100 μM DCF-DA 처리 후 37℃에서 30 분간 반응시켰다. DCF-DA를 제거한 다음 세포를 다시 PBS 로 세척한 후 형광현미경을 이용하여 세포내 DCF-DA의 양을 관찰하였다. 형광 강도는 microplate reader를 사용하여 excitation wavelength 485 nm, emission wavelength 520 nm에서 측정하였다.
4. 실험동물 및 순화
실험에 사용한 동물은 중앙실험동물에서 공급하는 C3H/ne 수컷 마우스로 주령은 8주이며, 27 ± 2 g 내외의 동물을 사용하였다. 공급업체에서 개체 모니터링 data와 외관을 확인한 후 시험을 실시하는 동물실에서 1주일 정도 순화 후 일반증상을 관찰하여 건강한 개체만을 시험에 제공하였다. 동물 사양은 한국원자력의학원의 실험동물 사양실 clean room에서 Auto controller에 의해, 온도 22 ± 1℃, 습도 50 ± 10%, 조명시간 12 Light: 12 Day cycle로 유지하며, 멸균된 사료를 3중 필터로 정수한 물과 함께 급식시켰다 (경북대학교 동물윤리위원회 승인: 2018-0070).
5. 방사선조사
방사선 조사군은 60CO 감마선을 이용하여 3.51 Gy/min의 선량율로 5 와 10 Gy를 전신 조사하였으며 대조군은 같은 과정을 가지나 감마선원을 제공하지 않았다.
6. 은시호 투여
방사선 조사군은 은시호 추출물을 체중당 50, 100 mg/kg의 용량으로 식염수에 녹여 1일 1회 경구 투여하였으며, 대조군에는 vehicle만을 같은 방법으로 주사하였다. 투여는 방사선 조사 9일 전부터 조사 당일까지 10회 투여하였다.
7. 시험군의 구성
먼저 치사용량의 방사선 (10 Gy)을 전신에 조사하고 은시호를 투여하여 마우스의 치사율을 평가하였다. 각 군당 10마리의 마우스가 치사율 평가에 사용되었다. 또한 반치사용량의 방사선 (5 Gy)을 전신에 조사하고 시간별로 그 변화를 관찰하고 방사선 피폭 후 은시호 투여에 따른 변화를 관찰하여, 은시호의 방사선 피폭 후에 치료적인 적용의 가능성을 관찰하였다. 반치사용량인 감마선 5 Gy를 전신에 조사하고 0.5, 3, 10, 21일에 마우스를 희생하였다. 마우스의 복대정맥을 통해 혈액을 채취하고 백혈구, 림프구, 혈소판, 적혈구 등의 변화를 관찰하였으며 비장의 무게 및 골수의 조직학적인 변화 등을 평가하였다 (Kim et al., 2015).
8. 시료 분석
희생시킨 마우스로부터 복대정맥에서 혈액을 채취하였으며 전혈검사를 위해 일부 혈액은 EDTA bottle에, 일부 혈액은 혈장을 분리하여 Fms-like tyrosine kinase 3 (FLT3) ligand ELISA 검사를 실시하였다. EDTA bottle에 채취한 혈액은 동물전용 자동혈구분석기인 Hemavet 950 (CDC Technologies Inc., Connecticut, USA)을 사용하여 백혈구, differential WBC count (중성구, 림프구, 호산구, 호염구, 대식세포), 적혈구, 혈소판의 빈도수를 평가하였다.
혈장성분을 이용하여 mouse FLT3 ligand (R&D Systems, Minneapolis, MN, USA)를 사용하여 키트 지침에 따라 반응시켰으며 검출항체와 효소를 이용해 발색 후 흡광도를 측정하였고, 표준곡선을 활용하여 FLT3 ligand 농도를 계산하였다.
말초혈액 변화와 대표적인 조혈 장기인 비장에서의 변화를 평가하기 위해 채혈 후 비장과 대퇴골을 적출하였다. 비장은 무게를 측정한 뒤, 비장과 대퇴골은 10% 중성완충포르말린 (10% neutral buffered formalin)에 고정하였다. 이후 일반적인 방법에 따라 파라핀 포매를 실시하고, 4 μm 두께로 절편하였다. 절편 조직은 hematoxylin & eosin (H&E) 염색을 시행하여 조직학적 변화를 관찰하였다.
9. 통계 처리
모든 데이터는 평균 ± 표준편차 (Standard Deviation, SD)로 표시하였으며, 통계분석은 일원분산분석 (One-way ANOVA) 후 Student-Newman-Keuls 사후검정을 통해 수행하였다. p < 0.05를 통계적으로 유의한 차이로 간주하였다.
결 과
1. 은시호 추출물의 항산화 효과
은시호 추출물의 항산화 활성을 확인하기 위해 DCF-DA 염색법을 사용해서 세포 내의 활성산소종의 양을 확인하였다. 1 mM 과산화수소의 처리에 의해 급격하게 증가하였던 세포 내 활성산소의 양이 은시호 추출물 투여 시 농도 의존적으로 감소되는 것을 확인할 수 있었다 (Fig. 1).
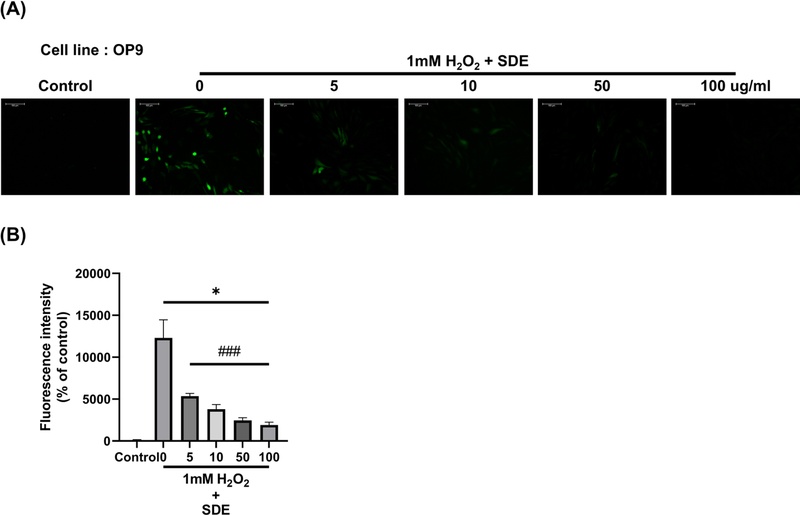
Antioxidant effect of Stellaria dichotoma extract (SDE) in OP9 cells.OP9 cells were pretreated with SDE (5, 10, 50, or 100 μg/ml) and then exposed to 1 mM H2O2. (A) Intracellular reactive oxygen species (ROS) levels were detected using 2',7'-dichlorodihydrofluorescein diacetate (DCFH-DA) staining and visualized by fluorescence microscopy. (B) Quantification of fluorescence intensity was performed using ImageJ software and expressed as a percentage of the control. Data represent mean ± SD (n = 3). * p < 0.05 vs. control; ### p < 0.001 vs. H2O2-treated group.
2. 치사용량 방사선 조사 후 생존율 지표를 적용한 은시호의 방사선 장해
10 Gy 전신 피폭 후 방사선 단독 조사군과 비교하여 은시호 투여가 생존율을 높이는 것을 확인하였다. 전신에 10 Gy의 방사선을 조사받은 군의 경우 조사 후 10일 무렵부터 사망하여 16일에 모두 사망하였다. 은시호 투여군의 경우에는 방사선 단독 조사군과 비교하여 높은 생존율을 확인하였으며 이를 통하여 방사선 피폭 시 장애 경감효과를 확인하였다 (Fig. 2).
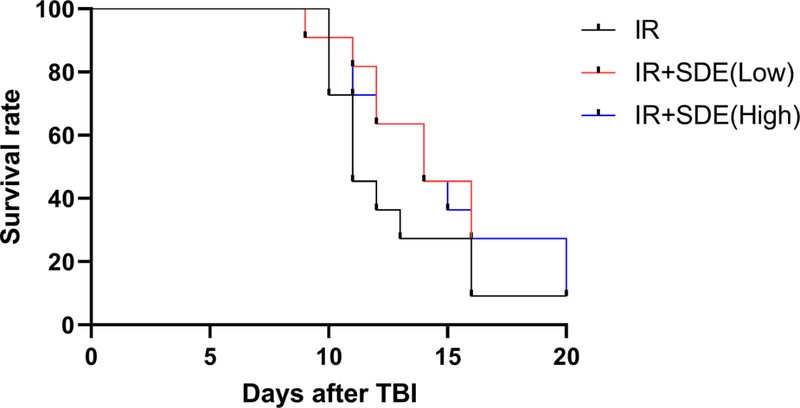
Protective effect of Stellaria dichotoma extract (SDE) on survival after lethal whole-body irradiation.Mice were treated with SDE for 10 days, starting from 9 days before whole-body γ-irradiation (IR) at 5 Gy. Survival rates were monitored daily for 20 days and analyzed by the Kaplan–Meier method. The SDE-treated group exhibited a significantly higher survival rate compared with the irradiation-only group (n = 10 per group).
3. 반치사용량 방사선 조사 후 말초혈액 변화에 대한 은시호의 치료검증
5 Gy 방사선 조사 후 말초혈액의 변화를 관찰하였다. 전체 백혈구 수는 조사 3일부터 감소하기 시작하여 21일까지 회복되지 않았다 (Fig. 3A). 조사 12시간 시점에서 호중구는 증가하는 경향을 보였으나, 림프구는 같은 시점부터 감소하는 경향을 나타냈다 (Fig. 3B, 3C). 은시호 투여군에서는 백혈구 수에서 뚜렷한 효과는 확인되지 않았으나, 호중구에서 의미 있는 변화가 나타났다. 조사 3일에는 호중구 수가 가장 크게 감소했지만, 은시호 투여군에서는 오히려 증가하는 경향을 보였으며, 10일부터는 유의한 증가가 관찰되었다 (Fig. 3B). 반면 림프구 수는 은시호 투여에 따른 차이가 없어, 은시호의 효과가 림프구 변화보다는 백혈구 수 회복을 통한 작용임을 확인할 수 있었다 (Fig. 3C).
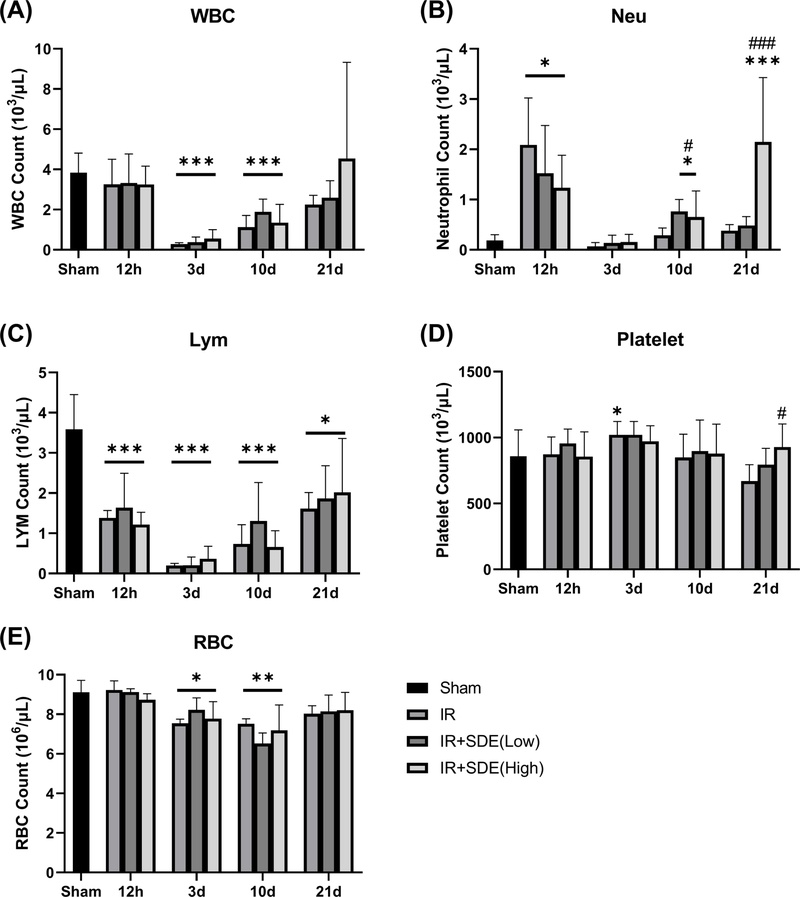
Effect of Stellaria dichotoma extract (SDE) on hematopoietic recovery after sublethal whole-body irradiation.Mice were treated with SDE for 10 days, starting from 9 days before whole-body γ-irradiation (IR) at 5 Gy. Peripheral blood counts were analyzed at days 3, 10, and 21 post-irradiation, including (A) white blood cells (WBC), (B) neutrophils (Neu), (C) lymphocyte (Lym), (D) platelets, and (E) red blood cells (RBC). Data represent mean ± SD (n = 6 per group). * p < 0.05, ** p < 0.01, *** p < 0.001 vs. sham group; # p< 0.05, ### p < 0.001 vs. IR only group.
혈소판의 경우 방사선 조사 후 10일째에서 증가가 나타났으며, 이는 백혈구 변화보다 늦게 관찰되었다. 특히 조사 21일에는 은시호 고용량 투여군에서 방사선 조사군에 비해 혈소판 수가 유의하게 증가하였다 (Fig. 3D). 방사선 단독 조사군에서는 RBC 수치가 조사 3일째부터 급격히 감소하였으며, 특히 10일째에서 가장 뚜렷한 저하가 관찰되었다. 반면 은시호 투여군에서는 RBC 수치에 유의한 변화가 나타나지 않았다 (Fig. 3E).
이러한 결과는 은시호 추출물이 방사선에 의해 유발되는 조혈 억제 및 면역계 손상을 효과적으로 완화하며, 특히 호중구의 보존 및 회복을 촉진할 수 있음을 시사한다.
4. 비장의 무게감소의 회복
5 Gy 방사선 조사 후 체중에서는 대조군과 비교하여 뚜렷한 변화가 관찰되지 않았다 (Fig. 4A). 그러나 비장 무게는 조사 12시간부터 감소하기 시작하여 21일까지 대조군에 비해 유의하게 낮았으며, 이 시점까지도 정상 수준으로 회복되지 않았다 (Fig. 4B).
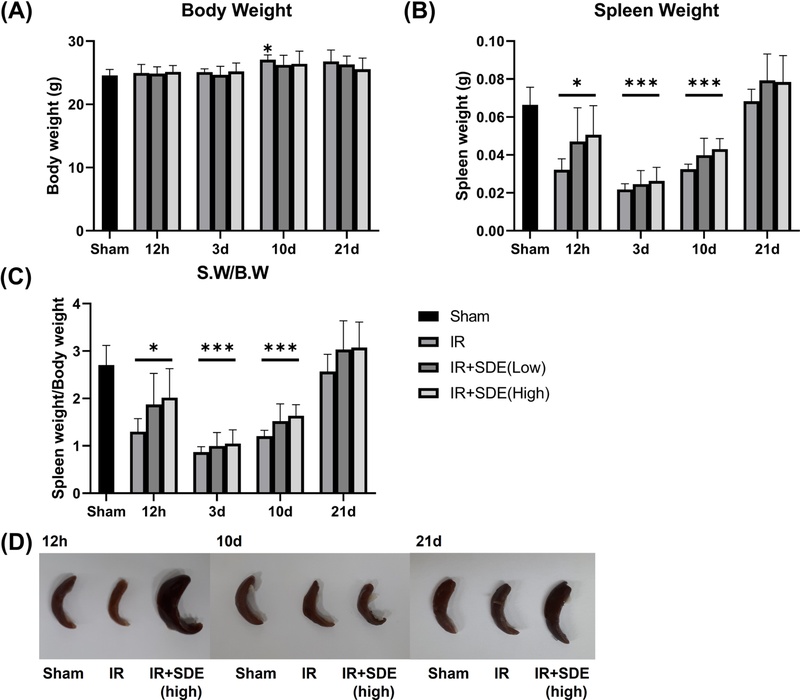
Effect of Stellaria dichotoma extract (SDE) on spleen recovery after sublethal whole-body irradiation.Before 5 Gy γ- irradiation (IR), mice were treated with SDE for 10 days, with the treatment ending on the day of irradiation. Body weight (A), Sspleen weights (B), and spleen weight/body weight (S.W/B.W; C) were measured on days 3, 10, and 21 post-irradiation. (D) Representative spleen images demonstrate enhanced spleen size recovery in SDE-treated groups compared with the irradiation-only group. Data are presented as mean ± SD (n = 6 per group). * p < 0.05, *** p < 0.001 vs. sham group.
은시호 투여군에서는 조사 12시간부터 10일까지 방사선 단독 조사군에 비해 비장 무게가 증가하는 경향을 보였으나, 유의성은 없었다. 다만 21일 이후에는 정상 수준을 넘어서는 증가가 확인되었다. 특히 은시호 고용량 투여군에서는 조사 12시간부터 비장 크기의 증가가 관찰되었다 (Fig. 4D).
5. 은시호의 방사선 조사 후 골수의 세포충실도 치료 검증 및 혈장 FLT3 ligand 발현 조절 효과
골수 조직학적 평가에서 방사선 단독군은 세포충실도(cellularity)의 현저한 감소와 조혈세포 밀도의 붕괴가 관찰되었다. 그러나 은시호 투여군에서는 이러한 감소가 완화되었으며, 특히 조사 3일 시점에서 최저치를 보인 방사선 단독군에 비해 유의하게 높은 세포충실도를 확인할 수 있었다 (Fig. 5A).
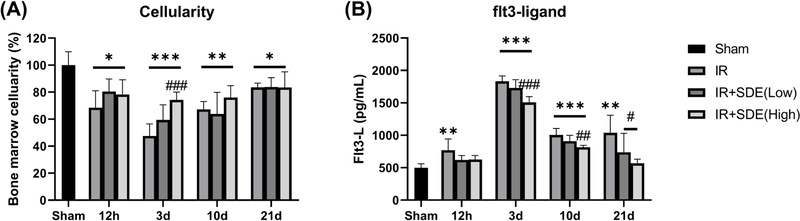
Effect of Stellaria dichotoma extract (SDE) on plasma Fms-related tyrosine kinase 3 (FLT3) ligand levels after irradiation.For 10 days, from 9 days before to the day of 5 Gy whole-body γ-irradiation (IR), mice were given oral doses of SDE. (A) Cellularity of Bone marrow was analyzed at days 3, 10, and 21 post-irradiation. (B) Plasma concentrations of FLT3 ligand were measured at 12h, 3d, 10d, and 21d after irradiation. Data are presented as mean ± SD (n = 6 per group). * p < 0.05, ** p < 0.01, *** p < 0.001 vs. sham group; # p < 0.05, # p < 0.01, ### p < 0.001 vs. IR only group.
방사선 조사 후 혈장 내 FLT3 ligand 농도는 sham 군에 비해 유의하게 증가하였고, 이는 조혈 전구세포의 동원과 분화가 촉발되었음을 시사한다. IR 단독군에서는 조사 12시간 이후부터 FLT3 ligand가 증가한 반면, 은시호 투여군에서는 방사선 조사 3일 이후부터 증가가 관찰되었으며, 동일 시점에서 IR 단독군보다 유의하게 낮은 수준을 유지하였다. 이러한 결과는 은시호가 방사선 조사 후 FLT3 ligand 발현을 억제함으로써 골수 세포충실도의 회복을 촉진하는 효과를 가질 수 있음을 시사한다 (Fig. 5B).
고 찰
본 연구는 전신 방사선 조사로 유도된 조혈기 및 면역계 손상 모델을 통해 전통 한약재 은시호의 생리학적 회복 효과를 평가하였다. 은시호는 골수세포의 산화적 스트레스 반응에 강력한 항산화 효과를 확인할 수 있었다.
10 Gy 치사용량 조사에서는 대조군에서 대부분 개체가 14일 이내 사망한 반면, 은시호 투여군에서는 생존율이 유의하게 향상되어 방사선 손상에 대한 보호 효과를 시사하였다 (Fig. 2). 5 Gy 반치사용량 조사 후 백혈구 및 호중구 수가 급감한 가운데, 은시호 투여군은 10일 및 21일 시점에서 유의한 회복 양상을 보였다 (Fig. 3). 혈소판 회복도 비교적 빠르게 나타났으며, 이는 은시호가 조혈모세포 및 전구세포의 생존 및 분화에 긍정적으로 작용했음을 시사한다. 비장 무게는 방사선 조사 후 감소했으나, 은시호 투여군에서는 점진적인 회복이 관찰되었으며 (Fig. 4), 이는 면역세포 재구성과 조직 회복이 진행되었음을 의미한다. 반면 림프구 회복은 상대적으로 미미하여, 은시호가 주로 골수계 회복에 작용함을 시사한다.
방사선 조사 후 FLT3 ligand 농도는 일시적으로 증가하였으나 점차 감소하는 양상을 보였다. 반면, 은시호 투여군에서는 FLT3 ligand 농도가 유의하게 더 높게 유지되었으며 감소 속도도 완만하였다. 이는 은시호가 FLT3 ligand 발현을 촉진하여 조혈 회복을 가속화하고 방사선 손상으로부터 보호 효과를 제공함을 시사한다. 따라서 은시호는 방사선 유도성 조혈 억제에 대한 잠재적 치료 인자로 활용될 수 있을 것이다.
흥미롭게도, 은시호는 림프구 수 변화에는 제한적인 영향을 보였으며, 이는 해당 약물이 주로 골수계 (myeloid lineage) 중심의 면역세포 회복에 작용함을 시사한다. 이러한 선택적 면역 회복 특성은 향후 림프계 회복을 위한 면역보조제와의 병합 치료 가능성을 제시한다 (Bakos et al., 2018; Venet et al., 2021). 림프구 재건의 지연은 방사선 손상 후 감염 민감도를 증가시키고, 장기적 면역 기능 저하로 이어질 수 있기 때문에, 은시호의 선택적 작용 양상은 병용 요법 설계 측면에서 중요한 단서를 제공한다 (Kusunoki and Hayashi, 2008; Wirsdörfer and Jendrossek, 2016; Hollingsworth et al., 2023).
한약적으로 은시호는 청허열 (淸虛熱) 및 보음 (補陰) 작용을 통해 열성 소모성 질환에 사용되어 왔으며, 이러한 효능은 방사선 손상 후 나타나는 음허 증상 및 전신 면역 저하 상태와 병태적 유사성을 갖는다. 본 실험 결과에서 은시호가 세포자멸사 억제, 항산화 및 항염작용을 통해 조직 손상을 완화하고 조혈 기능을 회복시킨 것은, 전통 효능에 대한 현대 약리학적 근거를 제공하는 결과라 할 수 있다 (Bae et al., 2018; Dong et al., 2021).
한편, 은시호 투여군에서는 전통적 청허열 (淸虛熱), 보음 (補陰) 효능에 부합하는 생리적 반응으로써, 조혈 회복 지연 억제 및 염증성 반응 완화가 관찰되었다. 특히 은시호는 실험적으로 apoptosis 억제, 항산화, 항염증 작용 등이 보고된 바 있으며, 이러한 생리활성이 방사선 손상으로 인한 세포 손상 및 면역 억제에 대하여 보호 및 회복 효과를 나타낼 가능성이 있다. 또한, 은시호가 가진 항염 기전은 조직 내 IL-6, TNF-α와 같은 염증성 사이토카인의 발현을 억제하고, 과도한 면역 반응으로 인한 2차 손상을 줄이는 데 기여할 수 있다 (Bae et al., 2018; Zhou et al., 2023). 이는 방사선 치료 후 나타나는 만성 염증과 그로 인한 조직 섬유화 예방 측면에서도 은시호의 가능성을 시사한다.
결론적으로, 은시호는 방사선 손상에 따른 생존율 저하, 조혈 기능 억제, 면역 장기 위축 등 복합적인 병태 생리에 대해 다면적인 회복 효과를 보였으며, 이는 은시호가 천연물 기반 면역조절제 및 조직 보호제로서 활용될 수 있는 가능성을 제시한다. 향후에는 은시호의 주요 유효 성분 규명, 세포 및 분자 수준의 작용 기전 분석, 그리고 기존 방사선 회복제와의 병용 효과에 대한 체계적 연구가 필요하다. 특히, 선별된 유효 성분 (예: 사포닌 하위군, 특정 플라보노이드 등)의 조혈세포에 대한 직접적인 작용 여부, 면역세포 분화 경로에서의 신호 전달 메커니즘 (SCF/c-Kit, IL-3, GM-CSF pathway 등)에 대한 분석은 학술적·임상적으로 매우 중요한 후속 연구 과제가 될 수 있다.
이를 통해 은시호는 재난 대비 또는 임상 방사선치료 보조제로서의 실용성을 한층 더 확보할 수 있을 것이다. 더불어, 환자의 체력 상태나 병태 조건에 따른 한의학적 변증-처방 체계를 병행한 맞춤형 치료 접근은 통합의학적 적용 가능성을 넓히는 방향이 될 수 있으며, 향후 임상시험을 통한 검증도 반드시 필요하다.
Acknowledgments
This work was supported by a grant from Korea Institute of oriental medicine (ERT2011180 and KSN2511030) and Regional Innovation System & Education (RISE) through the Gwangju RISE Center, funded by the Ministry of Education (MOE) and the Gwangju Metropolitan government (20250527000003426624).
References
-
Bae SJ, Choi JW, Park BJ, Lee J, Jo EK, Lee YH, Kim SB and Yuk JM. (2018). Protective effects of a traditional herbal extract from Stellaria dichotoma var. lanceolata against Mycobacterium abscessus infections. PLoS One, 13:e0207696.
[https://doi.org/10.1371/journal.pone.0207696]

-
Bakos O, Lawson C, Rouleau S and Tai LH. (2018). Combining surgery and immunotherapy: Turning an immunosuppressive effect into a therapeutic opportunity. Journal for ImmunoTherapy of Cancer. 6:86. https://jitc.bmj.com/content/6/1/86, (cited by 2025 Aug. 10).
[https://doi.org/10.1186/s40425-018-0398-7]

-
Berger ME, Christensen DM, Lowry PC, Jones OW and Wiley AL. (2006). Medical management of radiation injuries: Current approaches. Occupational Medicine. 56:162-172.
[https://doi.org/10.1093/occmed/kql011]

-
Dainiak N, Gent RN, Carr Z, Schneider R, Bader J, Buglova E, Chao N, Coleman CN, Ganser A, Gorin C, Hauer-Jensen M, Huff LA, Lillis-Hearne P, Maekawa K, Nemhauser J, Powles R, Schünemann H, Shapiro A, Stenke L, Valverde N, Weinstock D, White D, Albanese J and Meineke V. (2011). First global consensus for evidence-based management of the hematopoietic syndrome resulting from exposure to ionizing radiation. Disaster Medicine and Public Health Preparedness. 5:202-212.
[https://doi.org/10.1001/dmp.2011.68]

-
Dong L, Zhou X, Ma J, Zhou H and Fu X. (2021). Chemical constituents of Stellaria dichotoma var. lanceolata and their anti-inflammatory effect on lipopolysaccharide-stimulated RAW 264.7 Cells. Chemistry of Natural Compounds. 57:158-162.
[https://doi.org/10.1007/s10600-021-03306-0]

-
Drouet M and Hérodin F. (2010). Radiation victim management and the haematologist in the future: Time to revisit therapeutic guidelines? International Journal of Radiation Biology. 86:636-648.
[https://doi.org/10.3109/09553001003789604]

-
Farese AM, Hunt P, Grab LB and MacVittie TJ. (1996). Combined administration of recombinant human megakaryocyte growth and development factor and granulocyte colony-stimulating factor enhances multilineage hematopoietic reconstitution in nonhuman primates after radiation-induced marrow aplasia. The Journal of Clinical Investigation. 97:2145-2151.
[https://doi.org/10.1172/JCI118652]

-
Gamboa J, Lourenço P, Cruz C and Gallardo E. (2024). Aptamers for the delivery of plant-based compounds: A review. Pharmaceutics. 16(4):541. https://www.mdpi.com/1999-4923/16/4/541, (cited by 2025 Aug. 10).
[https://doi.org/10.3390/pharmaceutics16040541]

-
Green DE and Rubin CT. (2014). Consequences of irradiation on bone and marrow phenotypes, and its relation to disruption of hematopoietic precursors. Bone. 63:87-94.
[https://doi.org/10.1016/j.bone.2014.02.018]

- Heo J. (2013). Donguibogam(Vol. 3). Ministry of Health and Welfare. Seoul, Korea.
-
Hollingsworth BA, Aldrich JT, Case CM Jr, DiCarlo AL, Hoffman CM, Jakubowski AA, Liu Q, Loelius SG, PrabhuDas M, Winters TA and Cassatt DR. (2023). Immune dysfunction from radiation exposure. Journal of Radiation Research. 200:396-416.
[https://doi.org/10.1667/RADE-22-00004.1]

-
Jiao Y, Cao F and Liu H. (2022). Radiation-induced cell death and its mechanisms. Health Physics. 123:376-386.
[https://doi.org/10.1097/HP.0000000000001601]

-
Kim JS, Jang WS, Lee S, Son Y, Park S and Lee SS. (2015). A study of the effect of sequential injection of 5-androstenediol on irradiation-induced myelosuppression in mice. Archives of Pharmacal Research. 38:1213-22.
[https://doi.org/10.1007/s12272-014-0483-5]

-
Kusunoki Y and Hayashi T. (2008). Long-lasting alterations of the immune system by ionizing radiation exposure: implications for disease development among atomic bomb survivors. International Journal of Radiation Biology. 84:1-14.
[https://doi.org/10.1080/09553000701616106]

-
Liu W, Qiu K, Huang Y, Li Y and Zhang S. (2023). Molecular organization of the chloroplast genome and taxonomic position of Stellaria dichotoma var. lanceolate. Cytology and Genetics. 57:174-185.
[https://doi.org/10.3103/S0095452723020081]

-
Ma M, Zhan M, Mo X, Quan H and Dong L. (2024). Chemical constituents and anti-anxiety active sites from Stellaria dichotoma var. lanceolata. Chemistry of Natural Compounds. 60:798-802.
[https://doi.org/10.1007/s10600-024-04448-7]

-
Martínez C, Urbano-Ispizua A, Rozman C, Marín P, Mazzara R, Carreras E, Rovira M, Sierra J, Briones J, Ordinas A and Montserrat E. (1996). Effects of G-CSF administration and peripheral blood progenitor cell collection in 20 healthy donors. Annals of Hematology. 72:269-272.
[https://doi.org/10.1007/s002770050171]

-
Odell TT, Jackson CW and Friday TJ. (1971). Effects of radiation on the thrombocytopoietic system of mice. Radiation Research. 48:107-115.
[https://doi.org/10.2307/3573399]

-
Pellmar TC and Rockwell S. (2005). Priority list of research areas for radiological nuclear threat countermeasures. Radiation Research. 163:115-123.
[https://doi.org/10.1667/RR3283]

- Seo YS, Park G, Lim HS, Moon BC and Kim JS. (2020). Protective effect of Byeol Gab extract in radiation induced testicular injury. Korean Herbal Medicine Informatics. 8:13-24.
-
Son Y, Bae MJ, Lee CG, Jo WS, Kim SD, Yang K, Jang H and Kim JS. (2014). Treatment with granulocyte colony-stimulating factor aggravates thrombocytopenia in irradiated mice. Molecular & Cellular Toxicology. 10:311-317.
[https://doi.org/10.1007/s13273-014-0035-6]

-
Takamatsu Y, Jimi S, Sato T, Hara S, Suzumiya J and Tamura K. (2007). Thrombocytopenia in association with splenomegaly during granulocyte–colony-stimulating factor treatment in mice is not caused by hypersplenism and is resolved spontaneously. Transfusion. 47:41-49.
[https://doi.org/10.1111/j.1537-2995.2007.01061.x]

-
Venet F, Demaret J, Gossez M and Monneret G. (2021). Myeloid cells in sepsis-acquired immunodeficiency. Annals of the New York Academy of Sciences. 1499:3-17.
[https://doi.org/10.1111/nyas.14333]

-
Wang H, Li H, Li Z, Feng L and Peng L. (2023). Evaluation of prebiotic activity of stellariae radix polysaccharides and its effects on gut microbiota. Nutrients. 15:4843. https://www.mdpi.com/2072-6643/15/22/4843, (cited by 2025 Aug. 10).
[https://doi.org/10.3390/nu15224843]

-
Waselenko JK, MacVittie TJ, Blakely WF, Pesik N, Wiley AL, Dickerson WE, Tsu H, Confer DL, Coleman CN, Seed T, Lowry P, Armitage JO and Dainiak N. (2004). Medical management of the acute radiation syndrome: Recommendations of the Strategic National Stockpile Radiation Working Group. Annals of Internal Medicine. 140:1037-1051.
[https://doi.org/10.7326/0003-4819-140-12-200406150-00015]

-
Wirsdörfer F and Jendrossek V. (2016). The role of lymphocytes in radiotherapy-induced adverse late effects in the lung. Frontiers in Immunology. 7:591.
[https://doi.org/10.3389/fimmu.2016.00591]

-
Yahyapour R, Amini P, Rezapour S, Cheki M, Rezaeyan A Farhood B, Shabeeb D, Musa AE, Fallah H and Najafi M. (2018). Radiation-induced inflammation and autoimmune diseases. Military Medical Research. 5:9.
[https://doi.org/10.1186/s40779-018-0156-7]

-
Yu S, Wang Y, He P, Shao B, Liu F, Xiang Z, Yang T, Zeng Y, He T, Ma J, Wang X and Liu L. (2022). Effective combinations of immunotherapy and radiotherapy for cancer treatment. Frontiers in Oncology. 12:809304.
[https://doi.org/10.3389/fonc.2022.809304]

-
Zhou X, Quan H, Zang L and Dong L. (2023). Dichotomine B attenuates neuroinflammatory responses by regulating TLR4/MyD88-mTOR signaling pathway in BV2 Cells. Neurochemical Research. 48:2451-2462.
[https://doi.org/10.1007/s11064-023-03920-0]
