Online LC-radical 소거능 측정 시스템을 활용한 자생 활엽수 잎의항산화 활성 성분 탐색
This is an open access article distributed under the terms of the Creative Commons Attribution Non-Commercial License (http://creativecommons.org/licenses/by-nc/3.0/) which permits unrestricted non-commercial use, distribution, and reproduction in any medium, provided the original work is properly cited.
Abstract
Antioxidant compounds have been reported to be effective in preventing and improving various diseases, including cancer and neurodegenerative diseases. In this study, an online liquid chromatography (LC) radical scavenging ability measurement system was used to explore the antioxidant compounds present in the leaf extracts of five broad-leaved tree species native to the Jeonnam region.
Ultraviolet (UV) absorption spectra and LC-mass spectrometry (LC-MS) analyses were performed on 2,2'-azino-bis(3-ethylbenzothiazoline-6-sulfonic acid) (ABTS) and 1,1-diphenyl-2-picrylhydrazyl (DPPH) radical-scavenging active compound peaks identified in the measurement system. In Morus alba leaf extract, 3-caffeoylquinic acid, 4-caffeoylquinic acid, and isoquercitrin were identified as the major active compounds. In Eriobotrya japonica leaf extract, 5-caffeoylquinic acid, 3-caffeoylquinic acid, and epicatechin were identified. In Dendropanax morbiferus and Kalopanax septemlobus leaf extracts, 3-caffeoylquinic acid was identified as the major active compound, and in Crataegus pinnatifida leaf extract, epicatechin was identified as the major active compound.
The online LC-radical scavenging ability measurement and compound analysis method used in this study can be applied to study the antioxidant activities in other plant materials. In particular, it can be a useful method for screening analyses in the early stages of research and development.
Keywords:
Antioxidant, Crataegus pinnatifida, Dendropanax morbiferus, Eriobotrya japonica, Kalopanax septemlobus, Morus alba서 언
DNA나 세포막, 단백질 손상 등을 일으키는 것으로 알려진 활성산소 (reactive oxygen species)는 인체 내에서 에너지를 만드는 과정 중 발생되며, 정상 범위를 벗어나는 수준으로 증가하게 되면 염증반응이나 피부노화, 신경퇴행성 질환, 고혈압, 암 등 각종 질환에 해로운 영향을 미치는 것으로 다양한 연구에서 밝히고 있다 (Wiseman and Halliwell, 1996; Dhalla et al., 2000; Zhang et al., 2000; Devasagayam et al., 2004; Valko et al., 2007; Schieber and Chandel, 2014).
활성산소에 대응하기 위한 항산화 소재나 성분의 탐색에 있어서 각종 식물의 추출물을 대상으로 하는 연구가 지속적으로 진행되고 있으며, 항염증이나 미백 활성 등 다른 생리활성과 연관성이 높은 것으로 나타난 소재나 성분이 다양하게 보고되고 있다 (Amin et al., 2009; Song and Lee, 2015; Kim et al., 2018; Kim et al., 2019; Yoo et al., 2019; Im and Lee, 2020; Kim et al., 2020). 최근에는 대장암 등 암과 심혈관 질환에 대한 항산화 활성 성분의 효과와 알츠하이머(Alzheimer)와 같은 신경퇴행성 질환에 대한 긍정적인 효과, 그리고 치주 질환에 대한 효과 등 다양한 분야의 질환에 대한 예방 및 치료 효과를 항산화 활성 성분이 나타내는 것으로 보고되었다 (Choi et al., 2012; Griffiths et al., 2016; Amato et al., 2019; Condello and Meschini, 2021; Maccioni et al., 2022; Farhan et al., 2023; Hatami et al., 2023; Juiz et al., 2024).
식물 추출물과 같은 천연물의 항산화 활성 연구에서 가장 일반적으로 활용되고 있는 측정방법은 2,2'-azino-bis(3-ethylbenzothiazoline-6-sulfonic acid) (ABTS)와 1,1-diphenyl-2-picrylhydrazyl (DPPH)과 같은 물질을 이용한 radical 소거 활성을 측정하는 것으로서 분광광도계와 같은 장비를 사용하여 비교적 단시간에 활성의 측정이 가능하며, 결과 비교가 용이한 장점을 가지고 있다 (Li and Jeong, 2015; Kim et al., 2019). 다만 시료가 식물 추출물과 같이 많은 성분이 혼합된 형태일 경우 여러 성분의 활성이 병합되어 나타나므로 활성 성분을 구체적으로 확인하기 위해서는 추가적인 분리 및 확인 과정이 필요하게 된다.
이런 부분에 대한 해결방안의 하나로 liquid chromatography (LC)를 이용하여 추출물의 성분을 분리시킨 후 radical 용액과 반응시키는 online LC-radical 소거능 측정 시스템이 지속적으로 활용되고 있다 (Inoue et al., 2012; Zhang et al., 2015; Im et al., 2017). Online LC-radical 소거능 측정 결과로 활성이 확인된 성분에 대하여 추가로 mass spectrometry (MS)나 nuclear magnetic resonance (NMR) 분석을 연동해서 실시함으로써 활성 성분에 대한 정성이 용이한 장점도 가지고 있다 (Braham et al., 2020; Lee et al., 2023; Lee et al., 2024a; Lee et al., 2024b; Park et al., 2024).
본 연구에서는 식품공전에서 잎 부위를 식품에 사용할 수 있거나 특별한 사용조건 없이 제한적으로 사용할 수 있도록 허용되어 있어서 안전성이 인정되는 것으로 판단할 수 있는 식물 원료 중 전남 지역에서 자생하고 있는 뽕나무 (Morus alba), 음나무 (Kalopanax septemlobus), 비파나무 (Eriobotrya japonica), 황칠나무 (Dendropanax morbiferus), 산사나무 (Crataegus pinnatifida) 5 종의 활엽수 잎 추출물을 대상으로 online LC-radical 소거능 측정 시스템을 활용하여 각 추출물에 존재하는 항산화 활성 성분에 대한 탐색을 실시하였다. 각 추출물에 대하여 ABTS와 DPPH radical 소거 활성을 LC 분리·분석과 동일한 조건에서 측정한 후 확인된 radical 소거 활성 성분 peak에 대해 LC-MS 분석을 실시하여 활성성분을 구체적으로 확인하였으며, 주요 활성 성분에 대한 정량분석을 실시하여 함량을 비교하였다.
재료 및 방법
1. 식물재료 및 시약
뽕나무, 산사나무, 음나무의 잎 시료는 전남 나주 지역에 자생하는 나무에서 성숙한 잎을 2024년 6월에 채집하였으며, 비파나무, 황칠나무의 잎 시료는 전남 장흥 지역에 자생하는 나무에서 성숙한 잎을 2024년 4월에 채집하여 사용하였다. 각 활엽수의 잎 시료는 정제수로 세척 후 수분이 15% 이하가 되도록 50℃의 건조기 (WOF-155, Daihan, Wonju, Korea)에서 24 시간 동안 가열건조하였으며, 건조 후 각 시료는 No. 10 표준체 (DH.Si8027, Daihan, Wonju, Korea)를 통과할 수 있도록 직경 2 ㎜ 이하로 분쇄하였다.
측정 및 분석에 사용된 용매는 LC grade의 Duksan Pure Chemical (Seoul, Korea) 제품을 사용하였으며, chlorogenic acid (3-caffeoylquinic acid), cryptochlorogenic acid (4-caffeoylquinic acid), neochlorogenic acid (5-caffeoylquinic acid), epicatechin, rutin, isoquercitrin 표준품은 Sigma-Aldrich (St. Louis, MO, USA)에서 구입한 것을 사용하였다.
2. 추출물 제조
분쇄된 각 잎 시료 5 g에 95% 에탄올 95 ㎖를 혼합한 후 분당 180 회의 속도를 적용하여 24 시간 동안 상온에서 진탕 추출을 실시하였다. 추출액은 0.45 ㎛ syringe filter (Whatman, Maidstone, England)로 여과를 실시한 후 실험에 사용하였다.
3. Online LC-radical 소거능 측정
각 추출물의 online LC-radical 소거능 측정에는 Elite LaChrom (Hitachi, Tokyo, Japan) LC와 column으로서 ZORBAX Eclipse XDB-C18 (4.6 ㎜ × 250 ㎜, 5 ㎛, Agilent, Santa Clara, CA, USA)을 사용하였다. 이동상으로 0.1% formic acid를 함유한 water (A)와 acetonitrile (B)을 사용하였으며, 이동상 세부 조건은 Table 1과 같이 적용하였다. Column oven은 35℃를 유지하였으며, 각 radical 소거능과 LC profile 분석을 위한 시료 주입량은 10 ㎕를 적용하였다.
Column 분리 이후에 radical 용액을 공급하기 위해 추가로 LC-20AD pump (Shimadzu, Kyoto, Japan)를 설치하였다. Column에서 분리된 시료액과 radical 용액이 혼합된 이후 차광이 되는 재질의 reaction tubing 1 m를 지나면서 활성 성분의 radical 소거 반응이 나타나도록 하였다.
DPPH radical 소거능 측정에는 methanol에 50 μM로 용해시킨 DPPH 용액을 사용하였으며, radical 용액 pump의 유속은 0.2 ㎖/min으로 유지하면서 517 ㎚에서 측정을 실시하였다.
ABTS radical 소거능 측정에는 7.4 mM ABTS와 2.6 mM potassium persulfate를 혼합 후 상온, 암소에서 4 시간 동안 방치하여 형성된 radical을 측정 직전에 730 ㎚에서 흡광도가 0.7 ± 0.05가 되도록 증류수로 희석한 용액을 사용하였다. Radical 용액 pump의 유속은 0.2 ㎖/min으로 유지하면서 730 ㎚에서 검출을 수행하였다.
활성 성분의 확인을 위한 LC profile 분석은 radical 용액의 공급을 정지한 상태에서 254 ㎚ 검출 파장을 적용하여 실시하였으며, radical 소거 활성 성분 peak의 UV 흡수 spectrum은 200 ㎚ - 400 ㎚ 범위에서 측정하였다.
4. 주요 radical 소거 활성 성분의 LC-MS 분석
각 추출물의 online LC-radical 소거능 측정에서 확인된 주요 활성 성분 peak에 대한 질량분석은 LCMS-8050 (Shimadzu, Kyoto, Japan)를 사용해 측정하였으며, online LC-radical 소거능 측정과 동일한 이동상 및 column 조건을 적용하였다.
MS 분석은 electrospray ionization (ESI) 방법을 적용하였으며, interface, desolvation line, heat block 온도는 각각 350℃, 250℃, 380℃로 설정하였다. Nebulizing gas, drying gas, heating gas는 각각 3 ℓ/min, 10 ℓ/min, 10 ℓ/min을 적용하였으며, positive와 negative mode에서 100 m/z - 1,000 m/z의 범위의 MS scan 분석을 실시하였다.
5. 주요 radical 소거 활성 성분 함량 분석
각 추출물의 주요 radical 소거 활성 성분의 함량 분석은 online LC-radical 소거능 측정과 동일한 기기 및 column 조건에서 실시하였다. 이동상으로 0.1% formic acid를 함유한 water (A)와 acetonitrile (B)을 사용하였으며, online LC-radical 소거능 측정 결과에 확인된 radical 소거 활성 성분의 머무름시간이 분석 시간 초반에 나타난 결과를 반영하여 이동상 세부 조건은 Table 2와 같이 적용하였다.
시료 주입량은 10 ㎕, radical 소거 활성 성분의 정량분석을 위한 표준품 용액은 500 ㎍/㎖, 250 ㎍/㎖, 100 ㎍/㎖, 50 ㎍/㎖, 25 ㎍/㎖, 10 ㎍/㎖ 농도로 조제하여 분석에 사용하였으며, 검출기 파장은 6 종 성분을 동시에 분석하기 위해서 280 ㎚로 설정하였다.
결과 및 고찰
1. Online LC-radical 소거능
ABTS radical과 DPPH radical 소거능 측정은 각 radical 물질과 소거 활성 성분이 반응하여 색상의 변화 정도를 분광기기로 측정하는 단순한 절차와 결과의 비교가 용이하다는 장점으로 인해 항산화 활성 관련 연구에서 가장 많이 이용되고 있다 (Cha, 2015; Li and Jeong, 2015; Im et al., 2017; Kim et al., 2019). ABTS는 양이온 radical을, DPPH는 음이온 radical을 생성하는 차이가 있으므로 각 소거능 측정 방법에서 기질과 반응물질의 결합 정도가 서로 달라 측정 결과가 상이할 수 있다고 알려져 있다 (Lee et al., 2012). 또한 알콜과 같은 유기용매에 더 잘 용해되는 DPPH radical에 비해 ABTS radical이 물 또는 유기용매 모두에 용해되므로 강하기 때문에 극성 및 비극성 시료 모두에서 항산화 활성 측정이 용이하다는 차이가 있다 (Awika et al., 2003).
LC를 사용한 분리·분석과 연동시켜 radical 소거능을 측정하는 online LC-radical 소거능 측정 시스템에서는 LC의 column 분리 이후 검출기로 연결되는 중간에 radical 용액을 공급하게 되므로 항산화 활성 성분이 분리되어 나오는 시간 영역에서만 radical 소거 반응으로 인한 흡광도 변화가 나타나게 된다. Fig. 1 – Fig. 5의 (A), (B)에 제시된 것과 같이 각 radical이 항산화 활성 성분을 만나게 되면 radical 고유의 색상이 탈색되면서 흡광도가 낮아지게 되어 baseline을 기준으로 아래 방향의 peak를 형성하게 된다. 일부 연구에서는 검출기의 polarity를 반대로 전환하여 측정함으로써 일반적인 LC의 chromatogram과 같은 형상으로 표시한 예도 있었으나 (Im et al., 2017; Lee et al., 2023), 일반적으로는 본 연구에서와 같이 항산화 활성 성분과 반응하여 고유의 색상이 탈색되는 radical의 특성이 그대로 반영될 수 있도록 표시하고 있다 (Hong et al., 2014; Braham et al., 2020; Lee et al., 2022; Lee, 2023; Lee et al., 2024a; Lee et al., 2024b; Park et al., 2024). 활성이 높은 성분이거나 해당 성분의 함량이 높으면 상대적으로 peak 면적이 크게 나타나게 되므로 각 추출물 중에 포함된 주요 활성 성분을 확인할 수 있게 된다.
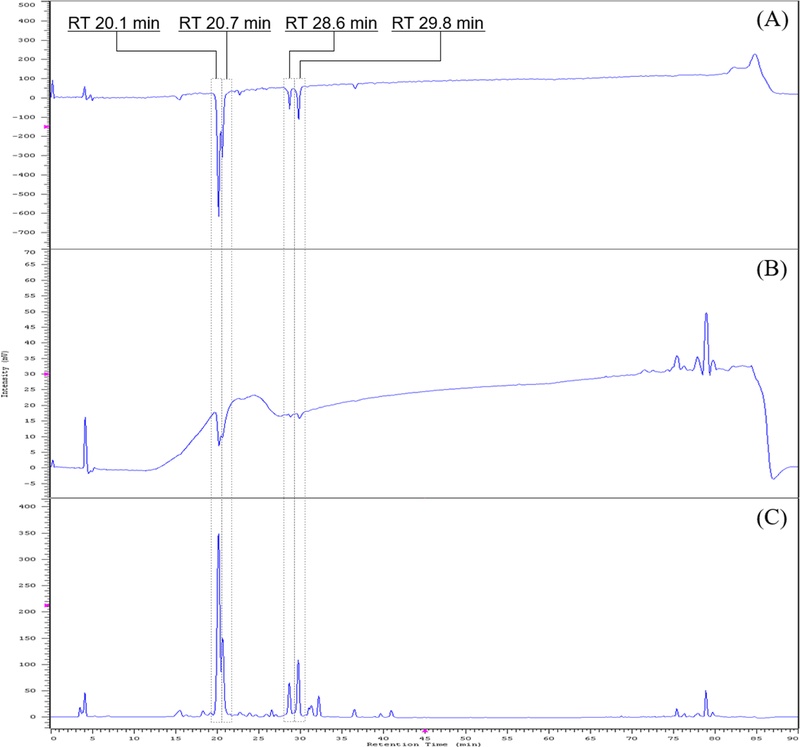
Radical scavenging active compounds in leaf extract of Morus alba.(A) ABTS radical scavenging ability measurement, (B) DPPH radical scavenging ability measurement, (C) LC-UV profile at 254 ㎚.
연구 대상 추출물 중 가장 많은 활성 성분이 확인된 뽕나무 잎 추출물의 경우, Fig. 1 (A)의 ABTS radical 소거능 측정 결과에서 머무름시간 20.1 분, 20.7 분, 28.6 분, 29.8 분 등 4 개의 특징적인 활성 성분이 존재함을 알 수 있었다. Fig. 1 (B)의 DPPH radical 소거능 측정 결과에서도 해당 성분들의 활성이 비교적 높게 나타남을 확인할 수 있었으며, Fig. 1 (C)에 제시한 뽕나무 잎 추출물의 LC-UV profile에서 동일한 머무름시간 영역을 나타내는 주요 성분의 peak들을 확인할 수 있었다.
Fig. 2 (A)에 제시한 비파나무 잎 추출물의 ABTS radical 소거능 측정 결과에서 머무름시간 15.5 분, 20.1 분, 23.5 분 등 3 개의 특징적인 활성 성분이 존재함을 확인하였다. Fig. 2 (B)의 DPPH radical 소거능 측정 결과에서도 해당 성분들의 활성이 비교적 높게 나타났으며, Fig. 2 (C)에 제시한 비파나무 잎 추출물의 LC-UV profile에서도 동일한 머무름시간에서 주요 성분 peak들을 확인할 수 있었다.
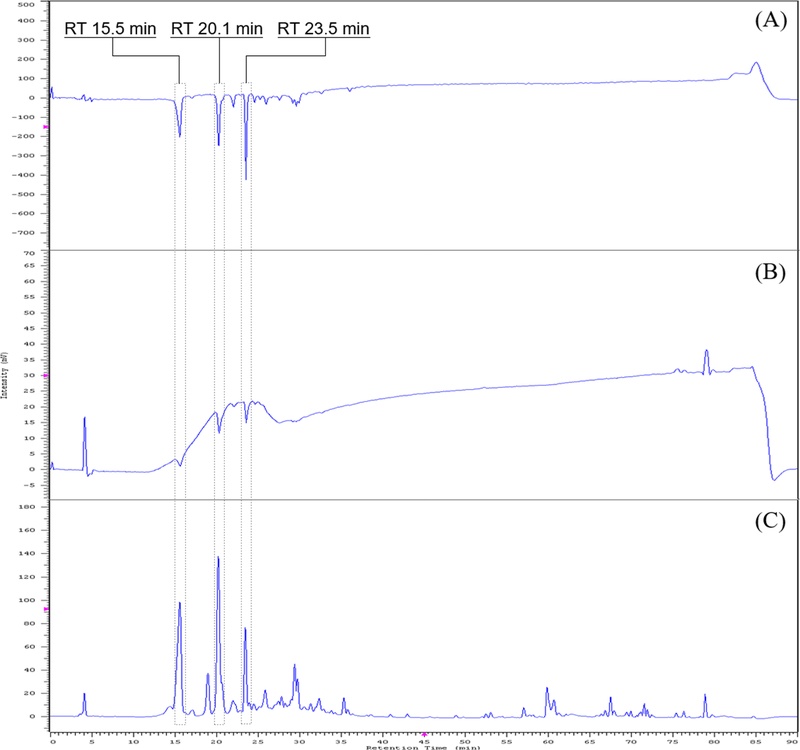
Radical scavenging active compounds in leaf extract of Eriobotrya japonica.(A) ABTS radical scavenging ability measurement, (B) DPPH radical scavenging ability measurement, (C) LC-UV profile at 254 ㎚.
황칠나무 잎 추출물의 경우, Fig. 3 (A)의 ABTS radical 소거능 측정 결과와 Fig. 3 (B)의 DPPH radical 소거능 측정 결과에서 머무름시간 20.1 분의 성분이 높은 활성을 나타냈으며, Fig. 3 (C)에 제시한 추출물의 LC-UV profile에서도 동일한 머무름시간에서 주요 성분 peak를 확인할 수 있었다.
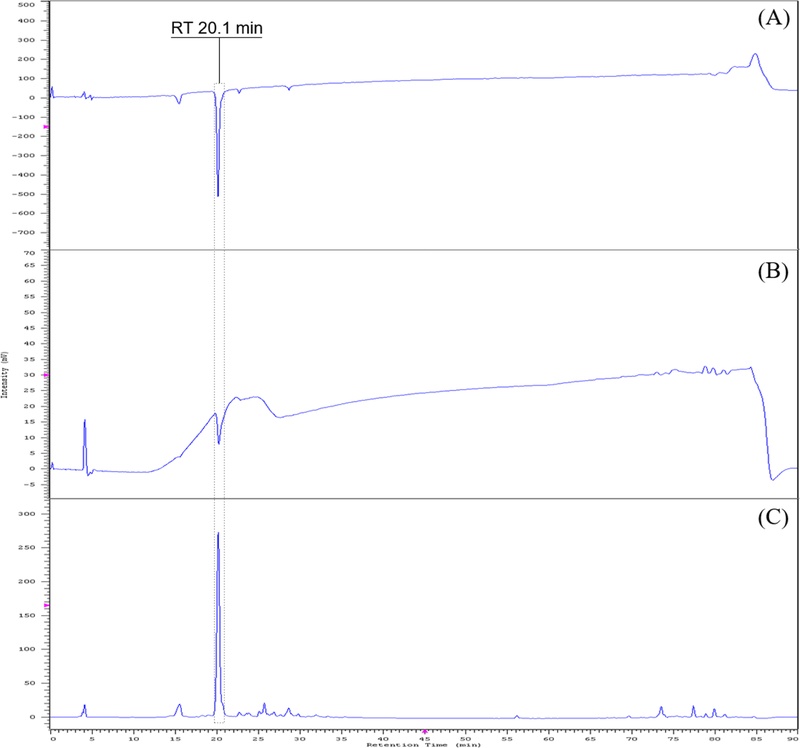
Radical scavenging active compounds in leaf extract of Dendropanax morbiferus.(A) ABTS radical scavenging ability measurement, (B) DPPH radical scavenging ability measurement, (C) LC-UV profile at 254 ㎚.
Fig. 4 (A), (B)에 제시한 산사나무 잎 추출물의 ABTS radical 소거능과 DPPH radical 소거능 측정 결과에서는 Fig. 4 (C)에 제시한 추출물의 LC-UV profile 중 머무름시간 23.5분의 성분이 높은 radical 소거 활성을 나타냈다.
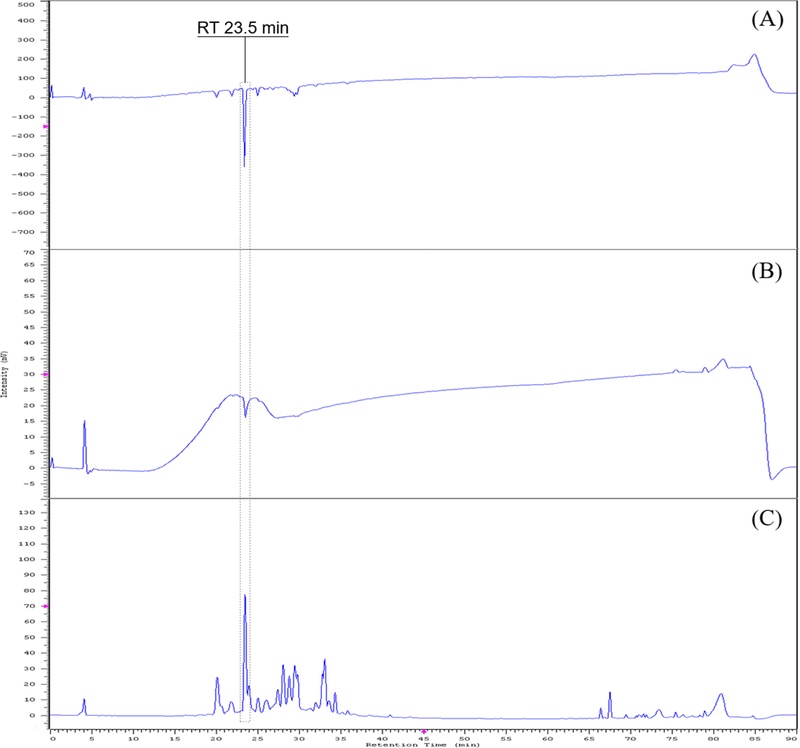
Radical scavenging active compounds in leaf extract of Crataegus pinnatifida.(A) ABTS radical scavenging ability measurement, (B) DPPH radical scavenging ability measurement, (C) LC-UV profile at 254 ㎚.
음나무 잎 추출물의 경우, Fig. 5 (A)의 ABTS radical 소거능 측정 결과와 Fig. 5 (B)의 DPPH radical 소거능 측정 결과에서 Fig. 5 (C)에 제시한 추출물의 LC-UV profile 중 머무름시간 20.1 분의 성분이 높은 활성을 나타내는 것으로 확인되었다.
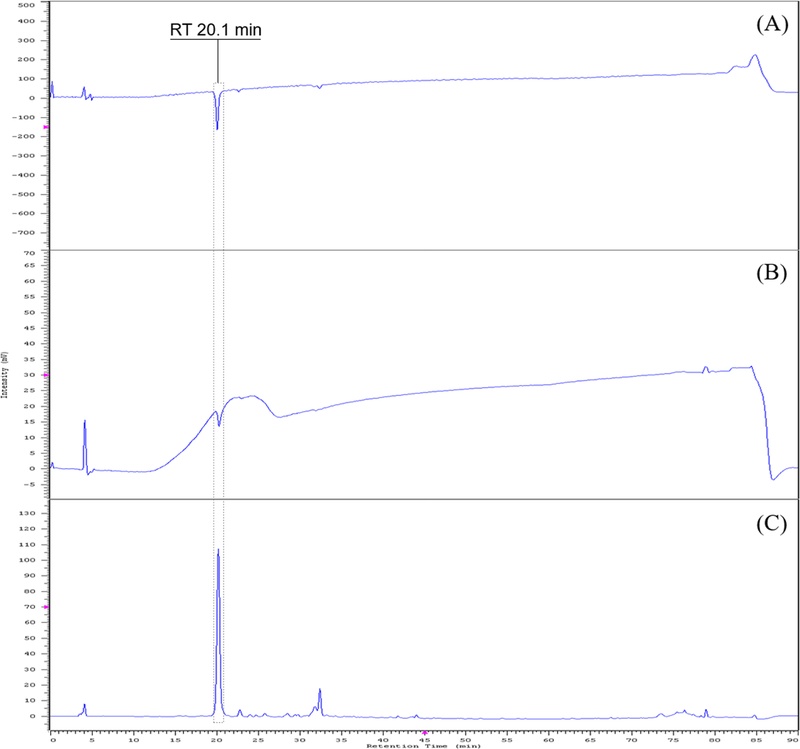
Radical scavenging active compounds in leaf extract of Kalopanax septemlobus.(A) ABTS radical scavenging ability measurement, (B) DPPH radical scavenging ability measurement, (C) LC-UV profile at 254 ㎚.
한편, Fig. 1 – Fig. 5에 제시된 ABTS radical 소거능 측정 결과에서 추출물 및 활성 성분에 따라 최대 - 600 ㎷ 수준으로 활성 peak가 생성된 반면, DPPH radical 소거능 측정 결과에서는 생성된 활성 성분 peak의 검출 강도가 최대 –20 ㎷ 수준으로 ABTS radical 소거능 측정 결과에 비해 현저히 낮은 수준의 활성 peak가 생성된 것을 확인할 수 있었다. 이로 인해 각 추출물의 DPPH radical 소거능 chromatogram의 baseline 변동이 ABTS radical 소거능 chromatogram보다 크게 나타나고 활성 peak 모양이 상대적으로 넓게 형성되었음을 알 수 있었다. 이는 DPPH radical 소거능 측정 결과보다 ABTS radical 소거능 측정 결과에서 활성 peak의 확인이 더 용이함을 나타내는 것으로 본 연구에서 활용한 online LC-radical 소거능 측정 시스템에 적용된 세부조건이 DPPH radical 소거 반응보다 ABTS radical 소거 반응의 검출에 더 적합한 것으로 판단되었다.
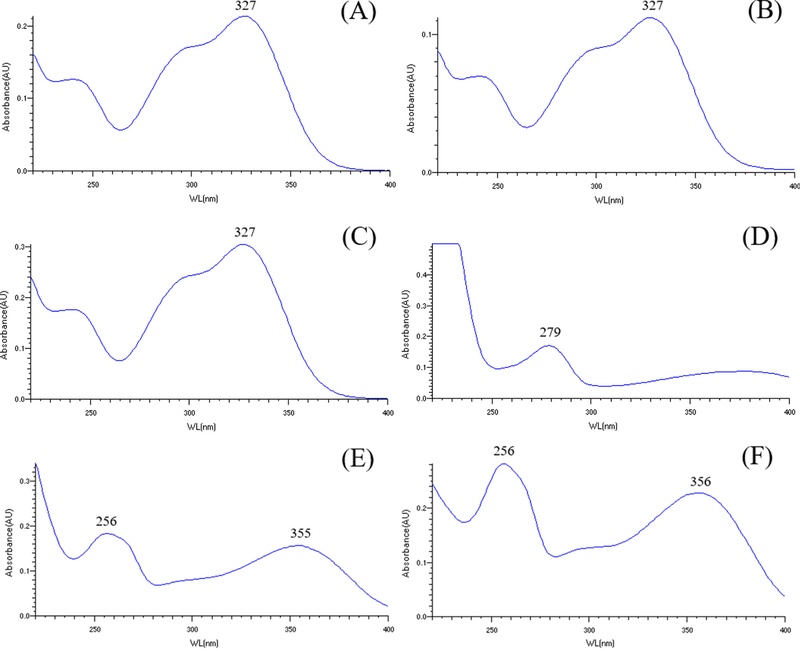
Radical 소거 활성 성분에 대한 정성을 위해 분석 결과에서 확인된 각 추출물의 주요 활성 성분 peak에 대한 UV 흡수 spectrum을 Fig. 6에 제시한 것과 같이 측정하였으며, 서로 다른 종의 추출물이라도 머무름시간이 같은 것으로 나타난 활성 성분 peak는 동일한 형태의 spectrum을 가지는 것으로 확인되었다.
2. 주요 활성 성분 peak의 LC-MS 분석
Online LC-radical 소거능 측정에서 확인된 주요 활성 성분에 대한 정성을 위해서 online LC-radical 소거능 측정과 동일한 LC 분리 조건을 적용한 MS 분석을 추가로 실시하였으며, 6 종의 주요 활성 성분 peak에 대한 MS 분석 결과를 Fig. 7에 제시하였다.

LC-MS analysis results of major active compounds.(A) compound of retention time 15.5 min, (B) compound of retention time 20.1 min, (C) compound of retention time 20.7 min, (D) compound of retention time 23.5 min, (E) compound of retention time 28.6 min, (F) compound of retention time 29.8 min.
일반적으로 ESI 방법이 적용되는 MS 분석에서는 [M+H]+와 함께 [M+Na]+ 형태의 모분자량 패턴이 positive mode에서 주로 나타나며, [M-H]- 형태의 모분자량 패턴이 negative mode에서 특징적으로 나타나게 되어 이를 바탕으로 대상 성분의 분자량을 추정할 수 있게 된다.
Fig. 7 (A)에 제시한 머무름시간 15.5 분의 활성 peak에 대한 MS spectra를 보면 negative mode에서 [M-H]- 형태로 볼 수 있는 353.1 m/z가 특징적으로 나타났고 positive mode에서 [M+H]+와 [M+Na]+ 형태로 볼 수 있는 355.1 m/z와 377.1 m/z가 확인됨에 따라 354의 분자량을 가진 성분임을 알 수 있었다. Fig. 7 (B)와 (C)의 머무름시간 20.1 분과 20.7 분의 활성 peak MS spectra도 머무름시간 15.5 분의 활성 peak와 유사한 형태로 나타남에 따라 354의 분자량을 가진 성분임과 동시에 3 종의 활성 peak들이 화학적으로 동일한 계열의 성분일 것으로 판단할 수 있었다. Fig. 6 (A), (B), (C)에 제시한 것과 같이 각 성분의 UV 흡수 spectrum 역시 유사한 형태로 확인됨에 따라 관련 문헌을 참고하여 3 종의 활성 성분이 caffeoylquinic acid 계열의 성분임을 알 수 있었다 (Bajko et al., 2016).
해당 성분이 확인된 뽕나무와 비파나무 잎 추출물 관련 문헌과 caffeoylquinic acid 계열 성분 관련 문헌을 검토한 후 각 성분의 표준품과 대조 분석을 실시하여 Fig. 8 (A) - (C)에 제시한 것과 같이 각 활성 성분 peak가 머무름시간 순서대로 5-caffeoylquinic acid (neochlorogenic acid), 3-caffeoylquinic acid (chlorogenic acid), 4-caffeoylquinic acid (cryptochlorogenic acid)임을 확인하였다 (Lee and Choi, 2012; Zhang et al., 2015; Chen et al., 2018; Kim et al., 2020). Caffeoylquinic acid 성분들은 다양한 연구에서 항산화 활성과 함께 항염증, 항균 활성, 혈압 조정, 신경퇴행성 질환 개선 효과 등을 나타내는 것으로 보고되고 있다 (Kim et al., 2015; Kim et al., 2017; Chen et al., 2018; Amato et al., 2019; Gao et al., 2020; Kim et al., 2025).
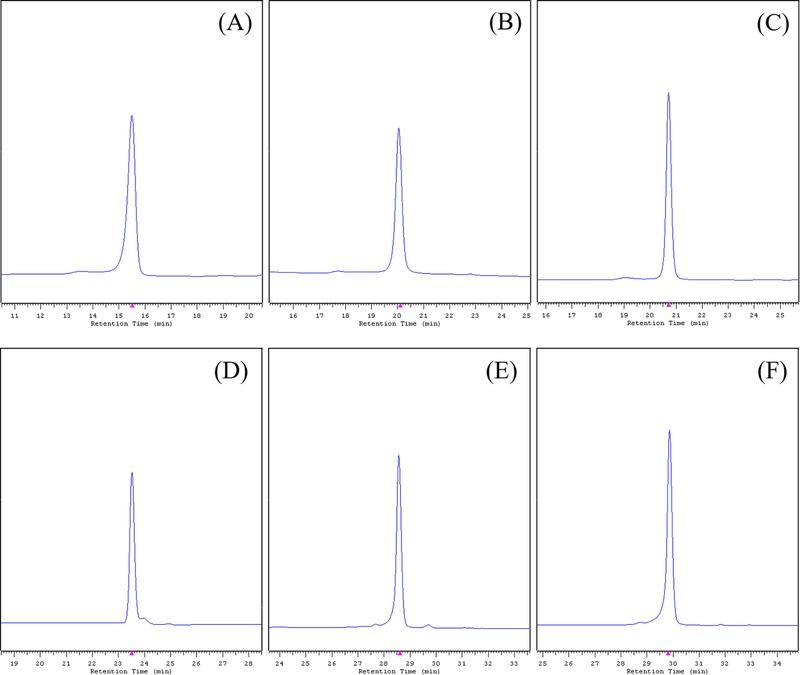
LC chromatograms of standard compounds under LC-UV profile analysis conditions.(A) 5-caffeoylquinic acid, (B) 3-caffeoylquinic acid, (C) 4-caffeoylquinic acid, (D) epicatechin, (E) rutin, (F) isoquercitrin.
Fig. 7 (D)에 제시한 머무름시간 23.5 분의 활성 peak에 대한 MS spectra 중 negative mode에서는 [M-H]- 형태의 289.1 m/z가 나타났고 positive mode에서는 [M+H]+와 [M+Na]+ 형태로 볼 수 있는 291.1 m/z와 313.1 m/z가 확인됨에 따라 분자량이 290인 성분임을 알 수 있었다. 이와 함께 Fig. 6 (D)와 같은 UV 흡수 spectrum을 가지는 화합물에 대한 문헌을 검토하여 녹차와 같은 식물에 존재하는 catechin 또는 epicatechin임을 추정하였으며, 표준품과 대조 분석을 실시하여 해당 활성 성분 peak가 Fig. 8 (D)에 제시한 것과 같이 epicatechin임을 확인하였다 (Choung and Lee, 2008; Ananingsih et al., 2013). Epicatechin은 기본적인 항산화 활성 외에도 전염성 질환이나 알츠하이머와 같은 신경퇴행성 질환에 대한 긍정적인 효과를 나타내는 것으로 보고되고 있다 (Kwon et al., 2011; Choi et al., 2012; Reygaert, 2018; Hatami et al., 2023).
Fig. 7 (E)에 제시한 머무름시간 28.6 분의 활성 peak에 대한 MS spectra에서는 negative mode에서 [M-H]- 형태의 609.1 m/z가 나타났으며, positive mode에서 [M+H]+와 [M+Na]+ 형태로 볼 수 있는 611.1 m/z와 633.1 m/z가 확인됨에 따라 분자량이 610인 성분임을 알 수 있었다. Fig. 6 (E)에 제시한 UV 흡수 spectrum을 나타내는 화합물에 대한 문헌을 검토하여 분자 내에 quercetin 구조를 포함하는 rutin과 같은 flavonoid 화합물에서 나타날 수 형태임을 확인하였으며, 표준품 대조 분석을 실시하여 Fig. 8 (E)에 제시한 것과 같이 rutin임을 확인하였다 (Zhu et al., 2015). Rutin은 다양한 식물에 존재하며, 항산화 활성을 포함하여 항염증, 항고혈압 및 뇌졸중 예방 효과, 콜레스테롤 저하 등의 효과를 가지는 것으로 알려져 있다 (Gim et al., 2020).
Fig. 7 (F)에 제시한 머무름시간 29.8 분의 활성 peak에 대한 MS spectra 중 negative mode에서 나타난 [M-H]- 형태의 463.1 m/z와 positive mode에서 나타난 [M+H]+와 [M+Na]+ 형태의 465.1 m/z와 487.1 m/z에서 해당 peak의 성분이 464의 분자량을 가진 것을 알 수 있었다. 이와 함께 Fig. 6 (F)와 같은 UV 흡수 spectrum을 가지는 화합물에 대한 문헌을 검토하여 quercetin 구조에 당이 결합된 구조의 flavonoid에서 나타나는 형태인 hyperoside나 isoquercitrin에서 나타나는 형태임을 확인하였고 표준품 대조 분석을 통해서 Fig. 8 (F)에 제시한 것과 같이 isoquercitrin임을 확인하였다 (Zhou et al., 2011). Isoquercitrin은 항산화 활성, 피부 미백 및 항주름 효과, 항균 활성 등을 나타내는 flavonoid 성분으로 알려져 있다 (Kim, 2021).
3. Radical 소거 활성 성분 함량 분석
LC-MS 분석과 표준품 대조 분석을 통하여 radical 소거 활성을 가지는 주요 성분이 5-caffeoylquinic acid, 3-caffeoylquinic acid, 4-caffeoylquinic acid, epicatechin, rutin, isoquercitrin임을 확인하였으며, 6 종 성분에 대한 함량 분석을 실시하였다.
앞서 실시한 online LC-radical 소거능 측정에서 모든 활성 성분의 머무름시간이 전체 분석시간 90 분 중 1/3에 해당하는 30 분 이전에 형성된 것과 적용된 이동상 조건에서 발견된 일부 활성 성분 peak 간의 분리도 부족 현상을 개선하기 위해서 이동상 조건을 Table 2와 같이 변경하였다.
또한 Fig. 6에 제시한 각 활성 성분의 UV 흡수 spectrum을 검토하여 상대적으로 흡광 파장 범위에 제한이 있는 것으로 판단된 epicatechin을 기준으로 6 종 성분을 동시에 분석하기 위한 검출기 파장을 280 nm로 설정하였다.
변경된 이동상 조건과 검출기 파장을 적용하여 실시된 LC 분석 결과는 Fig. 9에 제시하였으며, 각 추출물과 표준품 분석 chromatogram에서 개선된 분석 결과를 확인할 수 있었다. 10 µg/mL - 500 µg/mL 범위의 농도별 표준품 분석 결과에서 산출된 검량선 정보를 Table 3에 제시하였다.
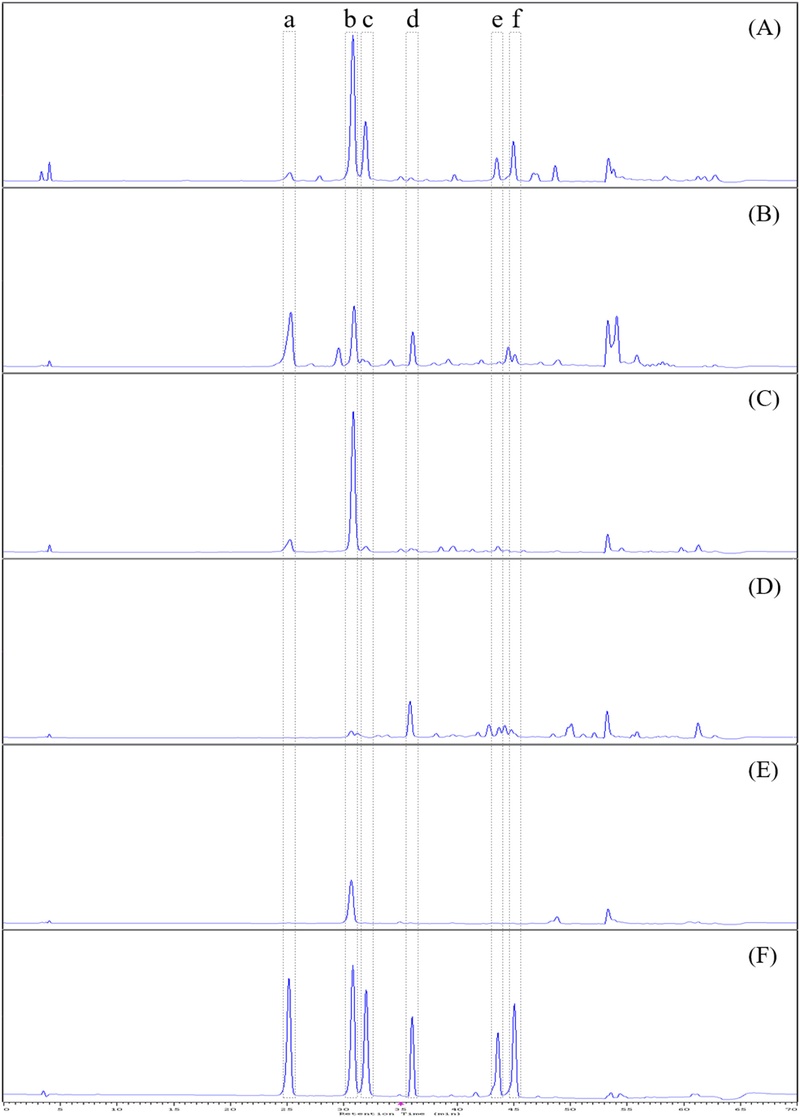
LC chromatograms of major active compounds in leaf extracts of 5 plants.(A) Morus alba, (B) Eriobotrya japonica, (C) Dendropanax morbiferus, (D) Crataegus pinnatifida, (E) Kalopanax septemlobus, (F) mixture of standards. a; 5-caffeoylquinic acid, b; 3-caffeoylquinic acid, c; 4-caffeoylquinic acid, d; epicatechin, e; rutin, f; isoquercitrin.
Table 4에 제시한 각 추출물의 활성 성분 함량 측정 결과, 뽕나무 잎 추출물에는 3-caffeoylquinic acid가 502.3 ㎍/㎖로 가장 함량이 높은 성분으로 확인되었으며, 4-caffeoylquinic acid와 isoquercitrin의 함량이 각각 223.5 ㎍/㎖ 와 188.2 ㎍/㎖로 나타났다. 비파나무 잎 추출물은 5-caffeoylquinic acid가 285.3 ㎍/㎖로 가장 함량이 높은 성분으로 나타났으며, 3-caffeoylquinic acid와 epicatechin이 210.1 ㎍/㎖ 와 191.0 ㎍/㎖의 함량을 나타냈다. 황칠나무와 음나무 잎 추출물은 3-caffeoylquinic acid가 각각 461.7 ㎍/㎖와 159.4 ㎍/㎖의 함량을 나타냄으로써 특징적으로 항산화 활성을 나타내는 성분으로 확인되었으며, 산사나무 잎 추출물에서는 epicatechin이 213.5 ㎍/㎖로 항산화 활성을 나타내는 주요 성분으로 나타났다.
한편, 본 연구에서와 같이 online LC-radical 소거능 측정 시스템을 활용하여 식물 추출물 중에 존재하는 항산화 활성 성분을 확인하려는 연구가 지속적으로 수행되고 있다. 커피나무 (Coffea arabica) 잎에는 5-caffeoylquinic acid, 3-caffeoylquinic acid, cinnamtannin B-1, mangiferin, 3,4-dicaffeoylquinic acid, 3,5-dicaffeoylquinic acid, 4,5-dicaffeoylquinic acid가 주요 항산화 활성 성분임이 확인되었으며 (Lee et al., 2022), 황해쑥 (Artemisia argyi)에서는 3,5-dicaffeoylquinic acid, 3,4-dicaffeoylquinic acid, 4,5-dicaffeoylquinic acid, 1,4-dicaffeoylquinic acid, 3-caffeoylquinic acid가 확인되었다 (Yang et al., 2023). 또한 환삼덩굴 (Humulus japonicus)에는 luteolin-7-glucoside 성분이 주요 활성 성분으로 나타났으며 (Lee, 2023), 두릅나무 (Aralia elata) 잎은 5-caffeoylquinic acid, 3,5-dicaffeoylquinic acid, 3,4-dicaffeoylquinic acid를 항산화 활성 성분으로 포함하고 있음이 밝혀졌다 (Lee et al., 2024a).
꾸지뽕나무 (Cudrania tricuspidata) 잎에서는 6,8-diprenylorobol이라는 flavonoid 성분이 확인되었으며 (Lee et al., 2024b), 폴리네시아 (Polynesia) 지역의 연구에서는 Calophyllum inophyllum, Gardenia taitensis, Cordia subcordata, Ficus prolixa 등의 지역 식물 소재에서 radical 소거 활성 성분으로서 quercetin-O-rhamnoside, rosmarinic acid, 3-caffeoylquinic acid, procyanidins, epicatechin, 5-O-caffeoylshikimic acid 등이 확인되었다 (Chambon et al., 2023). 본 연구의 결과를 포함하여 예외적인 경우를 제외하고 식물 중에 존재하는 항산화 활성 성분은 caffeoylquinic acid 계열의 성분과 luteolin이나 quercetin과 같은 flavonoid 구조의 유도체가 포함된 경우가 많음을 알 수 있다. 따라서 본 연구에서 사용된 측정 및 분석 방법이 다른 식물 소재의 항산화 활성 관련 연구에도 응용이 가능할 것으로 판단되며, 특히 연구개발 초기에 스크리닝 분석을 위한 유용한 방법이 될 수 있을 것이다.
본 연구에서는 다양한 질환의 예방과 개선에 효과를 나타내는 것으로 보고되고 있는 항산화 활성 소재 및 성분에 대한 탐색을 위해서 전남 지역에 자생하는 뽕나무, 비파나무, 황칠나무, 산사나무, 음나무 등 5 종의 활엽수 잎 추출물을 대상으로 online LC-radical 소거능 측정 시스템을 활용하여 항산화 활성 성분에 대한 탐색을 실시하였다.
각 추출물에서 확인된 ABTS와 DPPH radical 소거 활성 성분 peak에 대한 UV 흡수 spectrum과 LC-MS 분석을 실시하여 radical 소거 활성을 나타내는 주요 성분이 5-caffeoylquinic acid, 3-caffeoylquinic acid, 4-caffeoylquinic acid, epicatechin, rutin, isoquercitrin임을 확인하였다. 각 추출물의 주요 활성 성분에 대한 정량분석을 실시한 결과, 뽕나무 잎 추출물의 주요 활성 성분으로 3-caffeoylquinic acid, 4-caffeoylquinic acid, isoquercitrin이 확인되었으며, 비파나무 잎 추출물은 5-caffeoylquinic acid, 3-caffeoylquinic acid, epicatechin이 주요 활성 성분으로 나타냈다. 황칠나무와 음나무 잎 추출물에서는 3-caffeoylquinic acid가 주요 활성 성분으로 확인되었으며, 산사나무 잎 추출물에서는 epicatechin이 활성을 나타내는 주요 성분으로 확인되었다.
다만, 이상의 결과는 채취 시기나 지역, 건조 등 전처리 및 추출 조건, 세부 품종 등의 차이에 대한 부분은 검토되지 않았으므로 개별 소재에 대한 추가적인 연구가 필요할 것으로 판단된다.
Acknowledgments
이 논문은 2024학년도 조선대학교 학술연구비의 지원에 의해 이루어진 결과로 이에 감사드립니다.
References
-
Amato A, Terzo S and Mulè F. (2019). Natural compounds as beneficial antioxidant agents in neurodegenerative disorders: A focus on Alzheimer’s disease. Antioxidants. 8:608 https://www.mdpi.com/2076-3921/8/12/608, (cited by 2025 May 10).
[https://doi.org/10.3390/antiox8120608]

-
Amin ARMR, Kucuk O, Khuri FR and Shin DM. (2009). Perspectives for cancer prevention with natural compounds. Journal of Clinical Oncology. 27:2712-2725.
[https://doi.org/10.1200/JCO.2008.20.6235]

-
Ananingsih VK, Sharma A and Zhou W. (2013). Green tea catechins during food processing and storage: A review on stability and detection. Food Research International. 50:469-479.
[https://doi.org/10.1016/j.foodres.2011.03.004]

-
Awika JM, Rooney LW, Wu X, Prior RL and Cisneros-Zevallos L. (2003). Screening methods to measure antioxidant activity of sorghum(Sorghum bicolor) and sorghum products. Journal of Agricultural and Food Chemistry. 51:6657-6662.
[https://doi.org/10.1021/jf034790i]

-
Bajko E, Kalinowska M, Borowski P, Siergiejczyk L and Lewandowski W. (2016). 5-O-Caffeoylquinic acid: A spectroscopic study and biological screening for antimicrobial activity. LWT-Food Science and Technology. 65:471-479.
[https://doi.org/10.1016/j.lwt.2015.08.024]

-
Braham F, Carvalho DO, Almeida CMR, Zaidi F, Magalhães JMCS, Guido LF and Gonçalves MP. (2020). Online HPLC-DPPH screening method for evaluation of radical scavenging phenols extracted from Moringa oleifera leaves. South African Journal of Botany. 129:146-154.
[https://doi.org/10.1016/j.sajb.2019.04.001]

- Cha BC. (2015). Changes in the constituents and antioxidant activity in accordance with the processing conditions of Citrus unshiu Markovich. Korean Journal of Pharmacognosy. 46:23-30.
-
Chambon M, Ho R, Baghdikian B, Herbette G, Bun-Llopet SS, Garayev E and Raharivelomanana P. (2023). Identification of antioxidant metabolites from five plants(Calophyllum inophyllum, Gardenia taitensis, Curcuma longa, Cordia subcordata, Ficus prolixa) of the Polynesian pharmacopoeia and cosmetopoeia for skin care. Antioxidants. 12:1870. https://www.mdpi.com/2076-3921/12/10/1870, (cited by 2025 May 30).
[https://doi.org/10.3390/antiox12101870]

-
Chen X, Ma Z and Kitts DD. (2018). Effects of processing method and age of leaves on phytochemical profiles and bioactivity of coffee leaves. Food Chemistry. 249:143-153.
[https://doi.org/10.1016/j.foodchem.2017.12.073]

-
Choi DY, Lee YJ, Hong JT and Lee HJ. (2012). Antioxidant properties of natural polyphenols and their therapeutic potentials for Alzheimer’s disease. Brain Research Bulletin. 87:144-153.
[https://doi.org/10.1016/j.brainresbull.2011.11.014]

- Choung MG and Lee MS. (2008). Optimal HPLC condition for simultaneous determination of catechins and caffeine in green tea extracts. Korean Journal of Crop Science. 53:224-232.
-
Condello M and Meschini S. (2021). Role of natural antioxidant products in colorectal cancer disease: A focus on a natural compound derived from Prunus spinosa, Trigno ecotype. Cells.10:3326 https://www.mdpi.com/2073-4409/10/12/3326, (cited by 2025 May 10).
[https://doi.org/10.3390/cells10123326]

- Devasagayam TP, Tilak JC, Boloor KK, Sane KS, Ghaskadbi SS and Lele RD. (2004). Free radicals and antioxidants in human health: Current status and future prospects. Journal of Association of Physicians of India. 52:794-804.
-
Dhalla NS, Temsah RM and Netticadan T. (2000). Role of oxidative stress in cardiovascular diseases. Journal of Hypertension. 18:655-673.
[https://doi.org/10.1097/00004872-200018060-00002]

-
Farhan M, Rizvi A, Aatif M and Ahmad A. (2023). Current understanding of flavonoids in cancer therapy and prevention. Metabolites. 13:481 https://www.mdpi.com/2218-1989/13/4/481, (cited by 2025 May 10).
[https://doi.org/10.3390/metabo13040481]

-
Gao X, Zhang S, Wang L, Yu L, Zhao X, Ni H, Wang Y, Wang J, Shan C and Fu Y. (2020). Anti-inflammatory effects of neochlorogenic acid extract from mulberry leaf(Morus alba L.) against LPS-stimulated inflammatory response through mediating the AMPK/Nrf2 signaling pathway in A549 cells. Molecules. 25:1385. (cited by 2025 May 10).
[https://doi.org/10.3390/molecules25061385]

- Gim SW, Chae KS, Lee SJ, Kim KD, Moon JH and Kwon JW. (2020). Main constituents and bioactivities of different parts of aronia(Aronia melanocarpa). Korean Journal of Food Science and Technology. 52:226-236.
-
Griffiths K, Aggarwal B, Singh R, Buttar HS, Wilson D and De Meester F. (2016). Food antioxidants and their anti-inflammatory properties: A potential role in cardiovascular diseases and cancer prevention. Diseases. 4:28 https://www.mdpi.com/2079-9721/4/3/28, (cited by 2025 May 10).
[https://doi.org/10.3390/diseases4030028]

-
Hatami M, Mortazavi M, Baseri Z, Khani B, Rahimi M and Babaei S. (2023). Antioxidant compounds in the treatment of Alzheimer’s disease: Natural, hybrid, and synthetic products. Evidence-Based Complementary and Alternative Medicine. https://onlinelibrary.wiley.com/doi/10.1155/2023/8056462, (cited by 2025 May 10).
[https://doi.org/10.1155/2023/8056462]

-
Hong JS, Kang BG, Jang YS, Kim SH, Wang Z, Park YH, Park JH and Lim SS. (2014). Studies on standardization of licorice based on its active components with on-line HPLC bioassay system. Korean Journal of Plant Resources. 27:401-414.
[https://doi.org/10.7732/kjpr.2014.27.5.401]

- Im DY and Lee KI. (2020). LC-MS/MS screening method for radical scavenging active compounds in extracts of Ulmus pumila cortex. Journal of Life Science. 30:956-964.
-
Im DY, Pyo BS, Kim SM and Lee KI. (2017). Measurement of the anti-oxidative properties of extract from medicinal plants using an on-line HPLC-DPPH assay. Journal of Life Science. 27:44-49.
[https://doi.org/10.5352/JLS.2017.27.1.44]

-
Inoue K, Baba E, Hino T and Oka H. (2012). A strategy for high-speed countercurrent chromatography purification of specific antioxidants from natural products based on on-line HPLC method with radical scavenging assay. Food Chemistry. 134:2276-2282.
[https://doi.org/10.1016/j.foodchem.2012.02.219]

-
Juiz PJL, Ferreira LTB, Pires EA and Villarreal CF. (2024). Patent mining on the use of antioxidant phytochemicals in the technological development for the prevention and treatment of periodontitis. Antioxidants. 13:566. https://www.mdpi.com/2076-3921/13/5/566, (cited by 2025 May 10).
[https://doi.org/10.3390/antiox13050566]

-
Kim AY, Pyo BS, Kim SM, Park MJ, Lee SS and Lee KI. (2019). Radical scavenging effects of 10 plant essential oils and active compound screening analysis. Korean Journal of Medicinal Crop Science. 27:427-435.
[https://doi.org/10.7783/KJMCS.2019.27.6.427]

-
Kim HG, Kang SM, Park DJ, Yong SH, Yang WH, Park JH, Yu CY, Solomon T and Choi MS. (2018). Effects of blending oil and antioxidants to prevent rancidity of sancho oil. Korean Journal of Medicinal Crop Science. 26:455-463.
[https://doi.org/10.7783/KJMCS.2018.26.6.455]

- Kim HS. (2021). Physiological activities of ethanol extract of Allium tuberosum root. Korean Journal of Food Science and Technology. 53:160-164.
- Kim JH, Kim DS, Lee CY and Lee HS. (2025). Meta-analysis of chlorogenic acid and its role in blood pressure regulation. Journal of Life Science. 35:216-227.
-
Kim MN, Choi SY, Lee PJ and Hur JY. (2015). Neochlorogenic acid inhibits lipopolysaccharide-induced activation and proinflammatory responses in BV2 microglial cells. Neurochemical Research. 40:1792-1798.
[https://doi.org/10.1007/s11064-015-1659-1]

-
Kim SH, Park SY, Park YL, Myung DS, Rew JS and Joo YE. (2017). Chlorogenic acid suppresses lipopolysaccharide-induced nitric oxide and interleukin-1β expression by inhibiting JAK2/STAT3 activation in RAW264.7 cells. Molecular Medicine Reports. 16:9224-9232.
[https://doi.org/10.3892/mmr.2017.7686]

-
Kim SM, Kim AY and Lee KI. (2020). Nitric oxide production inhibitory effects of three caffeoylquinic acids isolated from hot water extract of Eriobotrya japonica L. leaves. Korean Journal of Medicinal Crop Science. 28:245-253.
[https://doi.org/10.7783/KJMCS.2020.28.4.245]

-
Kwon DJ, Kim JK and Bae YS. (2011). DPPH radical scavenging activity of phenolic compounds isolated from the stem wood of Acer tegmentosum. Journal of the Korean Wood Science and Technology. 39:104-112.
[https://doi.org/10.5658/WOOD.2011.39.1.104]

-
Lee KI. (2023). Radical scavenging active compound analysis in extract of Humulus japonicus using an online LC-DPPH assay. Korean Journal of Pharmacognosy. 54:184-190.
[https://doi.org/10.22889/KJP.2023.54.4.184]

-
Lee KI, Back JH, Pyo BS and Choi CH. (2023). Radical scavenging active compound analysis in extract of coffee silver skin. Korean Journal of Medicinal Crop Science. 31:211-221.
[https://doi.org/10.7783/KJMCS.2023.31.4.211]

-
Lee KI, Pyo BS, Choi CH and Cha SW. (2022). Radical scavenging active compound screening analysis in extract of Coffea arabica L. leaves. Korean Journal of Medicinal Crop Science. 30:264-277.
[https://doi.org/10.7783/KJMCS.2022.30.4.264]

-
Lee KI, Sun KH and Choi CH. (2024a). DPPH radical scavenging active compound analysis in the extract of Aralia elata leaves. Korean Journal of Pharmacognosy. 55:142-150.
[https://doi.org/10.22889/KJP.2024.55.3.142]

-
Lee KI, Yoon YS and Choi CH. (2024b). 1,1-Diphenyl-2-picrylhydrazyl radical scavenging active compound analysis in extracts of Cudrania tricuspidata leaves. Korean Journal of Medicinal Crop Science. 32:144-151.
[https://doi.org/10.7783/KJMCS.2024.32.3.144]

-
Lee SM, You YH, Kim KM, Park JJ, Jeong CS, Jhon DY and Jun WJ. (2012). Antioxidant activities of native Gwangyang Rubus coreanus Muq. Journal of the Korean Society of Food Science and Nutrition. 41:327-332.
[https://doi.org/10.3746/jkfn.2012.41.3.327]

-
Lee WJ and Choi SW. (2012). Quantitative changes of polyphenolic compounds in mulberry(Morus alba L.) leaves in relation to varieties, harvest period, and heat processing. Preventive Nutrition and Food Science. 17:280-285.
[https://doi.org/10.3746/pnf.2012.17.4.280]

-
Li H and Jeong JM. (2015). Antioxidant activities of various berries ethanolic extract. Korean Journal of Medicinal Crop Science. 23:49-56.
[https://doi.org/10.7783/KJMCS.2015.23.1.49]

-
Maccioni RB, Calfío C, González A and Lüttges V. (2022). Novel nutraceutical compounds in Alzheimer prevention. Biomolecules. 12:249 https://www.mdpi.com/2218-273X/12/2/249, (cited by 2025 May 10).
[https://doi.org/10.3390/biom12020249]

-
Park SA, Kim HJ, Bang MY, Um BH and Cha JW. (2024). A study on the photoisomerization of phenylpropanoids and the differences in their radical scavenging activity using in-situ NMR spectroscopy and on-line radical scavenging activity analysis. Applied Biological Chemistry. https://applbiolchem.springeropen.com/articles/10.1186/s13765-024-00925-3, (cited by 2025 May 10).
[https://doi.org/10.1186/s13765-024-00925-3]

-
Reygaert WC. (2018). Green tea catechins: Their use in treating and preventing infectious diseases. BioMed Research International. 2018:9105261. https://onlinelibrary.wiley.com/doi/10.1155/2018/9105261, (cited by 2025 May 25).
[https://doi.org/10.1155/2018/9105261]

-
Schieber M and Chandel NS. (2014). ROS function in redox signaling and oxidative stress. Current Biology. 24:453-462.
[https://doi.org/10.1016/j.cub.2014.03.034]

-
Song JH and Lee SR. (2015). Anti-oxidant and inhibitory activity on NO production of extract and its fractions from Rosa davurica Pall. leaves. Korean Journal of Medicinal Crop Science. 23:20-26.
[https://doi.org/10.7783/KJMCS.2015.23.1.20]

-
Valko M, Leibfritz D, Moncol J, Cronin MT, Mazur M and Telser J. (2007). Free radicals and antioxidants in normal physiological functions and human disease. International Journal of Biochemistry and Cell Biology. 39:44-84.
[https://doi.org/10.1016/j.biocel.2006.07.001]

-
Wiseman H and Halliwell B. (1996). Damage to DNA by reactive oxygen and nitrogen species: Role in inflammatory disease and progression to cancer. Biochemical Journal. 313:17-29.
[https://doi.org/10.1042/bj3130017]

-
Yang W, Huang Q, Wu M, Mei Q, Zou Y, Qian Z and Tang D. (2023). Rapid screening and evaluation of natural antioxidants from leaf, stem, and root of Artemisia argyi by online liquid microextraction combined with HPLC‐based antioxidant assay system coupled with calibration quantitative analysis. Journal of Separation Science. 47:20230616. https://analyticalsciencejournals.onlinelibrary.wiley.com/doi/10.1002/jssc.202300616, . (cited by 2025 May 30).
[https://doi.org/10.1002/jssc.202300616]

-
Yoo NH, Kim HK, Lee CO, Park JH and Kim MJ. (2019). Comparison of anti-oxidant and anti-inflammatory activities of methanolic extracts obtained from different parts of Cononeaster wilsonii Nakai. Korean Journal of Medicinal Crop Science. 27:194-201.
[https://doi.org/10.7783/KJMCS.2019.27.3.194]

-
Zhang H, Xi W, Yang Y, Zhou X, Liu X, Yin S, Zhang J and Zhou Z. (2015). An on-line HPLC-FRSD system for rapid evaluation of the total antioxidant capacity of Citrus fruits. Food Chemistry. 172:622-629.
[https://doi.org/10.1016/j.foodchem.2014.09.121]

-
Zhang Y, Dawson VL and Dawson TM. (2000). Oxidative stress and genetics in the pathogenesis of Parkinson’s disease. Neurobiology of Disease. 7:240-250.
[https://doi.org/10.1006/nbdi.2000.0319]

-
Zhou C, Liu Y, Su D, Gao G, Zhou X, Sun L, Ba X, Chen X and Bi K. (2011). A sensitive LC-MS-MS method for simultaneous quantification of two structural isomers, hyperoside and isoquercitrin: Application to pharmacokinetic studies. Chromatographia. 73:353-359.
[https://doi.org/10.1007/s10337-010-1879-0]

-
Zhu S, Yan H, Niu K and Zhang S. (2015). Simultaneous determination of seven components from hawthorn leaves flavonoids in rat plasma by LC-MS/MS. Journal of Chromatographic Science. 53:909-914.
[https://doi.org/10.1093/chromsci/bmu143]