
인간 노로바이러스의 대체 모델, 고양이 칼리시바이러스를 이용한 단삼 수용성 및 에탄올 추출물의 항바이러스 활성 비교
This is an open access article distributed under the terms of the Creative Commons Attribution Non-Commercial License (http://creativecommons.org/licenses/by-nc/3.0/) which permits unrestricted non-commercial use, distribution, and reproduction in any medium, provided the original work is properly cited.
Abstract
Feline calicivirus (FCV), a surrogate for human norovirus, was used to evaluate the antiviral activity of aqueous (SM-DW) and ethanolic (SM-E) extracts of Salvia miltiorrhiza. In the absence of effective antivirals against non-enveloped RNA viruses, such as noroviruses, screening traditional medicinal plants, such as S. miltiorrhiza, provides valuable insights for developing natural antiviral agents.
The cytotoxicity and maximal non-cytotoxic concentrations of both extracts were assessed in Crandell-Rees feline kidney cells. SM-E showed markedly stronger antiviral activity, inhibiting FCV replication at 3.13 ㎍/㎖, whereas SM-DW required 100 ㎍/㎖ to achieve a similar effect, indicating more than a 30-fold increase in potency. Additionally, SM-E exhibited a higher plaque reduction rate and greater suppression of viral titers, particularly in post-infection treatment, suggesting potential interference with intracellular viral replication. High-performance liquid chromatography revealed that SM-E contained substantially higher levels of lipophilic diterpenoids, especially tanshinone IIA, than SM-DW. This enriched composition appeared to be closely linked to the enhanced antiviral efficacy of SM-E, indicating that tanshinone IIA may be the key active constituent responsible for viral inhibition.
These results indicate that the choice of the extraction solvent critically affects the antiviral potential of S. miltiorrhiza and highlight SM-E as a promising natural antiviral candidate against noroviruses, acting through tanshinone-enriched mechanisms.
Keywords:
Salvia miltiorrhiza, Feline Calicivirus, Antiviral Activity, Norovirus, Pheolic Compound, Tanshinone, Time-of-Addition Model서 언
2019년 코로나바이러스감염증-19 (COVID-19)의 전 세계적 확산 및 지속적인 변이 발생, 항바이러스제 내성의 출현은 기존 치료 전략의 한계를 드러내며, 새로운 항바이러스제 개발의 필요성을 한층 부각시켰다 (WHO, 2020). 바이러스는 의료 환경뿐만 아니라 일상생활에서도 다양한 경로를 통해 건강에 위협을 가하며, 특히 식품은 주요 감염 매개체 중 하나로 자주 지목되고 있다. 이러한 상황에서, 독성이 낮고 다양한 작용 기전을 지닌 천연 유래 물질은 안전하고 효과적인 항바이러스 소재로 주목받고 있으며, 전 세계적으로 천연물 및 합성 화합물 기반 신약 개발 연구가 활발히 진행되고 있다 (Koehn and Carter, 2005; Rajasekaran et al., 2013).
노로바이러스 (norovirus, NoV)는 Caliciviridae과에 속하는 외피 비보유 단일 가닥 RNA 바이러스로서 전 세계적으로 급성위장염의 주요 원인으로 지목되고 있다. 강한 환경 저항성과 높은 전염력을 바탕으로 식중독의 주요 병원체로 분류되며 (Ahmed et al., 2014; Robilotti et al., 2015), 고유한 유전적 다양성과 감염 특성으로 인해 백신 및 항바이러스제 개발이 어렵고, 현재까지 임상적으로 승인된 치료제가 없다 (Lindesmith et al., 2010; Winder et al., 2022). 이에 따라 안전하고 친환경적인 항바이러스 소재의 확보가 중요한 과제로 대두되고 있으며, 특히 식품 및 생활 환경에 적용 가능한 무독성 천연물 기반 항바이러스 소재에 대한 관심이 증가하고 있다 (Stals et al., 2011).
그러나 NoV는 인간의 장 세포에서만 증식이 가능하여 일반적인 동물모델이나 세포주 기반 실험에서는 배양이 어렵고 복제 효율 또한 낮아 약물 효능 평가에 큰 제약이 있어 (Duizer et al., 2004), 약물 후보 물질의 기전 평가나 증식 억제 효과를 확인하는 데 기술적 한계가 있다. 이러한 한계를 극복하기 위해 NoV와 유전적으로 유사한 feline calicivirus (FCV) 및 murine norovirus (MNV-1)가 대체 모델로 활용되고 있으며, 이들을 이용한 항바이러스 평가 모델이 활발히 사용되고 있다 (Steinmann, 2004; Wobus et al., 2004; Cromeans et al., 2014).
지금까지 다양한 천연물이 MNV 및 FCV에 대해 항바이러스 활성을 나타낸다고 보고되었으며, 특히 polyphenol 및 flavonoid 기반 성분들이 주요 작용 성분으로 제시되었다. 예를 들어, Lee 등 (2014)은 오디 (Morus alba) 주스와 분획물이 MNV-1의 복제와 FCV-F9 바이러스 입자의 내재화를 억제함으로써 식품 매개 장내 바이러스에 대한 항바이러스 효과를 보인다고 보고하였다. 또한 black raspberry (Rubus coreanus) 주스는 바이러스 입자와 숙주 수용체 간의 결합을 차단하거나 바이러스 유입을 억제함으로써 MNV-1 감염을 효과적으로 억제하였다고 보고하였다 (Oh et al., 2012). 녹차의 polyphenol 성분은 anti-FCV-F9 활성이 높고 세포 독성은 낮은 이상적인 특성을 보였으며 (Oh et al., 2013), 오레가노 (Origanum vulgare)의 정유 (Gilling et al., 2014), 감 (Diospyros kaki) 추출물 (Kamimoto et al., 2014) 등 다양한 천연물이 항바이러스 활성을 나타내는 것으로 보고되었다.
그러나 기존의 연구들은 바이러스 억제 메커니즘에 대한 세포 및 유전자 수준의 기전 분석은 제한적이며, terpene 계열 성분과 같은 지용성 물질의 항바이러스 활성을 평가한 연구는 상대적으로 부족하다.
이러한 상황에서, 다양한 생리활성을 가진 약용 식물로 주목받고 있는 단삼 (Salvia miltiorrhiza)은 꿀풀과에 속하는 다년생 식물로서 뿌리를 약재로 사용하며, 심혈관계 질환 치료뿐 아니라 항염증, 항암, 항균 효과 등 광범위한 약리 활성이 보고되어 왔다 (Zhou et al., 2011; Wang et al., 2015; Gao et al., 2018; Cui et al., 2023).
단삼의 주요 활성 성분은 추출 용매에 따라 크게 수용성 및 지용성 그룹으로 나뉘며, 수용성 성분에는 salvianolic acid B, lithospermic acid, rosmarinic acid, danshensu 등이 있으며, 지용성 성분으로는 tanshinone I, tanshinone IIA, cryptotanshinone, dihydrotanshinone I 등이 포함된다 (Li, 1998; Li et al., 2010). 수용성 성분들은 강력한 항산화 작용을 통해 세포를 보호하며, 지용성 성분은 항균, 항염, 세포 탈과립 억제 등 면역 조절 효과를 나타낸다 (Liu et al., 1992; Lee et al., 1999; Ryu et al., 1999).
이러한 생리활성에 기반하여, 단삼의 항바이러스 효과는 다양한 병원체를 대상으로 보고되고 있다. 단삼 물 추출물은 인플루엔자 바이러스 감염 모델에서 생존율을 높이고 바이러스 복제를 억제하였으며 (Lee et al., 2018), enterovirus 71 (EV71) 감염 세포에서 RNA 합성 억제 및 세포 사멸 감소 효과를 나타냈다 (Wu et al., 2007). 또한 salvianolic acid B는 VP1 발현 억제와 eIF4G1 절단 억제를 통해 세포 생존 경로를 조절하였으며 (Kim et al., 2019), rosmarinic acid는 바이러스 입자의 숙주 수용체 결합을 차단해 선택적 항바이러스 활성을 나타내었다 (Hsieh et al., 2020). 또한 lithospermic acid A와 B는 세포에 대한 낮은 독성과 함께 HIV-1 integrase 활성을 억제하여 항바이러스 활성을 나타냄이 보고되었다 (Abd-Elazem et al., 2002).
그러나 이러한 연구에서 단삼의 항바이러스 활성에 대한 검정과 활성을 나타내는 핵심 물질은 주로 수용성 페놀 화합물에 집중되어 있으며, 지용성 tanshinone 계열 화합물의 항바이러스 연구는 상대적으로 제한적이었다. 최근 연구에 따르면 tanshinone I 및 IIA는 다양한 RNA 바이러스에서 viral L protein의 endonuclease domain에 결합하여 캡 절단 (cap-snatching)을 억제함으로써 바이러스 복제를 방해하는 것으로 나타났다 (He et al., 2023). 또한, tanshinone IIA sulfonate sodium은 돼지생식기호흡기증후군 (porcine reproductive and respiratory syndrome, PRRS), 중증급성호흡기증후군 코로나바이러스 2 (severe acute respiratory syndrome coronavirus 2, SARS-CoV-2) 및 그 변이주에서 복제 억제와 함께 복제 및 면역 조절에 관여하는 papain-like cysteine protease (PLpro) 효소의 작용을 저해하였고 (Sun et al., 2012; Chen et al., 2022), p38 MAPK 경로 억제를 통해 염증 반응 완화와 항바이러스 효과를 동시에 보였다고 보고되었다 (Valipour, 2023; Yang et al., 2023).
이처럼 지용성 tanshinone 계열 성분은 광범위한 항바이러스 활성을 지니는 것으로 보이나, NoV와 같은 장관 바이러스에 대한 직접적인 효과는 아직 명확히 규명되지 않았다. 단삼은 50여 종의 수용성 및 30여 종의 지용성 성분을 함유하고 있으며, 이들의 조성과 함량은 추출 용매에 따라 크게 달라진다 (Zhou et al., 2005). 95% 에탄올 추출 시 지용성 tanshinone 성분이 주로 얻어지며, 물 추출 시에는 주로 폴리페놀 계열의 수용성 성분이 포함된다 (Tran et al., 2021). 따라서 이러한 추출 용매에 따른 조성 차이는 항바이러스 활성을 포함한 다양한 생리활성에 중요한 영향을 미칠 수 있기 때문에 단삼 유래 성분의 항바이러스 활성의 작용 시점 및 기전을 구체적으로 분석하고 평가하는 연구가 필요하다.
본 연구에서는 NoV 대체 바이러스인 FCV를 감염 모델로 설정하고, 단삼 물 추출물과 95% 에탄올 추출물의 항바이러스 활성을 비교·평가하였다. 각 추출물의 유효성분을 HPLC로 정량 분석한 후, plaque reduction assay 및 time-of-addition 모델을 기반으로 한 TCID50 assay를 통해 바이러스 억제 정도와 작용 시점을 분석하였다. 이를 통해 추출 용매에 따라 변화하는 tanshinone IIA 함량과 항바이러스 효과 간의 상관성을 규명하고자 하였다.
재료 및 방법
1. 단삼 물 추출물 (SM-DW) 및 에탄올 추출물 (SM-E)의 제조
국내산 단삼 품종 ‘다산’ (Salvia miltiorrhiza Bunge)은 2021년 4월에 수확 및 건조한 것을 농촌진흥청 국립원예특작과학원 인삼특작부 (Eumseong, Korea)로부터 제공받았다. 원료는 분쇄기로 미세 분쇄한 후, 50호 표준체 (300 ㎛)를 통과시켜 균일한 입도의 분말 시료로 제조하였다.
SM-DW와 SM-E은 각각 증류수 및 5% acetic acid가 첨가된 95% ethanol을 용매로 하여 추출하였다. 에탄올 추출에 산성 에탄올을 사용한 이유는, tanshinone 계열의 추출 효율이 다른 농도 조건보다 95% ethanol에서 높았다는 연구 결과 (Tran et al., 2021)와, 약산성 에탄올 조건이 홍삼 내 유사 성분의 추출에 유리하였다는 연구 (Zhu et al., 2013)를 반영하였다.
각 추출은 분말 시료 45 g에 해당 용매 2,250 ㎖를 첨가한 뒤, 실온에서 30 분간 초음파 추출기 (UCP-20, 120 V, 60 ㎐, JeioTech, Daejeon, Korea)를 이용하여 수행하였다. 추출액은 여과지 (No. 6, Whatman International Ltd., Maidstone, England)를 통해 여과한 후, 감압 농축기 (Eyela Co., Ltd., Tokyo, Japan)를 이용해 농축하였다. 이후 동결건조기 (TFD5503, IlsinBioBase, Dongducheon, Korea)에서 분말 형태로 건조하고, 4℃에서 밀봉하여 보관하였다.
2. 단삼 추출물에서 수용성 페놀계 그룹과 지용성 tanshinone 계열의 성분 함량 분석
SM-DW, SM-E에 포함된 수용성 페놀계 및 지용성 tanshinone 계열 성분의 함량을 분석하기 위해, 각 시료를 10 ㎎/㎖의 농도로 추출 용매에 희석한 뒤 0.20 ㎛ syringe filter (13JP020AN, Advantec Mfs. Inc., Dublin, CA, USA)로 여과하였다.
HPLC 분석에는 총 14 종의 표준품을 사용하였으며, 수용성 페놀계 화합물은 danshensu (DS), protocatechuic aldehyde (PCA), vanillic acid (VA), caffeic acid (CA), rosmarinic acid (RA), lithospermic acid (LA), salvianolic acid B (Sal B), salvianolic acid A (Sal A), salvianolic acid C (Sal C), protocatechuic acid (PA)였으며, 지용성 tanshinone 계열은 dihydrotanshinone I (DHTS), cryptotanshinone (CT), tanshinone I (Tan I), tanshinone IIA (Tan IIA)였다. 표준품 중 DS, PCA, VA, CA, RA, LA, Sal B, DHTS, CT, Tan I, Tan IIA는 Sigma-Aldrich (St. Louis, MO, USA)에서, Sal A 및 Sal C는 Med-ChemExpress (Romulus, MI, USA)에서, PA는 HWI pharma services GmbH (Germersheim, Germany)에서 구입하였다.
각 표준물질은 5 ㎍/㎖, 10 ㎍/㎖, 20 ㎍/㎖, 40 ㎍/㎖, 80 ㎍/㎖의 농도로 희석하여 분석에 사용하였으며, 표준 곡선을 작성해 회귀방정식 및 결정계수 (R²)를 산출하였다. 실제 시료 내 성분 함량은 HPLC 크로마토그램 면적 값을 표준 곡선에 대입하여 계산하였다. 분석법은 Chen 등 (2012)의 시험법 밸리데이션이 확인된 동시 분석법을 기반으로 일부 조건을 변형하여 적용하였다 (Table 1).
3. 세포 및 바이러스의 배양
본 연구에 사용한 FCV (VR-782)는 American Type Culture Collection (ATCC, Manassas, VA, USA)에서 분양받았으며, 숙주세포인 Crandell-Reese feline kidney (CRFK, CCL-94)는 한국세포주은행 (KCLB, 10094, Seoul, Korea)에서 제공받아 사용하였다.
CRFK 세포는 75 ㎠ tissue culture flask (SPL Life Science, Pocheon, Korea)에서 10% fetal bovine serum (FBS; GIBCO, Grand Island, NY, USA), 1% antibiotics/antimycotics (AA, GIBCO, Grand Island, NY)가 포함된 Dulbecco's Modified Eagle's Medium (DMEM; GIBCO, Grand Island, NY, USA)에서 37℃, 5% CO2 조건의 배양기 (MCO-170AC, PHcbi, Wood Dale, IL, USA)에서 배양하였다. 세포가 90% 이상 밀집 상태에 도달한 경우 계대 배양하여 실험에 사용하였다.
FCV 증식을 위해서 단층 (monolayer) 상태의 CRFK 세포에 바이러스 배양액을 접종하고 37℃에서 90 분간 흡착시켰으며, 이후 2% FBS가 포함된 유지배지 (maintenance medium, DMEM)를 첨가해 37℃, 5% CO2 조건에서 16 시간에서 24 시간까지 배양하였다.
세포병변효과 (cytopathic effect, CPE)가 뚜렷해지면 부착 세포가 탈락하게 되는데, 이 시점에서 동결-해동을 2 회 반복하여 세포를 파쇄한 후 1,500 × g에서 15 분간 원심 분리하였다. 상등액은 세포 잔해를 제거한 뒤 cryogenic vial (SPL Life Science, Pocheon, Korea)에 0.5 ㎖씩 나누어 바이러스 stock으로 저장하였으며 사용할 때까지 –80℃에 보관하였다.
4. 세포 독성 시험
SM-DW, SM-E의 항바이러스 활성을 평가하기에 앞서, FCV의 숙주세포인 CRFK 세포에 대한 세포 독성을 확인하여 각 추출물의 최대 무독성 농도 (MNCC, maximum non-cytotoxic concentration)를 설정하였다. 세포 독성 평가를 위한 SM-DW와 SM-E의 농도 범위는 SM-DW의 인플루엔자 바이러스에 대한 항바이러스 활성 검정에서 HEK293T 세포주나 HeLa 세포주에 사용된 농도 범위 (1 ㎍/㎖ - 100 ㎍/㎖)를 참조하였으며 (Lee et al., 1998) 연속적인 단계 희석법을 이용하여 MNCC 설정을 위한 최적의 농도 범위를 검정하였다.
CRFK 세포는 96-well plate에 well 당 6.3 × 103 cells로 분주하고, 80% 밀집 상태에 도달할 때까지 배양하였다. 이후 SM-DW (1.09 ㎎/㎖ - 108.75 ㎎/㎖)와 SM-E (0.022 ㎎/㎖ - 0.218 ㎎/㎖)를 단계별로 희석해 각 well에 처리한 뒤, 2 시간 동안 배양하고 그 후 신선한 DMEM으로 교체해 24 시간 추가 배양하였다. 세포 생존율 평가는 WST-1 assay로 진행되었으며, 시약은 EZ-cytox (DoGenBio, Seoul, Korea)를 사용하고 흡광도는 450 ㎚ 에서 microplate reader (SpectraMax ABS, Molecular Devices, LLC, CA, USA)로 측정하였다.
음성대조군으로 추출물이 포함되지 않은 DMEM 단독 배지를, 양성 대조군은 0.1% sodium dodecyl sulfate (SDS)를 사용하였다. 세포 생존율은 음성대조군 대비 상대 흡광도 비율로 계산하였으며, 95% 이상 세포 생존율을 보이는 농도를 MNCC로 판단하고 이후 항바이러스 실험에 사용하였다.
5. 플라크 감소 시험 (plaque reduction assay)
CRFK 세포를 이용하여 FCV의 감염성과 SM-DW, SM-E 처리 효과를 평가하였다. 실험 하루 전, CRFK 세포를 well 당 1.8 × 105 cells로 분주해 37℃, 5% CO2 조건에서 부착 배양하였다. FCV stock 농도는 1 × 106 – 5 × 107 pfu/㎖로 측정되었으며 이를 기반으로 plaque assay에 적합한 희석 범위를 설정하였다.
SM-DW 및 SM-E는 각각 MNCC 농도 (5.44 ㎎/㎖ 및 0.174 ㎎/㎖)로 조제하여 FCV stock과 혼합한 뒤, 30 분간 반응시켰다. 혼합액은 성장 배지로 10 배 연속 희석하여, 바이러스 희석액을 준비하였다. 감염성 및 세포층 박리 효과를 고려하여, 희석 배수는 102에서 105까지 설정하였다.
배양된 CRFK 세포에서 상층 배지를 제거하고, 각 희석 바이러스 용액을 200 ㎕씩 접종하였다. 37℃, 5% CO2 조건에서 2시간 동안 흡착 배양 후, overlay medium (1.5% agarose와 배지를 1 : 1로 혼합)을 well 당 4 ㎖씩 분주해 고형화하였다.
Overlay media가 굳은 것을 확인한 뒤 plate를 다시 37℃, 5% CO2 incubator에 넣어 24 시간 배양하였다. 현미경 관찰을 통해 CPE가 80% 이상 관찰되면 세포를 4% formaldehyde로 30 분 이상 고정하였다. Overlay를 제거하고 1% crystal violet 용액 (DAEJUNG, Siheung, Korea)으로 염색 후, 증류수로 세척하고 상온에서 건조하였다.
플라크 수는 ImageJ 64-bit Java 8 (National Institutes of Health Bethesda, MD, USA)로 정량 분석하였다. 각 실험은 4회 반복하였으며 음성대조군 (무처리군)과 비교하여 바이러스 역가를 계산하였다. 역가는 다음 식으로 산출하였고 PFU (plaque forming unit)/㎖의 값을 로그 변환하여 분석하였다.
6. FCV 바이러스 감염력 변화를 통한 항바이러스 검정
FCV의 항바이러스 활성은 50% tissue culture infectious dose (TCID50)를 측정하는 end-point dilution assay로 평가하였다. 감염 후 5 일째에 CPE를 관찰하고, 50% 이상 CPE가 나타난 well의 희석 단계를 기준으로 Reed-Muench method를 적용해 TCID50 값을 산출하였다 (Hierholzer and Killington, 1996). 최종 결과는 log10 TCID50/㎖로 표시하였다.
SM-DW 및 SM-E의 항바이러스 활성을 평가하기 위해 time-of-addition 모델을 적용하여 세 가지 처리 조건으로 나누어 진행하였다 (Fig. 1).
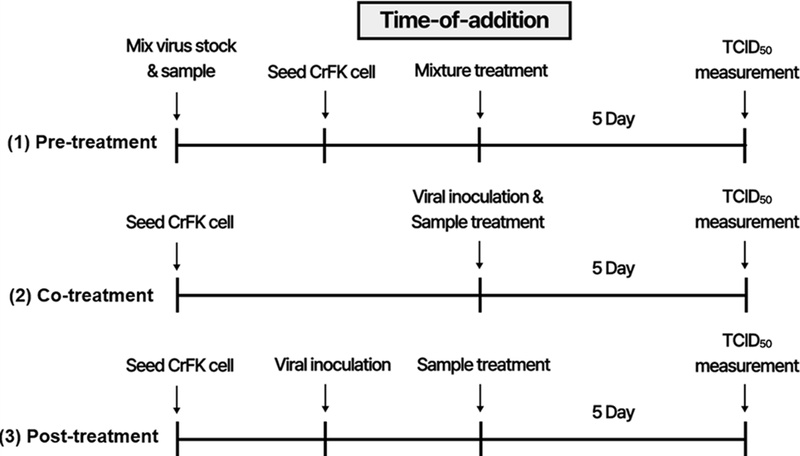
Schematic representation of the time-of-addition assay to evaluate antiviral activity of S. miltiorrhiza extracts against feline calicivirus (FCV).To investigate the antiviral activity of the water extract (SM-DW) and ethanol extract (SM-E) of S. miltiorrhiza, a time-of-addition assay was performed using Crandell-Rees feline kidney (CRFK) cells and feline calicivirus (FCV). The assay consisted of three treatment conditions: (1) Pre-treatment, where the virus and extract were pre-incubated prior to CRFK cell seeding and infection; (2) Co-treatment, where the extract and virus were simultaneously applied to pre-seeded CRFK cells; and (3) Post-infection treatment, where the extract was administered after viral infection had occurred. After 5 days of incubation, antiviral efficacy was determined using the 50% tissue culture infectious dose (TCID50) method based on end-point dilution assay. Viral titers were calculated and expressed as TCID50/㎖ in logarithmic scale, and compared across treatment groups to evaluate inhibitory effects of the extracts at different stages of the viral life cycle.
전처리 모델 (pre-treatment)에서는 바이러스를 세포에 접종하기 전에 추출물과 반응시켜 항바이러스 효과를 확인하였다. FCV stock 원액에 SM-DW (5.44, 2.72, 1.09 ㎎/㎖) 또는 SM-E (0.174, 0.087, 0.022 ㎎/㎖)를 첨가해 4℃에서 24 시간 동안 반응시킨 뒤 10 배 연속 희석하여 CRFK 세포에 접종하고 37℃, 5% CO₂조건에서 5 일간 배양하였다.
동시 처리 모델 (co-treatment)의 경우 추출물과 바이러스를 동시에 세포에 처리하여 항바이러스 활성을 평가하였다. SM-DW 및 SM-E를 각각 무독성 농도의 3 단계 (전처리 모델과 동일 농도 범위)로 희석하고 FCV 희석액과 함께 CRFK 세포와 함께 각 well에 동시에 접종하여 5 일간 배양하였다.
감염 후 처리 모델 (post-treatment)은 FCV 감염 이후 추출물을 처리하는 방식으로 항바이러스 효과를 분석하였다. CRFK세포에 FCV를 접종 후 phosphate buffered saline (PBS)로 세척한 뒤, SM-DW 또는 SM-E의 희석액 (전처리 모델과 동일 농도 범위)을 처리하고 5 일간 배양하였다.
각 배양이 종료된 후, 각 처리군의 바이러스 역가를 측정하여 감염 후 억제 효과를 대조군과 비교하였다.
7. 통계분석
모든 검정은 4 회 반복 수행되었고, 각 항목별 실험은 3 회 반복하였다. 측정값은 평균 ± 표준 편차 (mean ± standard deviation)로 표현하였다. 각 처리군과 대조군 간의 평균값의 유의성은 Student’s t-test (*p < 0.05)로 검정하였으며 통계 분석은 SAS Enterprise Guide 9.4 (Statistical analysis system, 2009, Cary, NC, USA)를 사용하였다.
결과 및 고찰
1. SM-DW 및 SM-E의 수용성·지용성 성분 함량 특성
SM-DW와 SM-E에 함유된 수용성 페놀계 그룹 및 지용성 tanshinone 계열 총 14 종에 대해 HPLC로 함량을 정량 분석하였다. 결과는 추출물 1 ㎎당 함량 (㎍/㎎·EX)으로 표기하였으며, 성분의 물리화학적 특성을 고려해 수용성과 지용성으로 구분하였다 (Fig. 2).
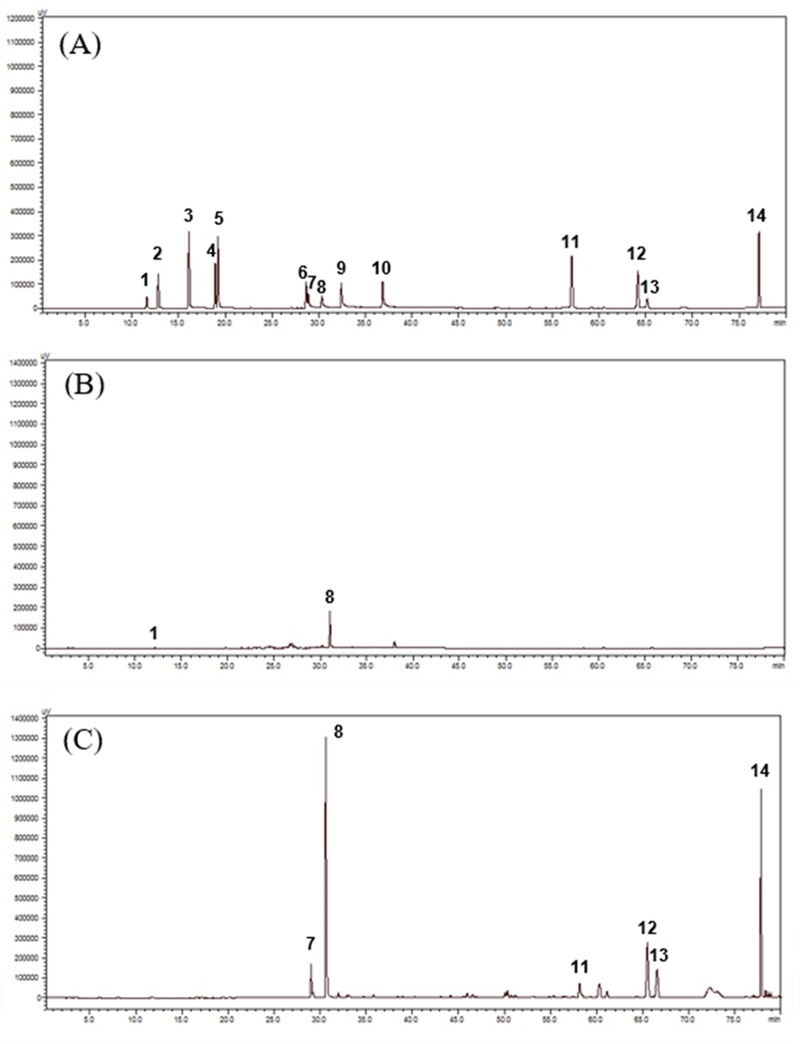
HPLC chromatogram of 14 pharmaceutical constituents in water (SM-DW) and 95% ethanol containing 5% acetic acid extract (SM-E) of S. miltiorrhiza.(A); standard mixture (10 ㎍/㎖, 1; danshensu (DS, R2=0.9992, y=7098.2x-27993), 2; protocatechuic acid (PA, R2=0.9971, y=70367x-358923), 3; protocatechuic aldehyde (PCA, R2=0.9999, y=34167x-55650), 4; vanillic acid (VA, R2=0.9995, y=14155x+7365), 5; caffeic acid (CA, R2=0.9994, y=32719x-320132), 6; rosmarinic acid (RA, R2=0.9927, y=7842.1x-76762), 7; lithospermic acid (LA, R2=0.9949, y=12680x-179771), 8; salvianolic acid B (Sal B, R2=0.9936, y=29340x-157971), 9; salvianolic acid A (Sal A, R2=0.9965, y=24927x-494795), 10; salvianolic acid C (Sal C, R2=0.9939, y=10218x-154256), 11; dihydrotanshinone I (DHTS, R2=0.9982, y=60408x-418237), 12; cryptotanshinone (CT, R2=0.9927, y=24681x-129808), 13; tanshinone I (Tan I, R2=0.9958, y=7161.7x-816.83), 14; tanshinone IIA (Tan IIA, R2=0.9978, y=52462x-5120.3), (B); water extract (SM-DW) of S. miltiorrhiza. (C); 95% ethanol containing 5% acetic acid extract (SM-E) of S. miltiorrhiza. All extract was treated ultrasound (120V, 60Hz) for 30 minutes in each solvent, filtered, and lyophilized.
추출수율은 SM-DW가 38.17%, SM-E가 17.88%로, SM-DW에서 약 2 배 이상 높았다. 이는 물의 강한 극성으로 인해 수용성 페놀류뿐만 아니라 다당류 등 수용성 고분자 화합물의 용출이 용이하기 때문으로 해석된다.
수용성 페놀계 화합물 중 caffeic acid는 SM-DW에서 0.41 ± 0.03 ㎍/㎎·EX로 SM-E (0.05 ± 0.01 ㎍/㎎·EX) 대비 약 9 배 높았다. Danshensu (DS)는 두 추출물 간의 유의한 차이가 없었으나 SM-E에서 약간 높은 경향을 보였다 (Table 2). Salvianolic acid A, B, C는 SM-E에서 각각 약 12 배, 23 배, 7 배 더 높은 함량을 보였으며, 이는 유기 용매 추출 조건이 해당 성분의 용출에 효과적임을 시사한다.

Hydrophilic phenolic acids contents of water (SM-DW) and 95% ethanol containing 5% acetic acid extract (SM-E) in S. miltiorrhiza.
지용성 tanshinone 계열의 경우, tanshinone IIA는 SM-DW에서 0.08 ± 0.01 ㎍/㎎·EX에 불과했으나 SM-E에서는 28.45 ± 0.13 ㎍/㎎·EX로 SM-DW 보다 356 배 높은 함량을 나타냈다 (Table 3). Dihydrotanshinone I (DHTS), cryptotanshinone (CT), tanshinone I (Tan I) 역시 SM-E에서 SM-DW에 대하여 각각 67배, 26 배, 28 배 더 높은 함량으로 검출되었다.

Hydrophobic diterpenoid quinone of water (SM-DW) and 95% ethanol containing 5% acetic acid extract (SM-E) in S. miltiorrhiza.
추출물의 수율을 고려하여 단삼 분말 기준 1 g당 함량으로 환산한 결과 에서도 동일한 경향이 관찰되었으며 (자료 미제시), SM-E는 salvianolic acid B (7,745.45 ± 940.57 ㎍/g·DW)는 SM-DW (742.37 ± 80.18 ㎍/g·DW) 대비 약 10 배 이상 높았다. SM-E에서 지용성 성분은 SM-DW 대비 DHTS는 29 배, CT의 경우 12 배, Tan I은 13 배, Tan IIA의 경우 156 배 이상으로 높았다 (자료 미제시).
전통적으로 단삼 추출에는 물을 용매로 사용하는 환류·연속 환류 추출법이 사용되며, 이러한 추출 방법은 고온·고압의 추출 조건을 적용하는데 유리하나, 추출에 시간이 오래 걸리며 단삼의 추출 과정에서 적용되는 가열 조건이 salvianolic acid B를 danshensu와 lithospermic acid로 분해시킬 우려가 있다는 점 (Gong et al., 2017)과 tanshinone 계열 성분 추출 효율이 낮다는 한계가 있다 (Ong and Len, 2004).
단삼은 다양한 생리활성 성분을 함유하고 있으며, 이들에 기인한 약리적 효능 또한 복합적으로 나타나기 때문에 질환에 따라 유효한 성분이 높은 함량으로 확보될 수 있는 추출법을 구분해 적용할 필요가 있다. 이를 위해 대상 성분의 특성에 맞는 용매와 추출 조건을 설정하고, 안전성과 효율성을 동시에 고려한 공정 개발이 요구된다.
본연구의 추출 방법인 초음파 보조 추출법 (ultrasound-assisted extraction)은 용매 소모를 줄이면서 추출 시간을 단축시킬 수 있는 장점이 있으며 (Gallo et al., 2010), 짧은 추출 시간으로 인해 가열이 필요하지 않아 열에 민감한 유용 성분의 열분해를 방지할 수 있다는 점에서 (Pan et al., 2002), 기존의 환류 추출법 등과 비교해 유리한 조건으로 평가된다. 또한, 전통적인 에탄올 추출법은 단순하고 조작이 쉬우며, 지용성 성분의 추출 효율이 우수하여 현재까지도 널리 활용되고 있다.
이외에도 약용작물로부터 천연물을 효율적으로 추출하기 위한 방법으로 초음파 보조 추출법 (ultrasound-assisted extraction) 뿐만 아니라 초임계유체 추출 (supercritical fluid extraction, Wang et al., 2008), 계면활성제 보조 추출 (surfactant-assisted extraction, Bi et al., 2010), 압력 액체 추출 (pressurized-liquid extraction, Jiang et al., 2010), 이온성액체기반고압추출 (ionic liquid-based ultrahigh pressure extraction, Liu et al., 2013) 등이 보고되고 있으며, tanshinone 계열 성분의 추출에 있어 이들 추출 방법을 적용하여 선택성과 수율을 개선하는 데 활용할 수 있을 것으로 생각된다.
따라서 본 연구에서 제시한 5% acetic acid를 포함한 95% ethanol 기반의 초음파 보조 추출은 수용성 페놀계 및 지용성 tanshinone 계열의 성분 함량 모두에 대해 높은 추출 효율을 나타내는 방식으로 평가되며, 특히 항바이러스 활성이 강하게 나타난 SM-E의 경우, 고함량의 tanshinone IIA가 주요 작용성분으로 작용할 가능성을 뒷받침하는 중요한 결과로 판단된다.
2. SM-DW 및 SM-E의 세포 독성 평가
CRFK 세포를 이용해 SM-DW와 SM-E의 세포 독성을 평가하고, MNCC를 산정하였다 (Fig. 3). SM-DW과 SM-E는 CRFK 세포에 대해 서로 다른 세포 독성을 나타내었으며 SM-E는 0.217 ㎎/㎖의 비교적 낮은 농도에서 세포 생존율이 81.9%로 감소하여 독성이 나타났으나, SM-DW는 10.88 ㎎/㎖의 이상에서 세포 생존율이 낮아져 상대적으로 세포 독성이 낮은 추출물로 확인되었다.
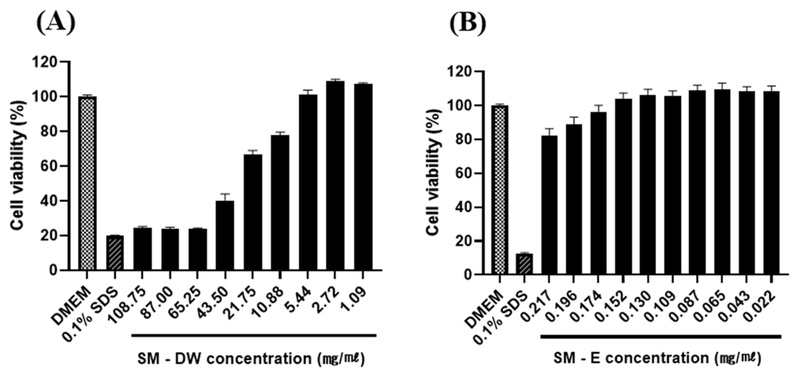
CRFK cell cytotoxicity of water (SM-DW) and 95% ethanol containing 5% acetic acid extract (SM-E) of S. miltiorrhiza was assessed by the WST-1 assay.(A); SM-DW, (B); SM-E. The maximum non-cytotoxic concentration (MNCC) were 5.44 ㎎/㎖ and 0.174 ㎎/㎖ for SM-DW and SM-E, respectively. This experiment was performed as quadruplicates.
음성 대조군으로 사용된 배지 단독 처리군 (DMEM)은 세포 생존율에 영향을 주지 않았다. SM-DW의 경우 5.44 ㎎/㎖ (101.2% 세포 생존율), SM-E에서 0.174 ㎎/㎖ (96.1%, 세포 생존율)에서 세포의 부착성과 증식에도 영향을 주지 않아 MNCC를 설정하였다. 이는 용매 특성과 성분 함량 차이에 따른 독성 차이를 반영하며, 이후 실험은 각 MNCC를 기준으로 수행하였다 (Fig. 3).
3. SM-DW 및 SM-E의 plaque reduction assay 기반 FCV 항바이러스 활성 평가
FCV를 대상으로 SM-DW 및 SM-E를 최대 무독성 농도 (SM-DW 5.44 ㎎/㎖, SM-E 0.174 ㎎/㎖)로 처리하고 plaque reduction assay를 통해 항바이러스 활성은 정량적으로 분석한 결과를 제시하였다 (Fig. 4A).
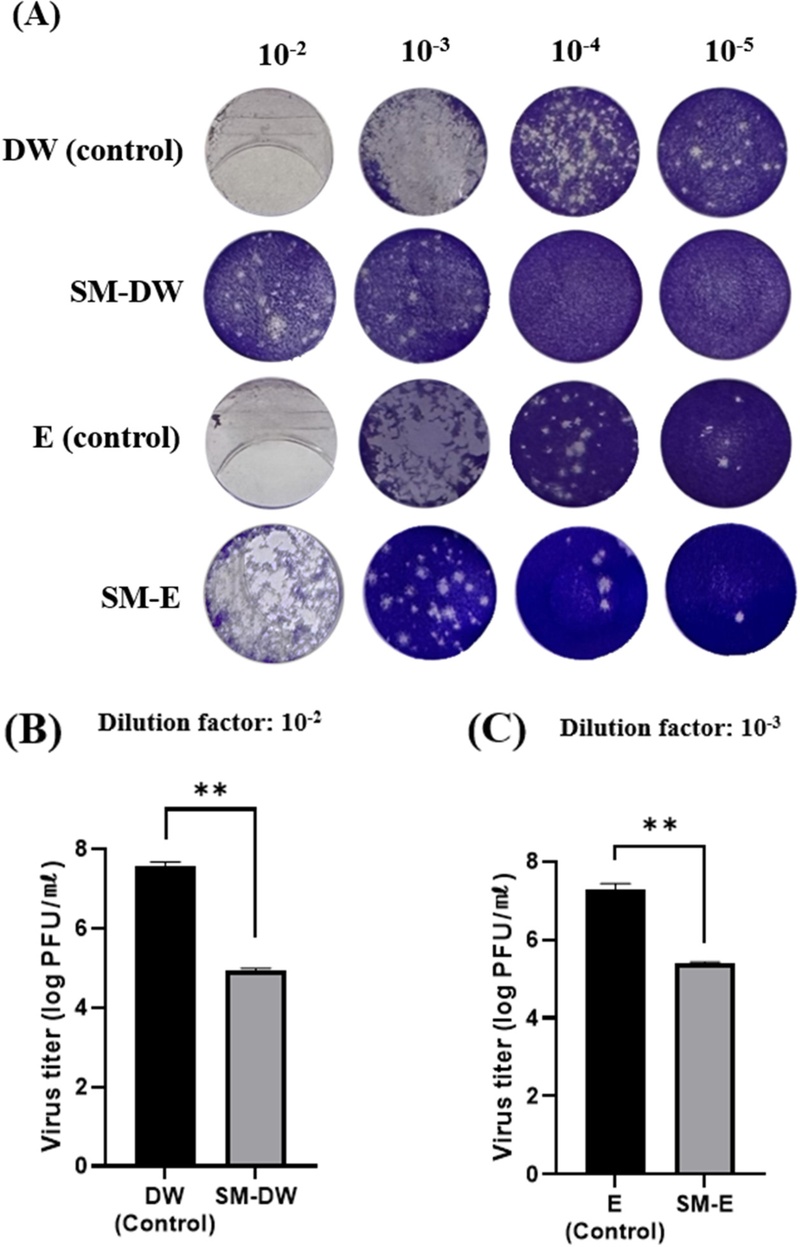
Antiviral activity of water (SM-DW) and 95% ethanol containing 5% acetic acid extract (SM-E) of S. miltiorrhiza against feline calicivirus (FCV) by plaque reduction assay.FCV was infected into Crandall-Reese feline kidney cells and incubated in the presence or absence of water (SM-DW) and 95% ethanol containing 5% acetic acid extract (SM-E) of S. miltiorrhiza. Antiviral activity was expressed as a comparative photographs to inhibit virus-induced plaque, compared with control as extraction solvents (A). Titer of surviving FCV (log PFU/㎖) to SM-DW compared with control (DW) as extraction solvents (B). Titer of surviving FCV (log PFU/㎖) to SM-E compared with control (E) as extraction solvents. This experiment was performed as quadruplicates. Significantly different according to Student’s t-test (**p < 0.01).
SM-DW 처리군은 10-2 희석 조건에서 plaque 수가 미처리 대조군 대비 99.784% 감소하였으며, 바이러스 역가는 물만 처리한 음성대조군 (DW)의 7.5638 ± 0.1077 log PFU/㎖에 비하여 4.9256 ± 0.0667 log PFU/㎖ 로 약 2.64 log 감소하였다 (Fig. 4B).
SM-E 처리군의 경우, 10-3 희석 조건에서 98.699%의 항바이러스 억제율을 나타내었으며, 5% acetic acid를 포함한 95% ethanol 처리 대조군 (E)의 바이러스 역가가 7.2764 ± 0.1585 log PFU/㎖ 인데 반하여 SM-E 처리군은 5.4102 ± 0.0247 log PFU/㎖로, 약 1.89 log 감소하였다 (Fig. 4B).
두 추출물 모두 FCV에 대해 유의한 항바이러스 활성을 나타냈지만, SM-E는 SM-DW에 비해 약 30 배 낮은 농도에서도 유사한 수준의 항바이러스 효과를 보였다. 이는 성분 분석 결과와 일치하며, 특히 SM-E에는 tanshinone IIA를 포함한 지용성 diterpenoid 계열 성분이 SM-DW보다 월등히 높은 농도로 존재하였고, 이러한 성분들이 바이러스 증식 억제의 주요 활성 인자로 작용했을 가능성이 크다. 이로써 SM-E는 상대적으로 낮은 농도로도 강력한 항바이러스 활성을 유도할 수 있는 유망한 천연 추출물임을 시사한다고 하겠다.
4. SM-DW 및 SM-E의 time-of-addition 모델 기반 항바이러스 활성 비교
단삼 추출물의 항바이러스 작용 시점을 명확히 규명하고자, time-of-addition assay를 통해 pre-treatment, co-treatment, post-treatment의 3 가지 조건별로 FCV에 대한 억제 효과를 비교하였다 (Fig. 5).
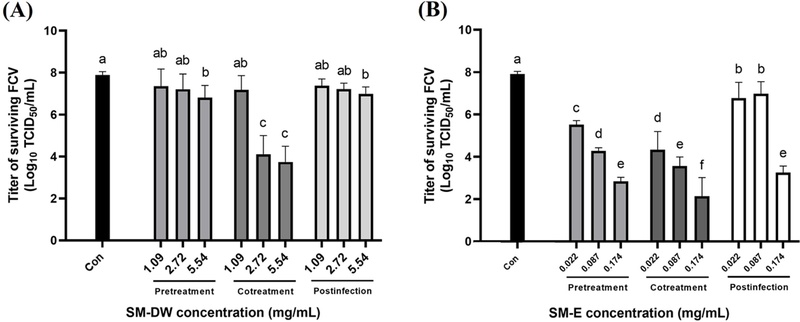
Anti-feline calicivirus (FCV) activity water extract (SM-DW) and ethanol (SM-E) extracts of S. miltiorrhiza in Crandell-Reese feline kidney (CRFK) according to time-of-addition model (pretreatment, cotreatment and postinfection treatment).(A) Time-of-addition experiment results for the water extract (SM-DW) of S. miltiorrhiza. (B) Time-of-addition experiment results for the ethanol extract containing 5% acetic acid (SM-E) of S. miltiorrhiza. Three concentrations (MNTC and two lower concentrations) of each extract were used. Pretreatment; Feline calicivirus (FCV) with natural extracts on virus titer. FCV was pretreated with non-diluted extracts for 24 h at 4℃. Cotreatment; three concentrations of each extract were used for treating CRFK simultaneously with viral for treating CRFK simultaneously with viral infection. Postinfection treatment; three concentrations each extract were used for treating CRFK 2 h after viral infection. Data are the average of triplicate experiments. Error bars represent standard deviations. MNTC; maximum nontoxic concentration. TCID50; 50% tissue culture infectious dose of the virus. Data are presented as the mean ± standard deviation (n = 5). Means with different letters in the same column are significantly different by Duncan’s multiple range test (DMRT, *p < 0.05).
SM-DW를 pre-treatment 조건으로 처리한 경우, 고농도 (5.44 ㎎/㎖)의 바이러스 역가는 6.81 ± 0.58 log TCID50/㎖로 미처리 대조군 (7.89 ± 0.16 log TCID50/㎖) 대비 1.08 log의 유의미한 바이러스 역가 감소가 관찰되었으며 SM-DW가 바이러스와의 직접 접촉을 통해 CRFK 세포로의 초기 부착을 차단한 결과로 해석된다. 중간 농도 (2.72 ㎎/㎖) 및 저농도 (1.09 ㎎/㎖)에서는 7.21 ± 0.73 log TCID50/㎖, 7.35 ± 0.82 log TCID50/㎖로 대조군 대비 감소 경향이 있었으나, 고농도에서와 같은 뚜렷한 억제 효과는 나타나지 않았다 (Fig. 5A, p < 0.05).
이는 SM-DW가 특정 농도 이상으로 적용하는 경우 SM-DW에 포함된 수용성 성분이 바이러스 입자와 상호 작용하여 초기 감염을 부분적으로 억제할 수 있음을 시사한다고 하겠다.
SM-DW를 co-treatment 조건으로 처리한 경우, 중간 농도 이상 (2.72, 5.44 ㎎/㎖)에서 바이러스 역가는 4.11 ± 0.89 log TCID50/㎖와 3.74 ± 0.75 log TCID50/㎖를 나타나 대조군 (7.89 ± 0.16 log TCID50/㎖) 대비 각각 3.78 및 4.15 log 감소를 나타내어 유의미한 바이러스 억제 효과가 확인된 반면, 1.09 ㎎/㎖의 저농도를 적용한 경우, 바이러스 역가는 7.18 ± 0.68 log TCID50/㎖로 나타나 대조군과 차이를 보였지만, 중간 농도 이상 (2.72, 5.44 ㎎/㎖)에서 확인된 수준의 항바이러스 활성을 나타내지 못하였으며 통계적 유의성도 낮았다 (Fig. 5A, p < 0.05). 이는 SM-DW가 바이러스의 세포 진입 및 초기 증식 억제에 효과적으로 작용하기 위해서는 특정 농도 (2.72 ㎎/㎖) 이상의 농도가 되어야 함을 의미한다고 할 수 있다.
SM-DW를 post-infection 조건으로 처리한 경우, 바이러스 역가는 1.09 ㎎/㎖의 농도에서 7.38 ± 0.32 log TCID50/㎖, 2.72 ㎎/㎖의 농도에서 7.22 ± 0.28 log TCID50/㎖, 5.44 ㎎/㎖의 농도에서는 6.99 ± 0.33 log TCID50/㎖ 를 나타내 각각 대조군 (7.89 ± 0.16 log TCID50/㎖) 대비 0.51, 0.67 및 0.90 log의 수준으로 감소하는 경향이 있었으나, 감소 폭은 제한적이었다 (Fig. 5A, p < 0.05). 모든 농도에서도 비교적 낮은 수준의 억제 효과만이 관찰되었으며, 이는 SM-DW가 감염 이후 복제·방출 단계에 대해서는 제한적인 억제능을 갖고 있음을 나타낸다고 하겠다.
Bellamy (1995)의 기준에 따르면 log TCID50 값이 4 log 이상 감소할 경우 항바이러스 효과가 있다고 평가되는데, SM-DW는 co-treatment 조건에서 해당 기준에 근접하는 가장 유의미한 억제 효과를 보였으며 pre-treatment 및 post-treatment에서는 농도 의존적 경향이 확인되었으나 상대적으로 효과가 낮았다. 따라서 SM-DW는 주로 바이러스의 세포 진입 단계에서 효과적으로 작용하며, 바이러스의 숙주세포로의 초기 부착 차단이나 감염 후 억제 효능은 상대적으로 낮은 것으로 판단된다.
SM-E를 pre-treatment 조건으로 처리한 경우, 각 농도 (0.022, 0.087, 0.174 ㎎/㎖)에서 바이러스 역가는 5.52 ± 0.19 log TCID50/㎖, 4.28 ± 0.15 log TCID50/㎖, 2.84 ± 0.18 log TCID50/㎖를 나타내어 대조군 (7.92 ± 0.12 log TCID50/㎖) 대비 각각 2.40 log, 3.64 log, 5.08 log의 수준으로 감소하여 FCV에 대한 유의미한 억제 효과가 관찰되었으며, 특히 고농도 (0.174 ㎎/㎖)에서는 가장 강력한 바이러스 역가 감소가 확인되었다 (Fig. 5B, p < 0.05). 이는 SM-E에 포함된 유효 성분, 특히 tanshinone IIA 등 지용성 diterpenoid 성분이 바이러스 외피 또는 캡시드 단백질에 직접 작용하여 숙주세포 부착을 억제할 수 있음을 시사한다.
SM-E를 co-treatment 조건으로 처리한 경우, 모든 농도 (0.022, 0.087, 0.174 ㎎/㎖)에서 바이러스 역가는 4.33 ± 0.86 log TCID50/㎖, 3.56 ± 0.43 log TCID50/㎖, 2.14 ± 0.88 log TCID50/㎖를 나타내어 대조군 (7.92 ± 0.12 log TCID50/㎖) 대비 각각 3.59 log, 4.36 log, 5.78 log의 수준으로 감소하여 FCV 바이러스에 대한 우수한 항바이러스 활성이 관찰되었고, pre-treatment와 비교하여 더 높은 수준의 억제 효과를 나타내었다 (Fig. 5B, p < 0.05). 이는 SM-E가 바이러스의 세포 진입 및 초기 복제 단계에서 탁월한 차단 효과를 발휘할 수 있음을 보여준다.
SM-E를 post-infection 조건으로 처리한 경우, 상대적인 저농도와 중간 농도 (0.022, 0.087 ㎎/㎖)에서 바이러스 역가가 각각 6.78 ± 0.74 log TCID50/㎖와 6.98 ± 0.57 log TCID50/㎖로 대조군 (7.92 ± 0.12 log TCID50/㎖) 대비 유의미한 바이러스 억제 효과가 확인되었으며, 특히 고농도 (0.174 ㎎/㎖)에서 바이러스 역가는 3.25 ± 0.31 log TCID50/㎖ 로 대조군 (7.92 ± 0.12 log TCID50/㎖) 대비 3.59 log 감소를 나타내어 가장 뚜렷한 역가 감소가 관찰되었다 (Fig. 5B, p < 0.05). 이는 SM-E가 감염 이후에도 바이러스 복제 또는 세포 외 방출 단계를 일정 수준 억제할 수 있으며 상대적 고농도에서는 강력한 항바이러스 효과를 나타낼 수 있음을 의미한다. 또한 SM-E는 FCV의 감염 단계별 각각의 작용 시점에서 유의미한 효과를 나타내는 광범위한 항바이러스 작용 스펙트럼을 나타낸다고 할 수 있겠다.
전반적으로 SM-E는 모든 처리 조건에서 농도 의존적인 억제 효과를 보였으며, 특히 pre-treatment 및 co-treatment 단계에서 강력한 항바이러스 활성을 나타내었다. 또한, 감염 후에도 특정 농도 이상에서는 바이러스 복제 또는 세포 외 방출 단계를 억제할 수 있음을 알 수 있었다. 이러한 효과는 SM-E에 함유된 고함량의 유효 성분들에 기인되는 것으로 판단되며 성분 분석 결과에서 확인된 바와 같이, SM-E에 고농도로 함유된 tanshinone IIA 등 지용성 diterpenoid 성분의 작용에 기인한 결과로 해석된다.
본 연구에서 SM-DW과 SM-E는 FCV를 대상으로 다양한 in vitro 항바이러스 평가에서 유의한 억제 활성을 나타냈다. 특히 SM-E는 낮은 농도에서도 뛰어난 항바이러스 활성을 보였고, 바이러스의 세포 부착, 침투, 복제 등 다양한 단계에서 바이러스 증식을 효과적으로 억제할 수 있음을 확인하였다. 또한 SM-E의 항바이러스 효과는 단일 유효 성분의 작용이 아닌 수용성 및 지용성 화합물의 상호작용에 기인하는 것으로 예측되며, 특히 SM-E의 주요 지용성 성분인 tanshinone 계열 화합물의 함량이 이러한 항바이러스 효과의 핵심 역할을 했을 것으로 판단된다.
이러한 항바이러스 효과는 기존의 보고들과 잘 부합되는데, 예를 들어 정향 에센셜 오일 (clove essential oil)이 FCV의 세포 부착 단계를 저해한다는 보고 (Elizaquível et al., 2013)와 다양한 항바이러스 성분의 시너지 작용이 바이러스 억제 효과를 증대시킬 수 있다는 최근 연구 (Gabbianelli et al., 2023)는 본 연구 결과의 해석에 중요한 근거를 제공한다. 특히 propolis 유래 terpenoid 성분들이 인간 노로바이러스 GII.4 및 쥐 노로바이러스 (MNV-1)의 숙주세포 부착 및 침투 단계를 억제한다는 보고 (Liao et al., 2021)는 SM-E의 항바이러스 기전과 유사한 작용 경로를 제시한다고 하겠다.
SM-E의 주요 지용성 성분인 tanshinone 계열 화합물은 p38 mitogen-activated protein kinase (MAPK), extracellular signal-regulated kinase (ERK), c-Jun N-terminal kinase (JNK), nuclear factor kappa B (NF-κB) 등 다양한 염증 및 생존 관련 세포 신호전달 경로에 영향을 미치는 것으로 보고되었다.
Jang 등 (2006)은 tanshinone IIA가 RAW 264.7 대식세포에서 LPS 유도 nuclear factor of kappa light polypeptide gene enhancer in B-cells inhibitor alpha (IκBα) 분해와 NF-κB 활성화를 억제하며, MAPK 경로 (p38, ERK1/2, JNK)의 억제 작용도 확인하였다.
FCV의 숙주세포를 감염시킬 시 p38 경로가 바이러스 유전자의 전사·번역 및 게놈 복제를 촉진하고, cyclooxygenase-2 (COX-2)/prostaglandin E-2 (PGE-2) 경로를 활성화해 면역 억제 및 세포 사멸을 유도한다는 보고 (Chander et al., 2021; Natoni et al., 2006)에 대하여 Akaberi 등 (2016)은 여러 tanshinone 유도체들이 p38 MAPK를 비롯한 주요 염증 신호 경로를 효과적으로 억제함으로써 항염 및 항바이러스 기전을 수행할 수 있음을 강조하였다. 이로 미루어볼 때, SM-E는 풍부한 tanshinone 계열 화합물의 역할에 기인하여 바이러스 부착 억제의 효과와 함께 세포 내 복제 및 신호전달 억제 작용을 함께 수행했을 가능성이 크다.
Su 등 (2022)은 FCV와 유사한 외피를 갖지 않은 RNA 바이러스인 Enterovirus D68 (EV68)에 대해 tanshinone IIA가 ataxia telangiectasia mutated (ATM) 신호전달 경로를 차단함으로써 DNA 손상 반응을 억제하고, 바이러스 복제 및 단백질 합성을 저해한다는 결과를 제시하였다. 해당 연구에서 tanshinone IIA는 phosphorylated histone H2A variant X (γ-H2AX) 및 viral protein 1 (VP1) 발현 감소, 바이러스 RNA 수준 76% 감소, TCID50 값 22.6 배 감소하였다는 등의 결과는 본 연구에서 관찰된 SM-E의 post-treatment 조건에서의 우수한 억제 효과와 SM-E에 포함된 tanshinone 계열 화합물의 핵심적 역할의 근거가 된다고 하겠다.
또한, SM-E에 함께 존재하는 수용성 phenolic 계열 화합물 역시 항바이러스 활성에 복합적으로 기여할 수 있는 기전을 가지고 있다. Salvianolic acid A와 B는 MAPK, NF-κB, Janus kinase/signal transducer and activator of transcription (JAK/STAT), toll-like receptor 4 (TLR4) 등 다양한 경로를 통해 염증성 사이토카인 생성을 억제하고 항산화 반응을 유도하여 세포를 보호하는 것으로 알려져 있으며 (Qian et al., 2019; Wei et al., 2023), 특히 salvianolic acid B는 internal ribosome entry site (IRES) 활성을 저해함으로써 바이러스 RNA의 번역을 억제하는 작용 (Kim et al., 2019)을 한다고 보고된 바, 이는 SM-E가 post-infection 조건에서도 항바이러스 활성을 보인 결과와 부합된다고 할 수 있다. 또한 rosmarinic acid 역시 enterovirus 71 (EV71)의 IRES 활성과 RNA 합성을 차단하여 바이러스 복제를 저해하는 효과를 보인다고 보고된 바 있다 (Chung et al., 2015).
본 연구에서 도출한 결과 및 이러한 이전 연구를 종합하여 볼 때, SM-E의 항바이러스 활성은 (1) 바이러스 입자의 세포 부착 및 침투 저해, (2) p38 MAPK 및 NF-κB 경로를 중심으로 한 염증 및 바이러스 복제 관련 신호전달 억제, (3) IRES 활성 차단을 통한 바이러스 단백질 합성 저해 등 복합적 작용 기전에 의한 것으로 판단되며 SM-E에 높은 수준으로 포함된 tanshinone 계열 화합물의 SM-E의 항바이러스 활성에 핵심적 기여할 것으로 예측된다.
향후, 단삼 유래 유효성분의 작용점을 명확히 규명하기 위해서는 SM-E 내 개별 성분 (tanshinone IIA, salvianolic acids 등)에 대한 분획 및 항바이러스 활성을 비교함으로써, 항바이러스 활성에 미치는 주요한 성분을 규명할 필요가 있으며, p38 MAPK, NF-κB, IRES 등 주요 신호전달 경로에 대한 phospho-protein 수준 분석 및 qRT-PCR 기반 유전자 발현 분석을 통해 세포 내 기전을 규명하고 노로바이러스 surrogate 확대 적용을 위하여 FCV 외에도 MNV-1, Tulane virus 등 다른 surrogate virus를 활용한 교차 검증 연구와 함께 in vivo 수준에서의 유효성 검증, 조직 독성에 대한 평가 및 다양한 RNA 바이러스에 대한 유효성을 비교·평가하는 후속 연구를 통해 실용화 가능성을 높일 수 있을 것으로 생각된다.
결론적으로, SM-E은 FCV에 대해 일관되고 강력한 항바이러스 활성을 나타냈으며, 이는 노로바이러스에 의한 급성 위장염을 예방하고 치료하는 천연물 기반 항바이러스제의 유망한 개발 후보로서의 가능성을 제시한다고 하겠다. 향후 용매 선택, 성분 최적화, 작용기전 규명 등을 통해 단삼 추출물의 응용 범위는 향후 더욱 확대될 수 있을 것으로 기대된다.
References
-
Abd-Elazem IS, Chen HS, Bates RB and Huang RCC. (2002). Isolation of two highly potent and non-toxic inhibitors of human immunodeficiency virus type 1(HIV-1) integrase from Salvia miltiorrhiza. Antiviral Research. 55:91-106.
[https://doi.org/10.1016/S0166-3542(02)00011-6]

-
Ahmed SM, Hall AJ, Robinson AE, Verhoef L, Premkumar P, Parashar UD, Koopmans M and Lopman BA. (2014). Global prevalence of norovirus in cases of gastroenteritis: A systematic review and meta-analysis. The Lancet Infectious Diseases. 14:725-730.
[https://doi.org/10.1016/S1473-3099(14)70767-4]

-
Akaberi M, Iranshahi M and Mehri S. (2016). Molecular signaling pathways behind the biological effects of Salvia species diterpenes in neuropharmacology and cardiology. Phytotherapy Research. 30:878-893.
[https://doi.org/10.1002/ptr.5599]

-
Bellamy K. (1995). A review of the test methods used to establish virucidal activity. Journal of Hospital Infection. 30:389-396.
[https://doi.org/10.1016/0195-6701(95)90043-8]

-
Bi WT, Tian ML and Row KH. (2011). Extraction and concentration of tanshinones in Salvia miltiorrhiza bunge by task-specific non-ionic surfactant assistance. Food Chemistry. 126:1985-1990.
[https://doi.org/10.1016/j.foodchem.2010.12.059]

-
Biswas D, Nandy S, Mukherjee A, Pandey DK and Dey A. (2020). Moringa oleifera Lam. and derived phytochemicals as promising antiviral agents: A review. South African Journal of Botany. 129:272-282.
[https://doi.org/10.1016/j.sajb.2019.07.049]

-
Chander Y, Kumar R, Khandelwal N, Singh N, Shringi BN, Barua S and Kumar N. (2021). Role of p38 mitogen‐activated protein kinase signalling in virus replication and potential for developing broad spectrum antiviral drugs. Reviews in Medical Virology. 31:1-16. https://onlinelibrary.wiley.com/doi/full/10.1002/rmv.2217, (cited by 2024 Jan. 11).
[https://doi.org/10.1002/rmv.2217]

-
Chen X, Chen K, Zhang Z, Wei P, Zhang L, Xu Y, Lun Q, Ma Y, Wu F, Zhang Y, Wang Y, Zhou Y, Zhan J and Xu W. (2022). Investigating derivatives of tanshinone IIA sulfonate sodium and chloroxine for their inhibition activities against the SARS-CoV-2 papain-like protease. ACS Omega. 7:48416-48426.
[https://doi.org/10.1021/acsomega.2c06675]

-
Chen X, Deng Y, Xue Y and Liang J. (2012). Screening of bioactive compounds in Radix Salviae Miltiorrhizae with liposomes and cell membranes using HPLC. Journal of Pharmaceutical and Biomedical Analysis. 70:194-201.
[https://doi.org/10.1016/j.jpba.2012.06.030]

-
Chung YC, Hsieh FC, Lin YJ, Wu TY, Lin CW, Lin CT, Tang NY and Jinn TR. (2015). Magnesium lithospermate B and rosmarinic acid, two compounds present in Salvia miltiorrhiza, have potent antiviral activity against enterovirus 71 infections. European Journal of Pharmacology. 755:127-133.
[https://doi.org/10.1016/j.ejphar.2015.02.046]

-
Cromeans T, Park GW, Costantini V, Lee D, Wang Q, Farkas T, Lee A and Vinjé J. (2014). Comprehensive comparison of cultivable norovirus surrogates in response to different inactivation and disinfection treatments. Applied and Environmental Microbiology. 80:5743-5751.
[https://doi.org/10.1128/AEM.01532-14]

-
Cui S, Chen S, Wu Q, Chen T and Li S. (2020). A network pharmacology approach to investigate the anti-inflammatory mechanism of effective ingredients from Salvia miltiorrhiza. International Immunopharmacology. 81:106040. https://www.sciencedirect.com/science/article/abs/pii/S1567576919320958, (cited by 2024 Jan. 11).
[https://doi.org/10.1016/j.intimp.2019.106040]

-
Duizer E, Schwab KJ, Neill FH, Atmar RL, Koopman MPG and Estes MK. (2004). Laboratory efforts to cultivate noroviruses. Journal of General Virology. 85:79-87.
[https://doi.org/10.1099/vir.0.19478-0]

-
Elizaquível P, Azizkhani M, Aznar R and Sánchez G. (2013). The effect of essential oils on norovirus surrogates Food Control. 32:275-278.
[https://doi.org/10.1016/j.foodcont.2012.11.031]

-
Gabbianelli R, Shahar E, De Simone G, Rucci C, Bordoni L, Feliziani G, Zho F, Ferrati M, Maggi F, Spinozzi E and Mahajna J. (2023). Plant-derived epi-nutraceuticals as potential broad-spectrum anti-viral agents. Nutrients. 15:4719. https://www.mdpi.com/2072-6643/15/22/4719, (cited by 2024 Jan. 11).
[https://doi.org/10.3390/nu15224719]

-
Gallo M, Ferracane R, Graziani G, Ritieni A and Fogliano V. (2010). Microwave assisted extraction of phenolic compounds from four different spices. Molecules. 15:6365-6374.
[https://doi.org/10.3390/molecules15096365]

-
Gao H, Huang L, Ding F, Yang K, Feng Y, Tang H, Xu Q, Feng J and Yang S. (2018). Simultaneous purification of dihydrotanshinone, tanshinone I, cryptotanshinone, and tanshinone IIA from Salvia miltiorrhiza and their anti-inflammatory activities investigation. Scientific Reports. 8:8460. https://www.nature.com/articles/s41598-018-26828-0, (cited by 2024 Jan. 11).
[https://doi.org/10.1038/s41598-018-26828-0]

-
Gilling D, Kitajima M, Torrey J and Bright K. (2014). Antiviral efficacy and mechanisms of action of oregano essential oil and its primary component carvacrol against murine norovirus. Journal of Applied Microbiology. 116:1149-1163.
[https://doi.org/10.1111/jam.12453]

-
Gong X, Huang S, Pan J and Qu H. (2017). Modeling of degradation kinetics of Salvianolic acid B at different temperatures and pH values. Chinese Journal of Chemical Engineering. 25:68-73.
[https://doi.org/10.1016/j.cjche.2016.06.005]

-
He X, Yang F, Wu Y, Lu J, Gao X, Zhu X, Yang J, Liu S, Xiao G and Pan X. (2023). Identification of tanshinone I as cap-dependent endonuclease inhibitor with broad-spectrum antiviral effect. Journal of Virology. 97:e00796-23. https://journals.asm.org/doi/full/10.1128/jvi.00796-23, (cited by 2024 Jan. 11).
[https://doi.org/10.1128/jvi.00796-23]

-
Hierholzer JC and Killington RA. (1996). Virus isolation and quantitation. In Mahy BWJ and Kangro HO. (eds.). Virology methods manual. Academy Press. San Diego. CA, USA. p.35-37.
[https://doi.org/10.1016/B978-012465330-6/50003-8]

-
Hsieh CF, Jheng JR, Lin GH, Chen YL, Ho JY, Liu CJ, Hsu KY, Chen YS, Chan YF, Yu HM, Hsieh PW, Chern JH and Horang JT. (2020). Rosmarinic acid exhibits broad anti-enterovirus A71 activity by inhibiting the interaction between the five-fold axis of capsid VP1 and cognate sulfated receptors. Emerging Microbes and Infections. 9:1194-1205.
[https://doi.org/10.1080/22221751.2020.1767512]

-
Jang SI, Kim HJ, Kim YJ, Jeong SI and You YO. (2006). Tanshinone IIA inhibits LPS-induced NF-κB activation in RAW 264.7 cells: Possible involvement of the NIK–IKK, ERK1/2, p38 and JNK pathways. European Journal of Pharmacology. 542:1-7.
[https://doi.org/10.1016/j.ejphar.2006.04.044]

-
Jiang Y, David B, Tu PF and Barbin Y. (2010). Recent analytical approaches in quality control of traditional Chinese medicines. Analytica Chimica Acta. 657:9-18.
[https://doi.org/10.1016/j.aca.2009.10.024]

-
Kamimoto M, Nakai Y, Tsuji T, Shimamoto T and Shimamoto T. (2014). Antiviral effects of persimmon extract on human norovirus and its surrogate, bacteriophage MS2. Journal of Food Science. 79:M941-M946.
[https://doi.org/10.1111/1750-3841.12462]

-
Kim SH, Lee J, Jung YL, Hong A, Nam SJ and Lim BK. (2019). Salvianolic acid B inhibits hand-foot-mouth disease enterovirus 71 replication through enhancement of AKT signaling pathway. Journal of Microbiology and Biotechnology. 30:38-43.
[https://doi.org/10.4014/jmb.1907.07079]

-
Koehn FE and Carter GT. (2005). The evolving role of natural products in drug discovery. Nature Reviews Drug Discovery. 4:206-220.
[https://doi.org/10.1038/nrd1657]

-
Lee DS, Lee SH, Noh JG and Hong SD. (1999). Antibacterial activities of cryptotanshinone and dihydrotanshinone I from a medicinal herb, Salvia miltiorrhiza Bunge. Bioscience, Biotechnology, and Biochemistry. 63:2236-2239.
[https://doi.org/10.1271/bbb.63.2236]

-
Lee ES, Kim MS, Weeratunga P, Lee HC, Chathuranga K, Ma JY, Kim HI and Lee JS. (2018). The anti-Influenza effect of a water soluble herbal extract from Salvia miltiorrhiza(Danshen) in vivo. Journal of Biomedical and Translational Research. 19:21-25.
[https://doi.org/10.12729/jbtr.2018.19.1.021]

-
Lee JH, Bae SY, Oh M, Kim KH and Chung MS. (2014). Antiviral effects of mulberry(Morus alba) juice and its fractions on foodborne viral surrogates. Foodborne Pathogens and Disease. 11:224-229.
[https://doi.org/10.1089/fpd.2013.1633]

-
Li LN. (1998). Biologically active components from traditional Chinese medicines. Pure and Applied Chemistry. 70:547-554.
[https://doi.org/10.1351/pac199870030547]

-
Li MH, Peng Y and Xiao PG. (2010). Distribution of tanshinones in the genus Salvia(family Lamiaceae) from China and its systematic significance. Journal of Systematics and Evolution. 48:118-122.
[https://doi.org/10.1111/j.1759-6831.2010.00070.x]

-
Liao N, Sun L, Wang D, Chen L, Wang J, Qi X, Zhang H, Tang M, Wu G, Chn J and Zhang R. (2021). Antiviral properties of propolis ethanol extract against norovirus and its application in fresh juices. LWT. 152:112169. https://www.sciencedirect.com/science/article/abs/pii/S0023643821013220, (cited by 2024 Jan. 11).
[https://doi.org/10.1016/j.lwt.2021.112169]

-
Lindesmith LC, Donaldson E, Leon J, Moe CL, Frelinger JA, Johnston RE, Weber DJ and Baric RS. (2010). Heterotypic humoral and cellular immune responses following norwalk virus infection. Journal of Virology. 84:1800-1815.
[https://doi.org/10.1128/JVI.02179-09]

-
Liu F, Wang D, Liu W, Wang X, Bai AY and Huang LQ. (2013). Ionic liquid-based ultrahigh pressure extraction of five tanshinones from Salvia miltiorrhiza bunge. Separation and Purification Technology. 110:86-92.
[https://doi.org/10.1016/j.seppur.2013.03.012]

-
Liu GT, Zhang TM, Wang BE and Wang YW. (1992). Protective action of seven natural phenolic compounds against peroxidative damage to biomembranes. Biochemical Pharmacology. 43:147-152.
[https://doi.org/10.1016/0006-2952(92)90271-J]

-
Natoni A, Kass GEN, Carter MJ and Roberts LO. (2006). The mitochondrial pathway of apoptosis is triggered during feline calicivirus infection. Journal of General Virology. 87:357-364.
[https://doi.org/10.1099/vir.0.81399-0]

-
Oh EG, Kim KL, Shin SB, Son KT, Lee HJ, Kim TH, Kim YM, Cho EJ, Kim DK, Lee EW, Shin IS and Kim JH. (2013). Antiviral activity of green tea catechins against feline calicivirus as a surrogate for norovirus. Food Science and Biotechnology. 22:593-598.
[https://doi.org/10.1007/s10068-013-0119-4]

-
Oh M, Bae SY, Lee JH, Cho KJ, Kim KH and Chung MS. (2012). Antiviral effects of black raspberry(Rubus coreanus) juice on foodborne viral surrogates. Foodborne Pathogens and Disease. 9:915-921.
[https://doi.org/10.1089/fpd.2012.1174]

-
Ong E and Len S. (2004). Evaluation of pressurized liquid extraction and pressurized hot water extraction for tanshinone I and IIA in Salvia miltiorrhiza using LC and LC-ESI-MS. Journal of Chromatographic Science. 42:211-216.
[https://doi.org/10.1093/chromsci/42.4.211]

-
Pan X, Niu G and Liu H. (2002). Comparison of micro-waveassisted extraction and conventional extraction techniques for the extraction of tanshinones from Salvia miltiorrhiza bunge. Biochemical Engineering Journal. 12:71-77.
[https://doi.org/10.1016/S1369-703X(02)00039-6]

- Qian W, Wang Z, Xu T and Li D. (2019). Anti-apoptotic effects and mechanisms of salvianolic acid A on cardiomyocytes in ischemia-reperfusion injury. Histology and Histopathology. 34:223-231.
-
Rajasekaran D, Palombo EA, Yeo TC, Ley DLS, Tu CL, Malherbe F and Grollo F. (2013). Identification of traditional medicinal plant extracts with novel anti-influenza activity. PLosOne. 8:e79293. https://journals.plos.org/plosone/article?id=10.1371/journal.pone.0079293, (cited by 21 June 2025).
[https://doi.org/10.1371/journal.pone.0079293]

-
Robilotti E, Deresinski S and Pinsky BA. (2015). Norovirus. Clinical Microbiology Reviews. 28:134-164.
[https://doi.org/10.1128/CMR.00075-14]

-
Ryu SY, Oak MH and Kim KM. (1999). Inhibition of mast cell degranulation by tanshinones from the roots of Salvia miltiorrhiza. Planta Medica. 65:654-655.
[https://doi.org/10.1055/s-2006-960839]

-
Stals A, Baert L, Van Coillie E and Uyttendaele M. (2011). Evaluation of a norovirus detection methodology for soft red fruits. Food Microbiology. 28:52-58.
[https://doi.org/10.1016/j.fm.2010.08.004]

-
Steinmann J. (2004). Surrogate viruses for testing virucidal efficacy of chemical disinfectants. Journal of Hospital Infection. 56:49-54.
[https://doi.org/10.1016/j.jhin.2003.12.030]

-
Su Y, Wu T, Yu X, Huo W, Wang S, Huan C, Liu Y, Liu J, Cui M, Li X and Yu J. (2022). Inhibitory effect of tanshinone IIA, resveratrol and silibinin on enterovirus 68 production through inhibiting ATM and DNA-PK pathway. Phytomedicine. 99:153977. https://www.sciencedirect.com/science/article/pii/S0944711322000551, (cited by 2025 June 21).
[https://doi.org/10.1016/j.phymed.2022.153977]

-
Sun N, Li E, Wang Z, Zhao J, Wang S, He J, Bai Y and Li H. (2013). Sodium tanshinone IIA sulfonate inhibits porcine reproductive and respiratory syndrome virus via suppressing N gene expression and blocking virus-induced apoptosis. Antiviral Therapy. 19:89-95.
[https://doi.org/10.3851/IMP2694]

-
Tran TB, Pham TLG and Pham THV. (2021). Extraction of tanshinones rich extract of Danshen(Salvia Miltiorrhiza Bunge) root using adsorptive(non-ionic) macroporous resins. VNU Journal of Science: Medical and Pharmaceutical Sciences. 37:59-66.
[https://doi.org/10.25073/2588-1132/vnumps.4333]

-
Valipour M. (2023). Therapeutic prospects of naturally occurring p38 MAPK inhibitors tanshinone IIA and pinocembrin for the treatment of SARS-CoV-2-induced CNS complications. Phytotherapy Research. 37:3724-3743.
[https://doi.org/10.1002/ptr.7902]

-
Wang D, Zhang W, Wang T, Li N, Mu H, Zhang J and Duan J. (2015). Unveiling the mode of action of two antibacterial tanshinone derivatives. International Journal of Molecular Sciences. 16:17668-17681.
[https://doi.org/10.3390/ijms160817668]

-
Wang LH, Song YH, Cheng YY and Liu XR. (2008). Orthogonal array design for the optimization of supercritical fluid extraction of tanshinones from Danshen. Journal of Separation Science. 31:321-328.
[https://doi.org/10.1002/jssc.200700386]

-
Wei B, Sun C, Wan H, Shou Q, Han B, Sheng M, Li L and Kai G. (2023). Bioactive components and molecular mechanisms of Salvia miltiorrhiza Bunge in promoting blood circulation to remove blood stasis. Journal of Ethnopharmacology. 317:116697. https://www.sciencedirect.com/science/article/abs/pii/S0378874123005652, (cited by 2025 June 21).
[https://doi.org/10.1016/j.jep.2023.116697]

-
Winder N, Gohar S and Muthana M. (2022). Norovirus: An overview of virology and preventative measures. Viruses. 14:2811. https://www.mdpi.com/1999-4915/14/12/2811, (cited by 2025 Jan 21).
[https://doi.org/10.3390/v14122811]

-
Wobus CE, Karst SM, Thackray LB, Chang KO, Sosnovtsev SV, Belliot G, Krug A, Mackenzie JM, Green KY and Virgin IV HW. (2004). Replication of norovirus in cell culture reveals a tropism for dendritic cells and macrophages. PLoS Biology. 2:e432. https://journals.plos.org/plosbiology/article?id=10.1371/journal.pbio.0020432, (cited by 2024 Jan. 11).
[https://doi.org/10.1371/journal.pbio.0020432]

- World Health Organization(WHO). (2020). WHO Director-general’s opening remarks at the media briefing on COVID-19; 11 March 2020. World Health Organization. Geneva, Switzerland. https://www.who.int/director-general/speeches/detail/who-director-general-s-opening-remarks-at-the-media-briefing-on-covid-19---11-march-2020, (cited by 2024 Jan. 11).
- Wu BW, Pan TL, Leu YL, Chang YK, Tai PJ, Lin KH and Horng JT. (2007). Antiviral effects of Salvia miltiorrhiza (Danshen) against enterovirus 71. The American Journal of Chinese Medicine. 35:153-168.
-
Yang N, Zhang L, Tian D, Wang P, Men K, Ge Y and Zhang C. (2023). Tanshinone increases hemopexin expression in lung cells and macrophages to protect against cigarette smoke-induced COPD and enhance antiviral responses. Cell Cycle. 22:645-665.
[https://doi.org/10.1142/S0192415X07004709]

-
Zhou L, Zuo Z and Chow MSS. (2005). Danshen: An overview of its chemistry, pharmacology, pharmacokinetics, and clinical use. Journal of Clinical Pharmacology. 45:1345-1359.
[https://doi.org/10.1080/15384101.2022.2129933]

-
Zhou Y, Li W, Xu L and Chen L. (2011). In Salvia miltiorrhiza, phenolic acids possess protective properties against amyloid β-induced cytotoxicity, and tanshinones act as acetylcholinesterase inhibitors. Environmental Toxicology and Pharmacology. 31:443-452.
[https://doi.org/10.1177/0091270005282630]

-
Zhu T, Park HE and Row KH. (2013). Ultrasonic-assisted extraction of tanshinones from Korean red ginseng by using amino-modified monolithic cartridge. Asian Journal of Chemistry. 25:7765-7768.
[https://doi.org/10.1016/j.etap.2011.02.006]
