
국내 작약 품종을 저비용으로 식별하기 위한 InDel 마커 개발
This is an open access article distributed under the terms of the Creative Commons Attribution Non-Commercial License (http://creativecommons.org/licenses/by-nc/3.0/) which permits unrestricted non-commercial use, distribution, and reproduction in any medium, provided the original work is properly cited.
Abstract
The herbaceous peony (Paeonia lactiflora) is widely used as an ornamental and medicinal crop in Korea; however, morphology-based cultivar discrimination is unreliable, highlighting the need for low-cost markers to facilitate the rapid identification, maintenance, distribution, and quality control of cultivars.
Next-generation sequencing was performed for five Korean cultivars (Uiseong, Taebaek, Sagok, Daecheong, and Geopung). Putative insertion/deletion (InDel) sites, mostly ≥19 bp, were detected by comparative analysis using CLC Genomics Workbench software, and primers were designed for 22 loci. Of these, nine markers yielded clear amplicon length polymorphisms that were resolved using simple PCR–agarose gels. In total, 18 distinct three-marker combinations uniquely identified all five cultivars; for example, PLID1-5/PLID5-2/PLID8-2. Weak upper bands at some loci were confirmed as heteroduplexes by T7 endonuclease I and were excluded from scoring. The Fragment Analyzer profiles were fully concordant with the gel results.
These InDel markers enable reliable, low-cost, and gel-based identification of Korean herbaceous peony cultivars, and are applicable for variety protection, purity testing, and distribution authentication.
Keywords:
Paeonia lactiflora, InDel Marker, Gel Electrophoresis, Varieties Identification서 언
작약속 (Paeonia spp.)은 작약과 (Paeoniaceae)에 속하는 다년생 식물로 전 세계에 약 30종이 분포한다 (Stern, 1943). 꽃이 화려하여 오랜 기간 관상용으로 이용되어 왔고 (Michener and Adelman, 2017), 뿌리는 한약재 작약 (芍藥)으로 이용된다. 『대한민국약전』 (Korean Pharmacopoeia, KP, 2008)에서는 작약을 Paeonia lactiflora 또는 동속 근연 식물의 뿌리로 규정하며 한방에서는 진경 (鎭痙), 진통 (鎭痛) 등의 효능이 알려져 있고 사물탕, 십전대보탕 등에 처방된다 (Ministry of Food and Drug Safety, 2008; Choi, 2009).
작약 뿌리에는 paeoniflorin, albiflorin 등의 성분이 다량 함유되어 있으며 (Zhang et al., 2001; Tan et al., 2010) 항염증, 항산화, 항암, 항우울증 등 다양한 효능이 알려져 있다 (Takagi and Harada, 1969; He and Dai, 2011; Jin et al., 2016; Xiang et al., 2020; Zhang et al., 2022). 약리적 효능에 더해 건강기능식품 시장이 확대되면서 국내 작약 수요가 증가하여 2023년 기준 1,987톤을 생산하고 있다 (Ministry of Agriculture, Food and Rural Affairs, 2024).
전 세계적으로 작약 육종은 주로 관상용 품종 개발 위주로서 1,900년 이후 등록된 관상·절화용 신품종은 2,200종을 넘어섰으며 (Yang et al., 2020), 이 가운데 연분홍 겹꽃 ‘Sarah Bernhardt’가 가장 널리 보급되었다 (Kamenetsky and Dole, 2012). 약용 품종 개발은 상대적으로 더딘 편이지만, 최근 중국에서는 내습성, 내고온성을 지닌 ‘Hang Baishao’, ‘Zi Xin’ (Purple Heart) 등의 품종이 개발된 바 있다 (Zhang et al., 2017; Wang et al., 2022). 국내 약용 작약 육종연구 현황을 보면 1990년대 수집·선발되어 육성된 ‘의성’ (1993), ‘태백’ (1995), ‘사곡’ (1997), ‘거풍’ (2000), ‘미강’ (2001), ‘대청’ (2003), ‘다호’ (2006) 등의 다수성 계통이 순차적으로 직무육성 신품종 선정 심의회를 통과한 바 있다. 이들은 육성기간이 20년 이상 경과하였으며 품종 보호등록은 되지 않았으나 ‘의성’, ‘태백’, ‘사곡’, ‘거풍’, ‘대청’ 등 일부는 보급되어 현재까지 재배되고 있는 것으로 파악된다 (Rural Development Administration, 2008).
한편, 작약속 식물은 주로 곤충 매개에 의해 이루어지는 타가수정 (outcrossing)에 의존하여 종자번식 시 유전형이 쉽게 분리되며 (Zhou, 1999; Wang, 2019; Yang et al., 2020), 특히 작약 (P. lactiflora)은 한 꽃에 암·수 작용을 동시에 가진 양성화 (hermaphrodite) 형태지만 자가수분은 잘되지 않고 자가수분 되어도 자식약세 (inbreeding depression)가 심한 것으로 보고 되고 있다 (Gao, 2018). 따라서 지금까지 영양번식 방법으로 작약 품종을 개발하고 기본식물을 관리하였으며 보급 단계에서 균일성 유지를 위해서는 판별마커 개발이 필수적이다.
품종 혹은 자원을 구분하기 위한 수단으로 표현형질을 활용한 판별마커가 널리 사용된 바 있으며 비용이 저렴하고 절차가 간단하다는 이점이 있으나 환경 조건에 따른 변이가 크고 결과의 일관성이 낮다는 점에서 한계가 지적된다 (Xu, 2010). 특히 동일한 유전형도 환경 조건에 따라 상이한 표현형을 보일 수 있어 판별 정확도에 제한이 따른다 (Cooper et al., 2024). 이러한 한계를 보완하기 위한 분자마커 기반의 유전자형 분석은 정밀하고 신뢰성 높은 방법으로 품종 식별과 자원 균일성 확보를 가능하게 한다. 또한 신품종 개발 과정에서 유전 정보 없이 자원을 선발할 경우, 중복 자원의 불필요한 평가, 비효율적인 교배조합 설계, 선발 오류 등의 문제가 발생하여 전체적인 육종 효율성을 저하시킬 수 있다 (Fu, 2015).
작약속 식물의 배수성은 다양하나 작약의 경우 2배체 (2n=10)로 알려져 있다 (Hao et al., 2016; Iwatsubo, 2017; Chen et al., 2023). 작약은 고품질 참조 유전체의 공개가 제한적이므로 정확한 유전체 크기는 알 수 없으나 작약속 식물 중 하나인 모란 (P. suffruticosa)의 유전체 크기가 약 13–16 Gb로 추정되고 반복서열 비중이 80% 수준으로 보고된 바 있다 (Lv et al., 2020). 또한 다른 근연종인 P. ostii는 12.28 Gb로 추정되었고 (Yuan et al., 2022), P. ludlowii 유전체 역시 10.6 Gb 크기로 보고 되었다 (Xiao et al., 2023). 따라서 작약의 경우도 유전체의 크기가 크고 복잡하여 마커 개발에 불리할 것으로 예상되나, 일부 보고된 판별용 마커는 있다. SSR의 경우 Gilmore 등 (2013)은 Illumina 기반 21종, Ji 등 (2014)은 SSR 15종, Wu 등 (2014)은 EST-SSR 30종을 개발하여 P. lactiflora를 포함한 유전적 변이 구분에 활용하였다. 그러나 SSR은 반복서열 변이 및 프라이머 부위의 단일 염기변이 (single nucleotide variant)에 민감해 오판별 가능성이 있고, 분석에 고가 장비가 필요하다는 단점이 있다 (Huo et al., 2021). 엽록체 및 ITS 염기서열 기반 마커도 보고되었으나 (Zhu et al., 2015; Gao et al., 2020; Wu et al., 2021; Lee et al., 2022), 엽록체의 경우 모계 유전 특성에 국한되어 주로 종 간 구분에 이용되며 ITS 서열은 핵 유래이지만 리보솜 DNA 반복단위 간의 재조합이 제한되어 비교적 보존적이고 개체 내 변이가 적어 품종 간 식별력은 낮다 (Ganley and Kobayashi, 2007). 유일하게 Lim 등 (2013)은 판별마커를 활용하여 ‘의성’, ‘태백’, ‘사곡’, ‘대청’, ‘거풍’ 등을 포함하여 국내 작약 유전자원을 구분한 사례가 있으나 사용한 마커의 경우 RAPD (Random Amplified Polymorphic DNA)로서 실험이 간편하다는 장점에도 불구하고 PCR 조건에 민감하여 재현성이 낮다는 한계가 지적된다 (Penner et al., 1993; Kumari and Thakur, 2014).
InDel 마커는 유전체 전반에 균일하게 분포하며 삽입·결실에 따른 서열 길이 차이를 이용해 간단히 PCR과 아가로스 겔 전기영동만으로 유전형을 구분하므로 SSR 마커나 SNP 마커와 달리 PCR 조건에 대한 최적화 부담이 상대적으로 적고, 형광 표지나 고가의 검출 장비가 필요하지 않아 분석 비용이 낮고 실험 효율이 높다 (Pacurar et al., 2012; Moghaddam et al., 2014; Song et al., 2015). 벼, 순무 등 여러 작물에서 품종 판별과 유연관계 분석에 성공적으로 적용된 바 있으며 (Hayashi et al., 2006; Liu et al., 2013), SSR 대비 분리도가 높고 분석 오류가 적다.
다만, 핵 InDel 마커를 이형접합 (heterozygous) 작물이나 F1 개체에 적용할 경우에는 전기영동할 때 PCR 산물의 크기가 다른 대립유전자가 변성 및 재결합되는 과정에서 비상동 부위가 결합해 이형이중가닥 (heteroduplex) 밴드가 형성될 수 있어 결과 판독 시 주의는 필요하다 (Constable and Symons, 2004; Mackay et al., 2008; Devey et al., 2009).
본 연구에서는 기본식물이 유지되고 현장에 보급 되어진 ‘의성’, ‘태백’, ‘사곡’, ‘대청’, ‘거풍’을 저비용으로 신속하게 식별할 수 있는 InDel 마커를 개발하고자 하였다. NGS를 통해 각 샘플에 대한 DNA 정보를 확보하여 InDel 마커를 개발하였고 PCR과 genotyping을 통해 식별 여부를 검증하였다.
재료 및 방법
1. 시험 재료 및 genomic DNA 추출
2021년에 경상북도농업기술원 봉화약용작물연구소 (36.9009°N, 128.8087°E)에서 기본식물로 분양받은 의성 (Euiseong), 사곡 (Sagok), 대청 (Daecheong), 거풍 (Geopoong)과 국립원예특작과학원 인삼특작부 특용작물육종과 시험포장 (36.9433°N, 127.7497°E)에서 보존하고 있는 태백 (Taebaek)의 어린잎 부위를 채취하여 동결건조 시킨 후 막자사발에 액체질소를 넣고 분말 상태가 될 때까지 분쇄하여 분말시료를 보관하였다. 보관된 시료는 GeneAll® Exgene™ Plant SV mini kit (GeneAll Biotechnology, Seoul, Korea)를 이용하여 제조사의 추출 프로토콜에 따라 gDNA를 분리 하였다. NanoDrop One (Thermo Scientific, Waltham, MA, USA)를 이용하여 농도와 순도를 측정하였다. 추출된 gDNA는 1.5% 아가로스 겔에서 100 V로 30 분간 전기영동을 수행하였으며, 시료는 4 ng/μL 농도의 DNA 5 μL (총 20 ng)와 1 μL의 loading dye를 혼합하여 주입하였다. 전기영동 후 밴드의 선명도와 smear 여부를 관찰하여 DNA의 품질을 확인하였다.
2. 차세대 염기서열분석
‘의성’, ‘태백’, ‘사곡’, ‘대청’, ‘거풍’ 등 5개 샘플을 대상으로 NGS (Next-Generation Sequencing) 분석을 수행하였다. DNA는 Qubit™ dsDNA BR Assay Kit (Q32850, Invitrogen, Eugene, OR, USA)를 사용하여 Qubit™ Fluorometer (Invitrogen, Eugene, OR, USA)로 측정하였다. 라이브러리 품질은 Agilent 2100 Bioanalyzer (Agilent Technologies, Santa Clara, CA, USA)로 평균 인서트 크기 550 ± 20 bp를 확인하였다. 이후, TruSeq™ Nano DNA Library Prep Kit (550 bp, Illumina Inc., San Diego, CA, USA)를 이용하여 시료별 라이브러리를 구축하였다. 염기서열분석은 DNALINK Inc. (Seoul, Korea)에 의뢰하여 Illumina NovaSeq 6000 platform (Illumina Inc., San Diego, CA, USA)에서 2 × 151 bp의 paired-end (PE) 방식으로 수행되었으며, 각 샘플당 약 15 Gb (Q30 ≥ 90%)의 염기서열분석 데이터를 확보하였다.
생성된 raw reads는 FastQC v0.11.9로 품질을 평가하였으며 Trimmomatic v0.39 (ILLUMINACLIP:adapters.fa:2:30:10, SLIDIN GWINDOW: 4:20,MINLEN:15)로 어댑터 제거 및 저품질 서열 (Phred < 20)과 길이 15 bp 미만 read를 필터링하였다. 전처리 후 평균 read 길이는 모든 샘플에서 151 bp로 유지되었다.
3. Contig 수준의 De novo 어셈블리 및 InDel 탐지
CLC Genomics Workbench v8.5.1 (QIAGEN, Aarhus, Denmark)을 활용하여 필터링된 reads를 de novo assembly 모듈을 이용하여 어셈블리하였다. 주요 파라미터는 Automatic word 및 bubble size 활성화, Scaffolding 옵션 해제로 설정하였다. 어셈블리 결과 contig N50, 평균 커버리지를 산출하고 시료별 평균 커버리지가 30× 미만인 contig는 제외하고 200 bp 이상의 contig를 작성하였다. 이후 각 자원의 contig에서 차이가 나는 부분을 비교하여 in silico 상 InDel이 확연한 차이 (19 bp 이상)가 보이는 유전자좌 22곳을 직접 확인하였다.
4. 프라이머 디자인
InDel 변이 부위에 대응하는 프라이머는 CLC Genomics Workbench v8.5.1 (QIAGEN, Aarhus, Denmark)의 ‘Design Primers’ 기능을 활용해 정방향과 역방향 모두 설계하였다. 우선, consensus 서열에서 변이가 관찰된 영역을 중심으로 증폭 대상 구간 (region to amplify)을 지정한 뒤 프라이머를 다음 조건에 따라 설정하였다. 프라이머 길이는 일반적으로 18–22 bp로 설정했으며 G+C 함량은 약 50% 수준으로 하였고, annealing 온도는 48–58℃ 범위 내로 하되, 프라이머 간 Tm 차이는 5℃를 넘지 않도록 하였다.
PCR 산물 크기 (amplicon length)는 100–400 bp 범위로 하였고 분석 효율을 고려하여 500 bp를 초과하지 않도록 하였다. 프라이머 설계 결과는 fragment length를 포함하여 표 형식으로 정리하고 같은 InDel 위치에 대해 여러 프라이머 조합이 추천되면 위치와 길이가 상이하도록 배치하였다. 또한 서열 내에서 ‘N’ 염기가 포함될 경우, 특히 3′ 말단에 존재하면 증폭 오류 가능성이 높아 가급적 제외하였다.
동일한 contig 상에 복수의 InDel 변이가 존재할 경우에는 서로 간의 거리와 중복 여부를 고려하여 대표 부위를 우선 선정하거나, 개별 프라이머 세트를 각각 설계하였다. 한편, 프라이머 내에 InDel 또는 SNP 변이가 포함된 경우에는 해당 위치가 3′말단이 아닌 경우에 한하여 허용하였다.
5. PCR 분석 및 겔 전기영동
선정된 InDel 좌위의 실제 변이 존재 여부와 프라이머의 증폭 특이성을 검증하기 위해, PCR 증폭은 C1000 Touch Thermal Cycler (Bio-Rad, Hercules, CA, USA)를 이용하여 수행하였다. 반응 혼합물은 총 20 μL로 조제하였으며, 구성은 다음과 같다: 20 ng/μL 농도의 주형 DNA 2 μL, Exel TB 2X Taq Premix with dye (Inclone™ Exel, Inclonebiotech Co., Korea) 10 μL, 정방향 및 역방향 프라이머 (각각 5 μM) 각 2 μL, 그리고 삼증류수로 부피를 보정하였다. PCR 조건은 95℃에서 5분간의 열변성 (pre-denaturation)을 시작으로, 95℃에서 30초, 52℃에서 40초, 72℃에서 30초의 조건으로 38 사이클을 반복하였다. 최종적으로는 72℃에서 5분간 최종 신장 (final extension)을 진행하였으며, 증폭된 PCR 산물은 변성 방지를 위해 −20℃에 보관하였다.
PCR 산물은 3% 아가로스 겔에 로딩되었으며, DNA 시각화를 위해 Safe gel stain (clonebiotech Co., Korea)을 첨가하였다. 겔은 1 × TAE 완충용액에 침지된 상태에서 135 V의 전압으로 20분간 전기영동을 수행하였다. 밴드 크기 비교를 위해 1 kb ladder plus (Dongshengbio Co., Guangdong, China)를 함께 주입하였으며, 밴드는 Bio-Print Gel Documentation System (Vilber, Collégien, France)를 이용하여 시각화 및 확인하였다.
6. T7 endonuclease I (T7E1) 분석
작약은 자가불화합성으로 인해 높은 이형접합성 (heterozygosity)을 가진 교잡성 식물이며 (Yang et al., 2020), PCR 산물을 아가로스 겔 전기영동한 결과, 일부 마커에서 3개의 밴드가 관찰되었다. 이 중 이동 속도가 느린 상위 밴드는 heteroduplex일 것이라고 판단하였다. heteroduplex는 mismatch 염기쌍을 포함하므로, 이를 검증하기 위해 mismatch 특이적 절단 효소인 T7 endonuclease I (T7E1)을 이용하여 절단 반응을 수행하였다.
PCR 산물은 95℃에서 5분간 변성 후 서서히 냉각시켜 heteroduplex를 형성한 뒤, 두 그룹으로 나누어 0.1 U의 T7E1 (New England Biolabs Inc., Ipswich, MA, USA)을 처리한 실험군과 무처리 대조군으로 설정하였다. 반응은 27℃에서 12시간 반 응시킨 후 2% 아가로스 겔 전기영동으로 분리하였다. 절단이 발생한 마커는 이형접합 또는 염기 불일치에 따른 heteroduplex 구조의 존재를 의미하므로, 해당 마커의 분석에서는 절단된 상위 밴드를 제외한 나머지 밴드를 대상으로 스코어링 (scoring)을 수행하였다.
7. Fragment analyzer 분석
개발된 InDel 마커의 정확한 peak를 확인하기 위해, 5개 샘플에 적용하여 PCR을 수행하였으며, 증폭산물은 Fragment Analyzer™ 시스템 (Advanced Analytical Technologies, Ames, IA, USA)을 이용하여 분석하였다. 분석은 제조사의 지침에 따라 수행되었으며, PCR 산물은 TE buffer 및 분석용 시약 (dsDNA 930 Inlet Buffer, dsDNA 905 Gel, Capillary Conditioning Solution, intercalating dye, size marker 등)과 함께 혼합한 후 96-well plate에 로딩하여 전기영동을 진행하였다. DNA 단편은 35–400 bp 범위의 DNA ladder를 기준으로 자동 분석되었으며, 밴드 사이즈 측정과 다형성 검출은 PROSize™ 데이터 분석 소프트웨어를 통해 수행하였다.
결과 및 고찰
1. 염기서열 데이터 품질 평가
InDel 마커 개발을 위한 염기서열분석은 ‘의성’, ‘태백’, ‘사곡’, ‘대청’, ‘거풍’ 각각에 대해 고품질 PE reads를 생성하였으며, 각 자원에 대해 샘플당 평균 1억 개의 read와 약 15.3 Gb의 염기서열분석 데이터 (raw data)가 확보되었다. FastQC v0.11.9로 수행한 품질 분석 결과, Q30 이상 비율은 최소 88.99%, 평균 Phred 품질 점수는 35.14–35.32 범위로 나타나, 전체적으로 높은 품질의 염기서열분석 데이터를 확보하였음을 확인하였다 (Table 1).
2. 다형성 InDel 탐색
‘의성’, ‘태백’, ‘사곡’, ‘대청’, ‘거풍’ 등 5개 샘플의 염기서열 분석 결과를 정렬한 후, CLC Genomics Workbench를 활용하여 InDel 변이 부위를 시각적으로 비교하였다 (Fig. 1 and Fig. 2). 이 과정에서 5개 샘플의 contig 서열을 상호 비교 (pairwise alignment)하여, 동일 위치에 대응되는 InDel 부위 중 최소 하나 이상의 자원에서 차이를 보이는 19 bp 이상의 다형성 영역을 선별하였으며 총 22개의 후보 좌위에 대해 프라이머를 설계하였다.
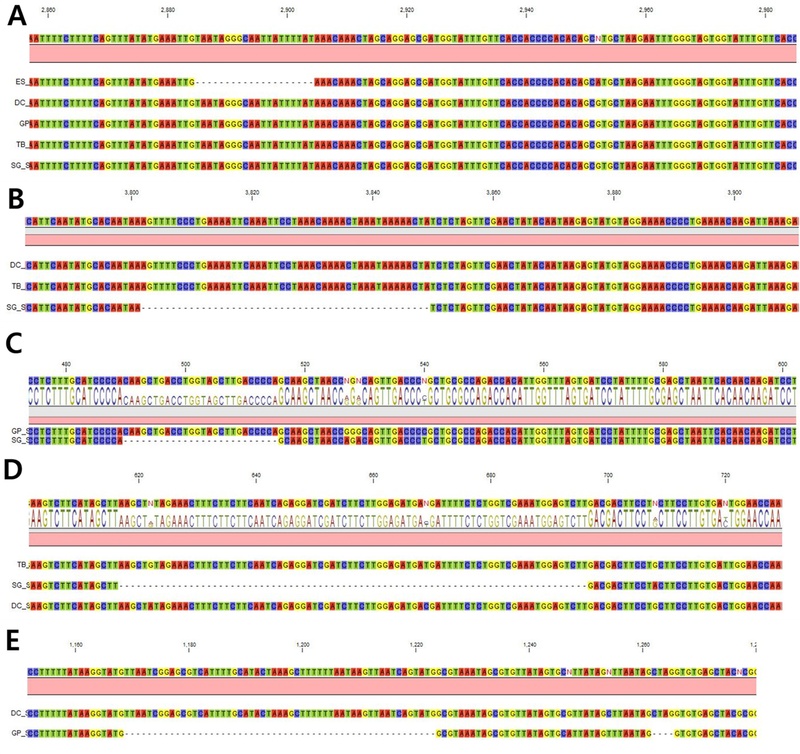
Multiple sequence alignment showing the InDel loci of the developed markers.(A) PLID1-1, (B) PLID2-2, (C) PLID5-2, (D) PLID8-2, and (E) PLID11-2. Each row represents the sequence of a different variety: Euiseong (ES), Daecheong (DC), Geopoong (GP), Taebaek (TB), and Sagok (SG). Colored boxes indicate individual nucleotides (A, T, G, and C), while gaps (dashes) represent insertion/deletion polymorphisms among varieties.
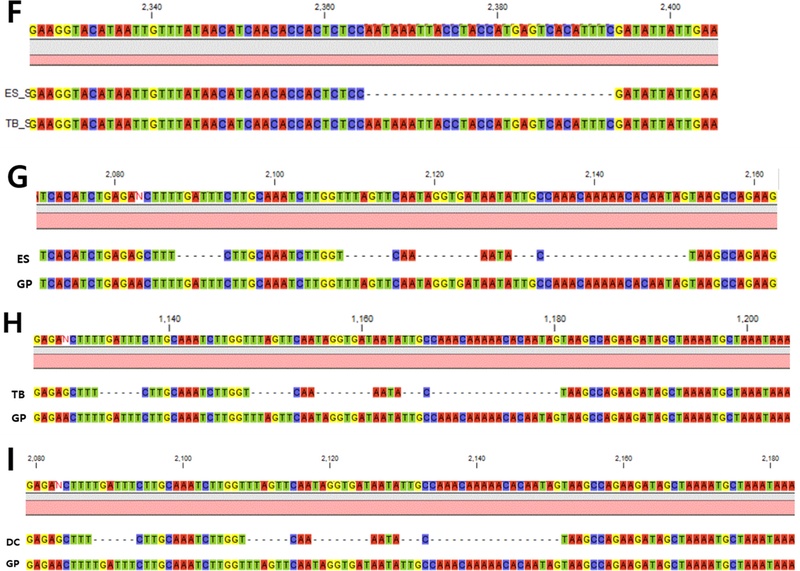
Multiple sequence alignment showing the InDel loci of the developed markers.(F) PLID15-2, (G) PLID16-2, (H) PLID17-1, and (I) PLID18-2. Sequence alignment was visualized as described in Fig. 1, where colored boxes represent nucleotides (A, T, G, C) and gaps (dashes) indicate insertion/deletion polymorphisms among five P. lactiflora varieties. Highlighted regions denote the InDel sites used for primer design.
설계된 프라이머는 해당 5개 샘플에 적용하여 PCR 증폭을 진행하였고, 그 결과 자원 간 유전형을 뚜렷하게 구분할 수 있었던 9종의 프라이머 조합을 최종적으로 선발하였다 (Table 2).
3. 전기영동 및 판별마커 선발
전기영동 결과를 바탕으로 분석한 결과, 22개 InDel 마커 후보 가운데 9개 마커에서 ‘의성’, ‘태백’, ‘사곡’, ‘대청’, ‘거풍’ 등 5개 샘플이 서로 명확히 구분되는 밴드 패턴을 보였으며, 이를 통해 시각적으로도 판별이 용이 하였다 (Fig. 3). 이들 마커의 밴드 패턴은 NGS 기반으로 예측된 InDel 다형성과 일치하는 경향을 보였으며, 주요 다형 구간에서 예상된 크기 차이와 일관된 결과를 나타냈다. 특히 마커별 밴드 유형이 뚜렷하게 구분되어, 이를 바코드 형태로 Table 3에 정리하였다. 추가 분석을 통해, 9개 마커 중 PLID1-5, PLID5-2, PLID8-2의 세 조합만으로도 해당 5개 샘플을 모두 구별할 수 있음을 확인하였다. 이처럼 최소 조합으로 자원 식별이 가능한 마커 세트는 총 18가지 조합이 도출되었으며 (Table 4), 이는 본 연구에서 선발된 InDel 마커들이 작약 품종 식별 도구로서의 실용적 가치를 지님을 뒷받침한다. 한편, 나머지 후보 마커들은 밴드 크기나 패턴이 자원 간 유사하거나 구분이 모호하여, 품종 간 판별을 위한 마커로서의 활용도는 제한적인 것으로 판단되었다.
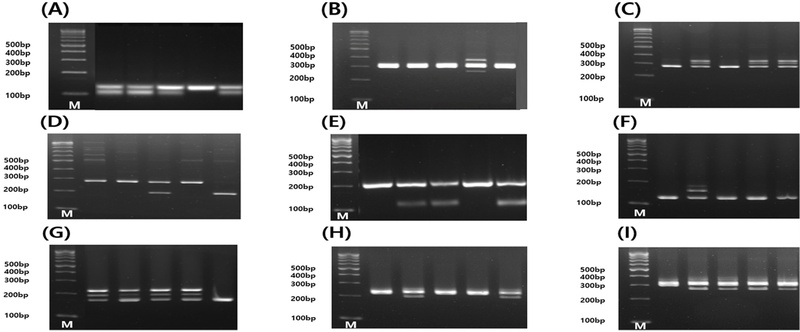
Results of electrophoresis performed on five herbaceous peony varieties using 9 InDel markers.Panels represent individual markers: (A) PLID1-5, (B) PLID2-2, (C) PLID5-2, (D) PLID8-2, (E) PLID11-2, (F) PLID15-2, (G) PLID16-2, (H) PLID17-1 and (I) PLID18-2. Lanes correspond, from left to right, to ‘Euiseong’, ‘Taebaek’, ‘Sagok’, ‘Daecheong’, and ‘Geopoong’. Lane M: 1kb DNA ladder, showing bands at 100, 200, 300, 400, and 500 bp. Distinct banding patterns indicate polymorphisms detected among cultivars for each marker.

Barcode representation of polymorphisms revealed by 9 InDel markers in five herbaceous peony varieties.
4. T7E1 분석 및 Fragment analyzer를 이용한 검증
PLID2-2, PLID5-2, PLID15-2, PLID16-2, PLID17-1, PLID18-2 등 일부 마커에서는 예상된 대립유전자 밴드 외에도 상위 위치에 약한 추가 밴드가 공통적으로 관찰되었으며, 이는 이형접합체에서 증폭된 서로 다른 단편이 재결합하여 형성된 heteroduplex일 가능성이 높다고 판단하였다. 이러한 해석을 뒷받침하기 위해 PLID16-2 마커에서 heteroduplex로 추정되는 밴드가 나타난 ‘사곡’ 샘플을 대상으로 T7E1 절단 반응을 수행한 결과, T7E1 처리한 샘플의 상위 밴드가 소실되었음을 확인하였는데 이는 이형접합체에서 발생한 염기 불일치 이중가닥 구조가 T7E1에 의해 절단되었음을 뜻한다 (Constable and Symons, 2004; Mackay et al., 2008). 이러한 결과는 작약이 이형접합성이 높다고 알려진 연구 결과와도 일치하며 (Yang et al., 2020), 상위 밴드가 PCR 산물에서 heteroduplex임을 고려하는 것이 유전형 판별의 정확도 향상에 필요하다. 본 연구에서도 heteroduplex에 해당되는 최상위 밴드는 분석 대상에서 제외하고 스코어링을 진행하였다.
동일한 PCR 산물을 Fragment Analyzer™로 정량 분석한 결과, 아가로스 겔 전기영동과 일치하는 단편 크기 및 패턴이 확인되어 결과의 신뢰성이 검증되었다 (Table 5).

Barcode representation of polymorphisms revealed by 9 InDel markers in five herbaceous peony varieties.
본 연구는 국내 작약 (P. lactiflora) 5개 샘플을 대상으로 저비용·고효율 InDel 마커를 개발하고 검증하여, 최소 3개 마커 조합만으로도 신뢰도 있게 구분할 수 있음을 확인하였다. 이 접근은 SSR 기반의 보고된 분자마커 (Gilmore et al., 2013; Ji et al., 2014)와 비교할 때 아가로스 겔 전기영동만으로 현장 적용이 가능하다는 점에서 비용과 접근성 측면의 이점이 있다. 나아가, 본 연구에서 개발된 InDel 좌위 주변 서열을 이용해 프라이머를 삽입/결실 경계에 배치하면 존재/부재 판별만을 이용하는 dominant형 마커로 전환하는 것도 가능할 것으로 보인다. 특히 Tₐ 조건이 같은 3개 마커 조합으로 dominant-type Multiplex 프라이머 세트를 구성하면 검사 효율을 높이고, 상업화 또는 서비스 응용 가능성도 기대할 수 있다. 다만 이 접근은 단일좌위 특이성 확보, 프라이머 간 간섭 최소화, multiplex 검증 등의 제약 요인을 철저히 고려해야 한다. 한편 작약은 아직 고품질 참조 유전체의 공개가 제한적이며, 근연종인 모란 (P. suffruticosa)의 유전체 크기가 약 13–16 Gb로 추정되고 반복서열 비중이 80% 수준으로 보고된 바 있어 (Lv et al., 2020), 작약 역시 대형 유전체·높은 반복서열 함량을 가질 가능성이 높다. 이러한 유전체적 특성은 대규모 SNP 패널의 구축·검증과 표준화에 상대적으로 높은 비용과 시간이 요구될 수 있다 (Rasheed et al., 2017). 또한 SNP 마커는 풍부한 형질 정보와 높은 확장성을 제공하지만, KASP, TaqMan 등 전용 플랫폼이나 NGS 기반 장비 의존도가 커 소규모 현장 판별에서는 경제성이 낮다 (Thomson, 2014). 본 연구에서 제시한 InDel 마커는 길이 차 (≥ 약 19 bp)에 기초한 간단한 PCR–겔 판별로 이러한 한계를 보완하여 향후 작약의 신품종 보호, 기본식물 관리, 이형주 제거 등 유전자원 관리, 유통 단계에서의 진위 판별 등에 다양한 분야에서 활용될 수 있을 것으로 기대된다.
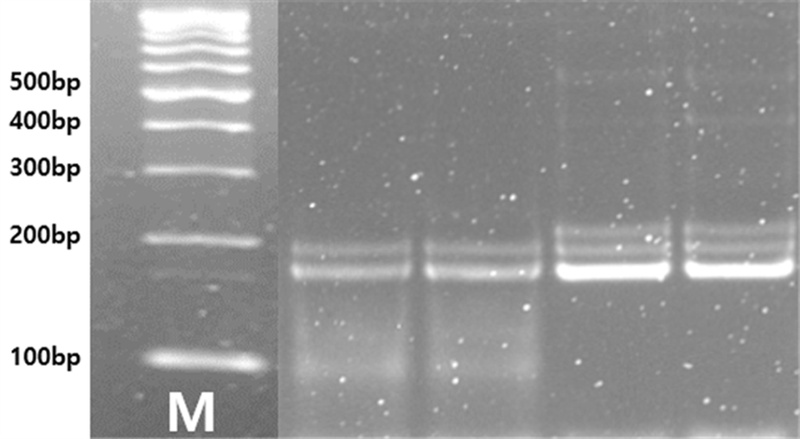
Heteroduplex confirmation at an InDel locus (PLID16-2) in ‘Sagok’.The right two lanes show PCR products without T7 endonuclease treatment, while the left two lanes show cleavage patterns after treatment with T7 endonuclease, which specifically digests heteroduplex DNA. Lane M: 1kb DNA ladder, showing bands at 100, 200, 300, 400, and 500 bp.
Acknowledgments
본 연구는 농촌진흥청 연구 사업(사업번호: PJ01732205)의 지원에 의해 이루어진 결과로 이에 감사드립니다.
References
-
Chen L, Wang Y, Guo Y, Liu Y, Zhang Z and Wang Z. (2023). Ploidy and karyotype analysis of different populations of Paeonia mairei, an endemic species to China. Cytologia. 88:55-59.
[https://doi.org/10.1508/cytologia.88.55]

- Choi SG. (2009). Herbal medicinal crop production: Special Part. Shinkwang Press, Seoul, Republic of Korea, p.186.
-
Constable FE and Symons RH. (2004). Genetic variability amongst isolates of Australian grapevine phytoplasmas. Australasian Plant Pathology. 33:115-119.
[https://doi.org/10.1071/AP03096]

-
Cooper M, van Eeuwijk FA, Chapman SC (2024). Genotype-by-environment interactions under water-limited conditions. In: Ribaut JM (ed.). Drought Adaptation in Cereals. Haworth Press. New York, USA. p.51-96.
[https://doi.org/10.1201/9781003578338-5]

-
Fu YB. (2015). Understanding crop genetic diversity under modern plant breeding. Theoretical and Applied Genetics. 128:2131-2142.
[https://doi.org/10.1007/s00122-015-2585-y]

-
Ganley ARD and Kobayashi T. (2007). Highly efficient concerted evolution in the ribosomal DNA repeats: Total rDNA repeat variation revealed by whole-genome shotgun sequence data. Genome Research 17:184-191.
[https://doi.org/10.1101/gr.5457707]

-
Gao C, Wang Q, Ying Z, Ge Y and Cheng R. (2020). Molecular structure and phylogenetic analysis of complete chloroplast genomes of medicinal species Paeonia lactiflora from Zhejiang Province. Mitochondrial DNA Part B. 5:1077-1078.
[https://doi.org/10.1080/23802359.2020.1721372]

-
Gao J, Fu Z, Dong X, Wang L, Yuan X, Zhang J, Wang H, Li Y, Feng N, Wang Y, Jiang H and Zhang HC. (2018). Studies on pollination characteristics and breeding system of Paeonia lactiflora Pall. Botanical Research 7: 536-542.
[https://doi.org/10.12677/BR.2018.75065]

-
Gilmore B, Bassil N, Nyberg A, Knaus B, Smith D, Barney DL and Hummer K. (2013). Microsatellite marker development in peony using next generation sequencing. Journal of the American Society for Horticultural Science. 138:64-74.
[https://doi.org/10.21273/JASHS.138.1.64]

-
Hao L, Sun H, Li H, Liu J, Zhang Q and Zhang J. (2016). Pollen morphology of herbaceous peonies with different ploidy levels and its taxonomic implications. Journal of the American Society for Horticultural Science 141:275-285
[https://doi.org/10.21273/JASHS.141.3.275]

-
Hayashi K, Yoshida H and Ashikawa I. (2006). Development of PCR-based allele-specific and InDel marker sets for nine rice blast resistance genes. Theoretical and Applied Genetics. 113:251-260.
[https://doi.org/10.1007/s00122-006-0290-6]

-
He DY and Dai SM. (2011). Anti-inflammatory and immunomodulatory effects of Paeonia lactiflora Pall., a traditional Chinese herbal medicine. Frontiers in Pharmacology. 2:10.
[https://doi.org/10.3389/fphar.2011.00010]

-
Huo Y, Zhao Y, Xu L, Yi H, Zhang Y, Jia X, Zhao H, Zhao J and Wang F. (2021). An integrated strategy for target SSR genotyping with toleration of nucleotide variations in the SSRs and flanking regions. BMC Bioinformatics. 22:429.
[https://doi.org/10.1186/s12859-021-04351-w]

- Iwatsubo Y, Teraoka A and Muraguchi K. (2017). Chromosome numbers of Paeonia cultivars(Paeoniaceae). Journal of Phytogeography and Taxonomy. 65:29-32.
-
Ji LJ, Teixeira da Silva JA, Zhang JJ, Tang ZJ and Yu XN. (2014). Development and application of 15 novel polymorphic microsatellite markers for sect. Paeonia(Paeonia L.). Biochemical Systematics and Ecology. 54:257-266.
[https://doi.org/10.1016/j.bse.2014.02.009]

-
Jin ZL, Gao N, Xu W, Xu P, Li SQ, Zheng YY and Xue M. (2016). Receptor and transporter binding and activity profiles of albiflorin extracted from Radix Paeoniae Alba. Scientific Reports. 6:33793.
[https://doi.org/10.1038/srep33793]

- Kamenetsky R and Dole JM. (2012). Herbaceous peony(Paeonia): Genetics, physiology and cut flower production. Floriculture and Ornamental Biotechnology. 6:62-77.
-
Kumari M and Thakur A. (2014). Randomly amplified polymorphic DNA - a brief review. American Journal of Animal and Veterinary Sciences. 9:6-13.
[https://doi.org/10.3844/ajavsp.2014.6.13]

-
Lee, MS, Jeong HJ, Park SH, Chung H, Jeong JT, Kim MK and Lee Y. (2022). Development of a chloroplast-based InDel marker that discriminates between Paeonia suffruticosa and P. lactiflora. Korean Journal of Medicinal Crop Science. 30:430-439.
[https://doi.org/10.7783/KJMCS.2022.30.6.430]

-
Lim MY, Jana S, Sivanesan I, Park HR, Hwang JH, Park YH and Jeong BR. (2013). Analysis of genetic variability using RAPD markers in Paeonia spp. grown in Korea. Korean Journal of Horticultural Science and Technology. 31:322-327
[https://doi.org/10.7235/hort.2013.12210]

-
Liu B, Wang Y, Zhai W, Deng J, Wang H, Cui Y, Cheng F, Wang X and Wu J. (2013). Development of InDel markers for Brassica rapa based on whole-genome re-sequencing. Theoretical and Applied Genetics. 126:231-239.
[https://doi.org/10.1007/s00122-012-1976-6]

-
Lv S, Cheng S, Wang Z, Li S, Jin X, Lan L, Yang B, Yu K, Ni X, Li N, Hou X, Huang G, Wang J, Dong Y, Wang E, Huang J, Zhang G and Zhang C. (2020). Draft genome of the famous ornamental plant Paeonia suffruticosa. Ecology and Evolution. 10:4518-4530.
[https://doi.org/10.1002/ece3.5965]

-
Mackay JF, Wright CD, Bonfiglioli RG. (2008). A new approach to varietal identification in plants by microsatellite high resolution melting analysis: Application to the verification of grapevine and olive cultivars. Plant Methods. 4:8.
[https://doi.org/10.1186/1746-4811-4-8]

- Michener DC and Adelman CA (2017). Peony: The best varieties for your garden. Timber Press.
- Ministry of Agriculture, Food and Rural Affairs(MAFRA). (2024). Final results of the 2023 census of agriculture, forestry and fisheries. Ministry of Agriculture, Food and Rural Affairs. Sejong, Republic of Korea. pp.107-110.
- Ministry of Food and Drug Safety(MFDS). (2008). The Korea pharmacopoeia. Ministry of Food and Drug Safety. Shinilbooks. Seoul, Republic of Korea. p.969.
-
Moghaddam SM, Song Q, Mamidi S, Schmutz J, Lee R, Cregan P and McClean PE. (2014). Developing market class-specific InDel markers from next generation sequence data in Phaseolus vulgaris L. Frontiers in Plant Science 5:185.
[https://doi.org/10.3389/fpls.2014.00185]

-
Pacurar DI, Pacurar ML, Street N, Bussell JD, Pop TI, Gutierrez L and Bellini C. (2012). A collection of InDel markers for map-based cloning in seven Arabidopsis accessions. Journal of Experimental Botany. 63:2491-2501.
[https://doi.org/10.1093/jxb/err422]

-
Penner GA, Bush A, Wise R, Kim W, Domier L, Kasha K, Laroche A, Scoles G and Molnar S. (1993). Reproducibility of random amplified polymorphic DNA(RAPD) analysis among laboratories. Plant Molecular Biology Reporter. 11:17–27.
[https://doi.org/10.1101/gr.2.4.341]

-
Rasheed A, Hao Y, Xia X, Khan A, Xu Y, Varshney RK and He Z. (2017). Crop breeding chips and genotyping platforms: Progress, challenges, and perspectives. Molecular Plant. 10:1047-1064.
[https://doi.org/10.1016/j.molp.2017.06.008]

- Rural Development Administration(RDA). (2008). Comprehensive catalogue of medicinal crop cultivars. Department of Medicinal Crops. NIHHS, RDA. pp. 106-109.
- Song Q, Jia G, Zhu Y, Grant D, Nelson RT, Hwang EY, Hyten DL and Cregan PB. (2015). Abundance of SSR motifs and development of candidate polymorphic InDel markers in soybean using next-generation sequencing. BMC Genomics. 16:134.
- Stern FC. (1943). Genus Paeonia. Journal of the Royal Horticultural Society. 68:124-131.
-
Takagi K and Harada M. (1969). Pharmacological studies on herb paeony root. II. Anti-inflammatory effect, inhibitory effect on gastric juice secretion, preventive effect on stress ulcer, antidiuretic effect of paeoniflorin and combined effects with licorice component FM 100 Yakugaku Zasshi. 89:887-892.
[https://doi.org/10.1248/yakushi1947.89.7_887]

- Tan J, Zhao Q, Yang L, Shang Z, Du Z and Yan M. (2010). Chemical constituents in roots of Paeonia lactiflora. Chinese Traditional and Herbal Drugs. 41:1245-1248.
-
Thomson MJ. (2014). High-throughput SNP genotyping to accelerate crop improvement. Plant Breeding and Biotechnology. 2:195-212.
[https://doi.org/10.9787/PBB.2014.2.3.195]

-
Wang SQ. (2019). Inbreeding and inbreeding depression of Paeonia decomposita(Paeoniaceae), a threatened endemic plant to China. Botanical Studies 60:28.
[https://doi.org/10.1186/s40529-019-0276-8]

- Wang XB, Zhang D, Shi XH, Li DQ, Zhang RL, Shao LM, Xu T, Xia YP and Zhang JP. (2022). A new Paeonia lactiflora cultivar ‘Purple Heart’. Acta Horticulturae Sinica. 49:115-116.
-
Wu K, Yang M, Liu H, Tao Y, Mei J and Zhao Y. (2014). Genetic analysis and molecular characterization of Chinese sesame(Sesamum indicum L.) cultivars using insertion-deletion (InDel) and simple sequence repeat (SSR) markers. BMC Genetics. 15:35.
[https://doi.org/10.1186/1471-2156-15-35]

-
Wu L, Nie L, Wang Q, Xu Z, Wang Y, He C, Song J and Yao H. (2021). Comparative and phylogenetic analyses of the chloroplast genomes of species of Paeoniaceae. Scientific Reports. 11:14643.
[https://doi.org/10.1038/s41598-021-94137-0]

-
Xiao PX, Li Y, Lu J, Zuo H, Pingcuo G, Ying H, Zhao F, Xu Q, Zeng X and Jiao WB. (2023). High-quality assembly and methylome of a Tibetan wild tree peony genome(Paeonia ludlowii) reveal the evolution of giant genome architecture. Horticulture Research 10:uhad241.
[https://doi.org/10.1093/hr/uhad241]

-
Xiang YJ, Zhang Q, Wei SJ, Huang C, Li ZS and Gao YX. (2020). Paeoniflorin: A monoterpene glycoside from plants of Paeoniaceae family with diverse anticancer activities. Journal of Pharmacy and Pharmacology. 72:483-495.
[https://doi.org/10.1111/jphp.13204]

-
Xu Y. (2010). Molecular plant breeding. CAB International. pp. 1-6.
[https://doi.org/10.1079/9781845933920.0001]

-
Yang Y, Sun M, Li S, Chen Q, Teixeira da Silva JA, Wang A, Yu X and Wang L. (2020). Germplasm resources and genetic breeding of Paeonia: A systematic review. Horticulture Research. 7:107.
[https://doi.org/10.1038/s41438-020-0332-2]

-
Yuan JH, Jiang SJ, Jian JB, Liu MY, Yue Z, Xu JB, Li J, Xu CY, Lin LH, Jing Y, and Hu YH. (2022). Genomic basis of the giga-chromosomes and giga-genome of tree peony Paeonia ostii. Nature Communications. 13:7328.
[https://doi.org/10.1038/s41467-022-35063-1]

-
Zhang HH, Wang J, Lang W, Liu HL, Zhang ZQ, Wu TL, Li HQ and Bai LY. (2022). Albiflorin ameliorates inflammation and oxidative stress by regulating the NF-κB/NLRP3 pathway in methotrexate-induced enteritis. International Immunopharmacology. 109:108824.
[https://doi.org/10.1016/j.intimp.2022.108824]

-
Zhang JP, Li DQ, Shi XH, Zhang D, Qiu S, Wei J, Zhang J, Zhou JH, Zhu KY and Xia YP. (2017). Mining and expression analysis of candidate genes involved in regulating the chilling requirement fulfillment of Paeonia lactiflora ‘Hang Baishao’. BMC Plant Biology. 17:262.
[https://doi.org/10.1186/s12870-017-1205-1]

- Zhang X, Wang J and Li X. (2001). A study on the chemical constituents of Paeonia lactiflora Pall. Journal of Shenyang Pharmaceutical University. 18:30-32.
-
Zhou SL, Hong DY and Pan KY (1999) Pollination biology of Paeonia jishanensis T. Hong & W.Z. Zhao(Paeoniaceae), with special emphasis on pollen and stigma biology. Botanical Journal of the Linnean Society 130:43-52.
[https://doi.org/10.1111/j.1095-8339.1999.tb00781.x]

-
Zhu S, Yu X, Wu Y, Shiraishi F, Kawahara N and Komatsu K. (2015). Genetic and chemical characterization of white and red peony root derived from Paeonia lactiflora. Journal of Natural Medicines. 69:35-45.
[https://doi.org/10.1007/s11418-014-0857-5]
