
Tanshinone IIA 고함유 단삼 추출물의 지방 생성 억제 및 이상지질혈증 마우스 모델에서의 혈중 지질 개선 효과
Correspondence to: #Ye Rim Shin and So Hee Jang are contributed equally to this paper.
This is an open access article distributed under the terms of the Creative Commons Attribution Non-Commercial License (http://creativecommons.org/licenses/by-nc/3.0/) which permits unrestricted non-commercial use, distribution, and reproduction in any medium, provided the original work is properly cited.
Abstract
This study aimed to evaluate the anti-adipogenic and lipid-modulating effects of tanshinone IIA (Tan IIA)-enriched Salvia miltiorrhiza extract (SM-CPE) prepared using cloud-point extraction (CPE), an eco-friendly method designed to enhance the yield of hydrophobic bioactive compounds.
High-performance liquid chromatography confirmed that SM-CPE contained approximately 35 times more Tan IIA than the conventional water extract (SMW). In 3T3-L1 preadipocytes, Tan IIA showed cytotoxicity at concentrations ≥ 5 μM, while SMW was non-cytotoxic up to 200 ㎍/㎖. In contrast, SM-CPE began to show cytotoxicity from 200 ㎍/㎖, likely due to the high concentration of Tan IIA. An adipogenesis assay revealed that SM-CPE inhibited lipid accumulation by 17.6% at 100 ㎍/㎖ and by 81.0% inhibition at 200 ㎍/㎖. In comparison, SMW showed relatively weak inhibition (19.9% at 200 ㎍/㎖), while Tan IIA exhibited a dose-dependent inhibition, reaching 64.4% at 20 μM. In a P-407-induced dyslipidemic mouse model, 14 days of oral administration of SM-CPE significantly reduced serum triglycerides by 54.2%, which was more than double that of SMW (23.9%) and similar to that of Tan IIA (65.6%). SM-CPE also lowered total cholesterol and low-density lipoprotein levels, whereas HDL levels increased slightly, although not statistically significant.
SM-CPE demonstrated superior anti-adipogenic and lipid-lowering effects compared with SMW and Tan IIA, supporting its potential as a natural agent for treating obesity-related metabolic disorders, such as dyslipidemia. CPE offers a practical strategy for enhancing the functional efficacy of herbal extracts by concentrating lipophilic bioactive compounds such as Tan IIA.
Keywords:
Salvia miltiorrhiza, Adipogenesis, Cloud Point Extraction, Dyslipidemia, P-407 Mouse Model, Tanshinone IIA, 3T3-L1서 언
비만은 에너지 섭취가 소비를 초과할 때 발생하는 에너지 대사 불균형으로, 전 세계적으로 심각한 건강 문제로 대두되고 있다 (Shin and Yoon, 2017). 이러한 유병률 증가는 서구화된 식생활, 유전적 요인, 환경적 요소 등 복합적 원인에 기인하며, 국내에서도 비만 유병률이 지속적으로 상승하여 중대한 공중보건 문제로 간주된다 (WHO, 2023; KDCA, 2025). 비만은 단순한 체중 증가를 넘어 다양한 대사성 질환의 발병과 밀접하게 연관된 복합적인 질환으로, 병태생리학적으로는 지방 세포의 분화 및 기능 변화가 주요 기전으로 여겨지고 있다.
지방세포는 과잉 에너지를 중성지방 (triglyceride, TG) 형태로 저장하며, 세포 분화를 통해 지방 축적 기능을 획득한다 (An et al., 2023). 이러한 지방세포의 과도한 형성 (hyperplasia)과 비대 (hypertrophy)는 인슐린 저항성, 심혈관계 질환, 염증 반응 등 다양한 대사질환의 발병에 기여한다. 특히 지방 조직에서 분비되는 adipokine인 leptin, adiponectin, 염증성 사이토카인 등의 불균형은 대사 항상성의 교란을 초래한다 (Alessi et al., 2003; Chen et al., 2013). 더불어 이상지질혈증은 비만과 밀접히 연관되며, 혈중 총 콜레스테롤 (total cholesterol, TC), TG, 저밀도 지단백 (low density lipoprotein, LDL)의 증가와 고밀도 지단백 (high density lipoprotein, HDL)의 감소는 심혈관 질환의 주요 위험 인자로 작용한다 (Addisu et al., 2023).
현재 임상에 사용되는 항비만 약물은 식욕 억제제, 지방 흡수 억제제, glucagon like peptide-1 (GLP-1) 유사체 등을 통해 체중 감소를 유도하지만, 장기 복용 시 부작용과 내성 문제가 지속적으로 제기되고 있어 (Tak and Lee, 2021; Jung and Jung, 2022), 보다 안전하고 장기 복용이 가능한 천연물 기반 항비만 소재 개발에 대한 관심이 증가하고 있다. 천연물은 다양한 생리활성을 지니며 부작용이 비교적 적다는 점에서 대체 전략으로 주목받고 있으며, 항비만 효과 외에도 염증 조절, 지질 개선, 혈당 조절 등 대사 균형 회복에 다방면의 작용을 할 수 있어 유망한 연구 분야로 평가된다 (Ferrari, 2004).
그러나 천연물의 실제 응용 가능성을 높이기 위해서는 표적 성분의 고효율 추출 및 정량적 확보, 그리고 이를 통한 표준화가 필수적이며, 이는 소재 개발의 품질관리 측면에서도 핵심 요소로 작용한다. 특히 기존의 유기용매 기반 추출법은 극성 및 독성을 지닌 유기용매를 다량 사용함으로써 환경적·인체적 유해성이 문제로 제기되고 있으며, 공정 복잡성과 비용 부담도 크다 (Chowdhury et al., 2010). 이러한 문제를 극복하기 위한 대안으로 cloud point extraction (CPE) 기술은 유기용매를 거의 사용하지 않으면서도 선택적으로 소수성 생리활성 물질을 추출할 수 있는 친환경 기술로 주목받고 있다.
CPE는 비이온성 계면활성제를 일정 농도 이상 물에 첨가한 용액을 가열하여 구름점 (cloud point) 이상에 도달하면, 계면활성제 분자가 자가 조립되어 미셀 (micel l e)을 형성하고, 용액이 두 개의 상 [계면활성제가 풍부한 상 (surfactant-rich phase)과 수용액 상 (surfactant-lean phase)]으로 분리되는 원리를 기반으로 한다 (Xie et al., 2010; Kori et al., 2021). 이 과정에서 소수성 생리활성 물질은 미셀의 소수성 중심부에 선택적으로 포획되어 계면활성제층으로 농축되고, 수용액 층과 쉽게 분리되어 효율적이고 선택적인 추출이 가능하다. 특히 이 기술은 유기용매를 거의 사용하지 않고도 추출과 동시에 전처리 및 농축이 가능하다는 점에서 고부가가치 약용작물 소재의 추출에 적합하다 (Giovanoudis et al., 2023).
단삼 (Salvia miltiorrhiza)은 고대로부터 어혈 제거, 고지혈증, 협심증, 심혈관계 질환 등의 치료에 활용되어온 대표적인 약용작물로, 그 약리 효과는 salvianolic acid B, lithospermic acid, protocatechuic aldehyde 등과 같은 hydrophilic한 phenolic 화합물과 tanshinone IIA (Tan IIA), tanshinone I, cryptotanshinone, dihydrotanshinone I과 같은 hydrophobic한 tanshinone 계열 성분의 복합 작용에 기인한다 (Zhou et al., 2005; Guo et al., 2020).
이 중 Tan IIA는 단삼의 대표적인 지용성 생리활성 물질로서, 강력한 항염증, 항산화, 항비만 및 지질 개선 효과가 보고되었으나, 낮은 극성으로 인해 일반적인 물 추출에서는 수율이 낮다 (Shi et al., 2004). 최근 CPE 기술을 활용하여 비이온성 계면활성제 l ecithin으로 추출한 결과, 기존 열수 추출 대비 약 35 배 이상의 Tan IIA 함량이 확보되었다는 보고가 있으며, 이를 통해 해당 기술의 적용 가능성이 제시되었다 (Shin et al., 2024).
Tan IIA는 지방 생성 억제를 통해 항비만 및 심혈관계 질환 개선에 기여하는 것으로, peroxisome proliferator-activated receptor gamma (PPAR-γ)와 같은 지방세포 분화 관련 전사인자의 발현을 억제하고, 중성지방 축적과 지질대사를 조절하는 것으로 알려져 있다 (Jia et al., 2016; Zhong et al., 2021). 그러나 기존 연구 대부분은 유기용매 기반 추출물이나 정제된 개별 성분을 대상으로 수행되었으며, CPE 기반 추출물을 이용한 항비만 및 지질 개선 효과에 대한 전임상 수준의 평가는 부족하다.
따라서 본 연구에서는 전통적인 물 추출법으로 얻은 단삼 물 추출물 (SMW)과 CPE 방법으로 추출한 단삼 추출물 (SM-CPE)의 Tan IIA 함량을 비교하고, 3T3-L1 지방전구세포 분화 및 지방 생성 억제 효과 (in vitro)와 poloxamer-407 (P-407) 유도 이상지질혈증 마우스 모델의 혈중 지질 개선 효과 (in vivo)를 평가하였다. 이를 통해 SM-CPE의 생리활성 증진 가능성과 CPE 기술 기반으로 한 항비만 기능성 천연물 소재로서의 활용 가능성을 검토하고자 하였다.
재료 및 방법
1. 시약
Dulbecco’s Modified Eagle’s Medium (DMEM)은 Hyclone Laboratories (Logan, UT, USA)에서 구입하였다. Bovine calf serum (BCS)와 phosphate buffer saline (PBS), insulin은 Welgene (Daegu, Korea)에서, fetal bovine serum (FBS)과 penicillin/streptomycin (P/S)은 각각 GenDEPOT (Katy, TX, USA)과 Gibco (Grand Island, NY, USA)에서 구입하여 사용하였다. 10% formalin 용액은 Tech & Innovation (Chuncheon, Korea)에서, tanshinone IIA, dexamethasone, 3-isobutyl-1-methylxanthine powder, 3-(4,5-dimethylthiazol-2-yl)-2,5-diphenyltetrazolium bromide (MTT), Oil red O, isopropanol, dimethylsulfoxide (DMSO), poloxamer-407 (P-407), fenofibrate 및 기타 시약은 Sigma-Aldrich (St. Louis, MO, USA)에서 구입하여 사용하였다.
2. 단삼 물 추출물 (SMW)과 Tan IIA 고함유 단삼 추출물 (SM-CPE)의 제조
단삼 (S. miltiorrhiza) 지하부는 충청북도 2022년 4월에 음성군 소이면에서 수확하여 농촌진흥청 국립원예특작과학원 약용작물과로부터 제공받았다. 수확된 원료는 60℃에서 열풍 건조한 후 분쇄하여 추출에 사용하였다.
단삼 물 추출물 (SMW)은 단삼 분말 1 g에 증류수 20 ㎖를 첨가한 후 초음파 처리기 (120 V, 60 ㎐, UCP-20, JeioTech, Daejeon, Korea)를 이용해 실온에서 30 분간 초음파 처리를 수행하였다. 이후 여과지 (No. 6, Whatman International Ltd., Maidstone, England)로 여과하여 침전물을 제거하고 상등액을 회수하였다.
단삼 CPE 추출물 (SM-CPE)은 Shin 등 (2024)의 방법을 일부 변형하여 제조하였다. 단삼 분말 1 g에 3% lecithin 용액 (w/v) 20 ㎖을 혼합하고, 실온에서 40 분간 초음파 처리 (120V, 60Hz, UCP-20, JeioTech, Daejeon, Korea)를 실시하였다. 이후 2% (w/v) NaCl을 첨가하고, 1 M citric acid로 pH를 6.0으로 조정하였다. 30 분간 평형 반응 후, 3,500 rpm에서 15 분간 원심분리하여 수용액 층 (aqueous phase)를 제거하고, 계면활성제가 포함된 상 (surfactant-rich phase)를 분리·획득하였다 (Fig. 1).
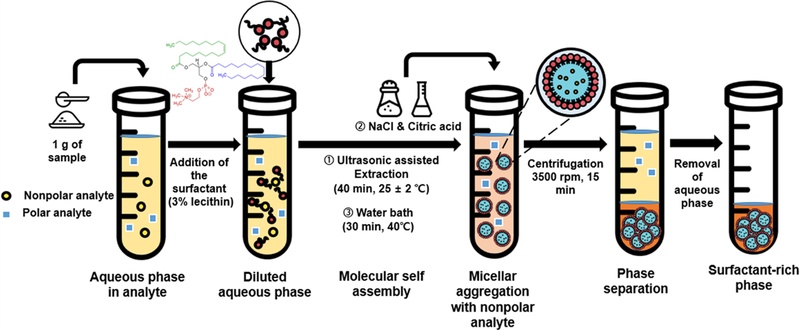
Schematic representation of the cloud point extraction (CPE) process for preparing tanshinone IIA-enriched S. miltiorrhiza extract.The CPE procedure was conducted using 1 g of S. miltiorrhiza powder and 3% (w/v) lecithin solution. The sample underwent ultrasonic extraction (40 min, 25 ± 2℃), followed by NaCl and citric acid treatment to adjust the ionic strength and pH (pH 6.0). Upon heating in a water bath (30 min, 40℃), micellar self-assembly facilitated the selective entrapment of nonpolar analytes (e.g., tanshinone IIA). After centrifugation (3,500 rpm, 15 min), the surfactant-rich phase containing hydrophobic components was separated from the aqueous phase.
제조된 SMW 및 SM-CPE 시료는 동결건조기 (TFD5503, IlsinBioBase, Dongducheon, Korea)로 분말화한 뒤, –20℃에 보관하여 실험에 사용하였다.
3. HPLC 분석 조건
Tan IIA의 정량 분석은 Chen 등 (2012)의 방법을 일부 수정하여 HPLC (Shimadzu LC-20AT system, Shimadzu Co., Kyoto, Japan)로 수행하였다. 각 추출물은 10 ㎎/㎖의 농도로 준비하였으며 시료 및 표준품을 각각 10 ㎕ 주입하였고 유속은 1.0 ㎖/min으로 설정하였다.
이동상은 0.8% acetic acid를 포함한 water (A)와 0.8% acetic acid를 포함한 acetonitrile (B)로 구성되었으며 gradient elution 조건을 적용하였다 [gradient 조건 : 0분 – 40분 (A : B = 98 : 2) → 40분 – 60분 (A : B = 54 : 46) → 60분 – 70분 (A : B = 34 : 66) → 70분 – 71분 (A : B = 10 : 90) → 71분 – 80분 (A : B = 10 : 90)].
Column은 ODS-AM (250 ㎜ × 4.6 ㎜, 5 ㎛, YMC Co., Ltd., Kyoto, Japan)을 사용하였고, 검출 파장은 280 ㎚로 설정하였다. 표준물질의 검량선은 0.5 ㎍/㎖ - 200 ㎍/㎖ 범위에서 작성하였다.
4. 세포주 및 세포배양 조건
3T3-L1 전지방세포주는 American Type Culture Collection (Rockville, MD, USA)으로부터 분양받아 사용하였다. 세포는 DMEM에 10% BCS, 100 U/㎖ penicillin, 100 ㎍/㎖ streptomycin을 첨가한 배지에서 37℃, 5% CO2 조건의 CO2 배양기 (Forma Direct Heat CO2 Incubator, Thermo Fisher Scientific, Madison, WI, USA)에서 배양하였다.
5. 세포 생존율 측정 (MTT assay)
3T3-L1 전지방세포를 96-well plate에 well당 1 × 104 cells로 분주하고, Tan IIA 및 각 추출물 (SMW, SM-CPE)을 처리하여 24 시간 동안 배양하였다. 이후 5 ㎎/㎖의 MTT 용액을 첨가하여 3 - 4 시간 반응시킨 뒤, 상등액을 제거하고 생성된 formazan 결정체를 DMSO 200 ㎕에 용해하였다. 흡광도는 microplate reader (VICTOR X3, PerkinElmer, Waltham, MA, USA)로 540 ㎚에서 측정하였으며, 세포 생존율은 대조군 대비 백분율로 계산하였다.
6. 3T3-L1 지방세포 분화 유도
3T3-L1 세포를 12-well plate에 well 당 2 × 105 cells로 분주하고 confluent 상태에 도달할 때까지 2 일 간격으로 배지를 교환하며 배양하였다. 분화를 유도하기 위해 DMEM에 10% FBS, 1% P/S, 1 μM dexamethasone, 0.5 mM 3-isobutyl-1-methylxanthine (IBMX), 5 ㎍/㎖ insulin을 포함한 분화유도 배지로 교체하고 Tan IIA, SMW, SM-CPE를 각각 처리하였다.
분화 유도 2 일 차부터는 DMEM에 10% FBS, 1% P/S, 5 ㎍/㎖ insulin을 포함한 유지배지로 교체하고 2 일 간격으로 총 6 일간 배양하였다.
7. Oil red O 염색
분화가 완료된 세포를 PBS로 세척한 뒤, 10% formalin 용액 1 ㎖로 실온에서 25 분간 고정하였다. 고정 후 isopropanol에 용해한 0.5% Oil red O 용액 1 ㎖를 첨가하여 35 분간 염색하였다. 염색 후 증류수로 세척·건조한 뒤 현미경으로 관찰하였으며, 염색된 Oil red O는 isopropanol로 용출하여, microplate reader (VICTOR X3, PerkinElmer, Waltham, MA, USA)를 이용해 510 ㎚에서 흡광도를 측정하였다.
8. 실험동물
7주령의 수컷 ICR 마우스를 오리엔트바이오사 (Orient Co., Seongnam, Korea)에서 구입하여 1 주간 일반 사료를 급여하면서 환경 적응시킨 후 실험에 사용하였다. 사육 조건은 온도 23 ± 2℃, 상대습도 50 ± 4%, 광주기 12 시간 (09:00 – 21:00)으로 유지하였다. 모든 동물실험은 강원대학교 동물실험윤리위원회의 승인을 받아 수행하였다 (승인번호 : KW-211029-1).
9. 이상지질혈증 유발
P-407은 Johnston (2004) 및 Johnston과 Palmer (1993)의 방법에 따라 사용하였다. P-407을 생리식염수에 용해하여 300 ㎎/㎏ 농도로 조제한 뒤, 4℃에서 overnight 보관하였다. 이상지질혈증 유도는 실험 종료 24 시간 전에 단회 복강 주사(intraperitoneal injection)로 수행하였다.
10. 실험군 분리 및 투여
실험동물은 무작위로 6 개 군 (n = 5 / group)으로 구분하였다. 물과 일반 사료를 공급한 정상대조군 (vehicle only), P-407 투여에 의한 이상지질혈증 유도군, P-407 + SMW (200 ㎎/㎏, p.o.) 투여군, P-407 + SM-CPE (200 ㎎/㎏ p.o.) 투여군, P-407 + Tan IIA (10 ㎎/㎏, i.p.) 투여군, P-407 + fenofibrate (3.3 ㎎/㎏, p.o.) 투여군. SMW, SM-CPE 및 양성대조군으로 사용한 fenofibrate는 14 일간 경구투여하였고, Tan IIA는 동일 기간 동안 복강 투여하였다. P-407은 실험 종료 24 시간 전에 300 ㎎/㎏을 단회 복강 투여하였다 (Fig. 2).
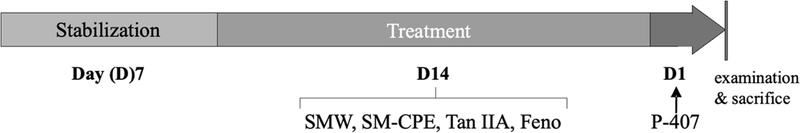
Mice experimental protocol schedule.Mice received administration of SMW and SM-CPE (200 ㎎/㎏, p.o.) or fenofibrate (3.3 ㎎/㎏, p.o.) or Tan IIA (3.3 ㎎/㎏, i.p.) for 14 days. P-407 (300 ㎎/㎏, i.p.) was administeresd 24 hours before killing mice. SMW; S. miltiorrhizae water extract, SM-CPE; S. miltiorrhiza cloud point extract, Tan IIA; tanshinone IIA, P-407; poloxamer-407.
11. 체중 및 비장 무게 측정
체중은 전자저울 (BT 224S, Sartorius, FRA)로 매주 측정하였다. 실험 종료 후 마우스를 희생하고 비장을 절제하여 0.9% 멸균 생리식염수로 세척한 뒤 여과지로 수분을 제거하고 무게를 측정하였다. 비장 무게는 체중 (g)에 대한 상대값(% of body weight)으로 계산하였다.
12. 혈액학적 분석 방법
실험 종료 후 마우스를 경추 탈골로 희생시킨 뒤 심장에서 약 1 ㎖의 혈액을 채취하였다. 혈액은 4℃에서 8,000 rpm으로 15 분간 원심분리 (1730R, BMS, Seoul, Korea)하여 혈청을 분리하였다. 총콜레스테롤 (total cholesterol)은 cholesterol reagent (Bayer, Whippany, NJ, USA), 중성지방 (triglyceride)은 triglycerides reagent (Bayer, Whippany, NJ, USA), HDL은 direct HDL cholesterol kit (Bayer, Whippany, NJ, USA), LDL은 direct LDL chol esterol kit (Bayer, Whippany, NJ, USA)를 이용하여 측정하였다. 혈청 내 농도는 ㎎/㎗ 단위로 표시하였다.
13. 통계분석
실험 결과는 4 회 이상 반복한 값을 평균 ± 표준편차 (mean ± SD)로 표시하였다. 통계분석은 SPSS 26.0 (Statistical Package for Social Sciences, SPSS Inc., Chicago, IL, USA)을 사용하였으며 one-way analysis of variance (ANOVA) 후 Tukey HSD 다중분석법 및 t-test를 사용하여 각 처리의 유의성을 판단하였다 (*p < 0.05).
결과 및 고찰
1. 단삼 2종 추출물의 tanshinone IIA 함량
Tan IIA의 정량 분석을 위해 HPLC를 이용한 측정 결과, 표준물질의 검출 피크는 약 76.77분의 retention time에서 단일 peak로 확인되었다 (Fig. 3A). 검량선은 y = 149538x – 62759로 작성되었으며, 결정계수 (R²)는 0.9995로 매우 우수한 직선성과 정량 정확성을 나타내어, 본 분석법의 신뢰성을 확인하였다.
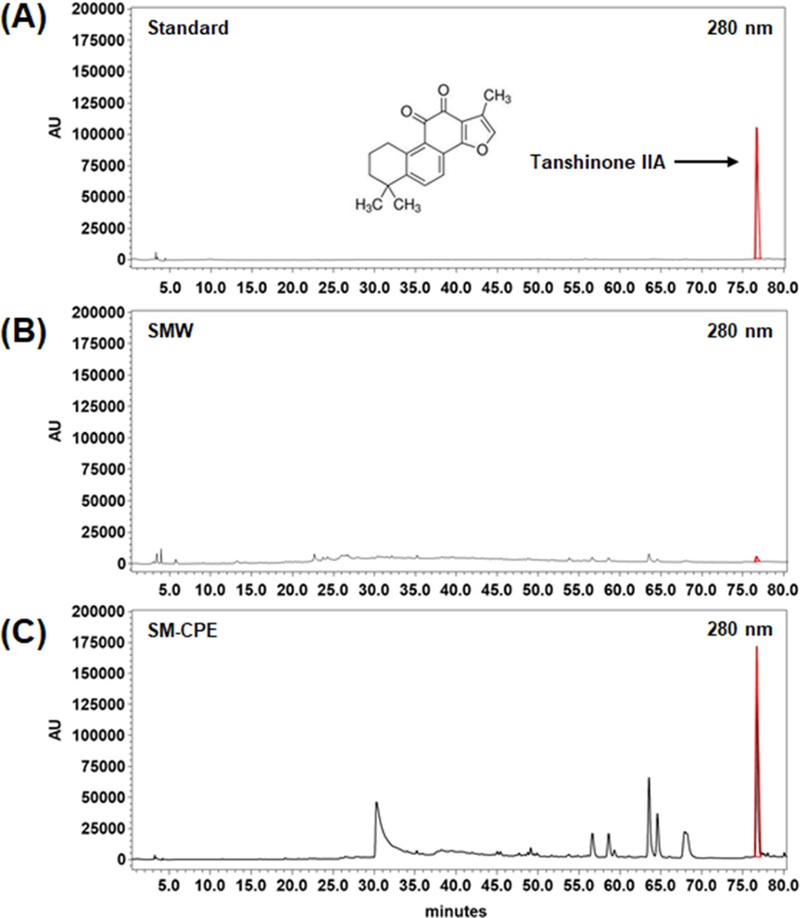
Comparative HPLC chromatograms of S. miltiorrhiza water extract (SMW) and cloud point extract (SM-CPE) showing the quantification of tanshinone IIA.(A); Chromatogram of tanshinone IIA standards chemical (100 ㎍/㎖), (B); chromatogram of the SMW, (C); chromatogram of the SM-CPE. SMW; Salvia miltiorrhiza water extract, SM-CPE; Salvia miltiorrhiza cloud point extract, HPLC; high-performance liquid chromatography.
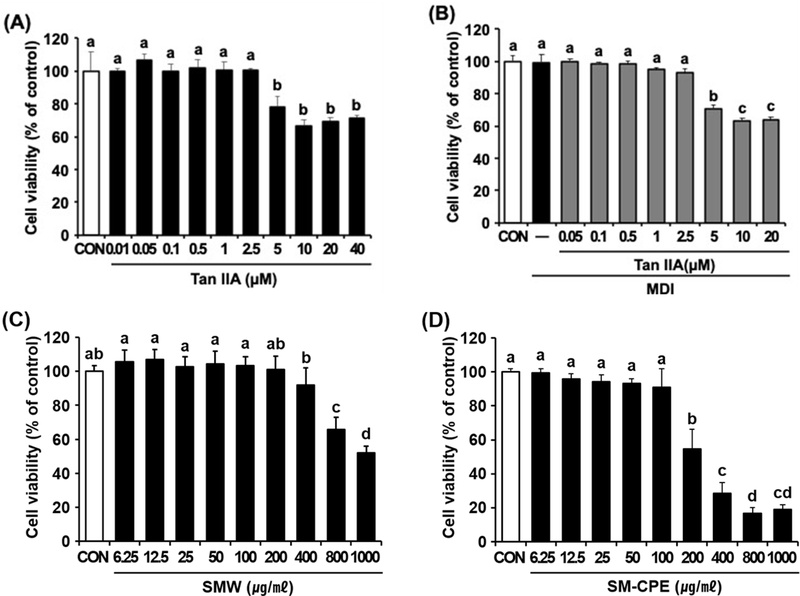
Effect of Tan IIA and two extracts of SM on the lipid accumulation of 3T3-L1 adipocytes.(A); Cell viability following Tan IIA treatment was assessed by MTT assay. (B); After treatment with MDI medium and Tan IIA for 24 hours, cell viability was assessed by MTT assay. (C-D); Cell viability following SMW or SM-CPE treatment was assessed by MTT assay.
추출물 내 Tan IIA 함량을 비교한 결과, 열수 추출법으로 제조된 단삼 물 추출물 (SMW)에서는 0.220 ± 0.005 ㎎/g의 Tan IIA가 함유되어 있었으며, CPE 방식으로 제조된 단삼 추출물 (SM-CPE)에서는 7.710 ± 0.268 ㎎/g이 검출되었다. 이는 SM-CPE의 Tan IIA의 함량이 SMW 대비 약 35.05 배 높음을 의미하며, CPE 기술이 단삼 내 지용성 유효성분의 수득률을 현저히 향상시킬 수 있음을 보여준다 (Fig. 3 and Table 1).

Comparison of tanshinone IIA content between S. miltiorrhiza water extract (SMW) and cloud point extract (SM-CPE).
이러한 결과는 CPE 기술이 소수성 생리활성 물질의 선택적 농축 및 추출에 효과적이라는 기존 보고 (Shin et al., 2024)와 일치하며, 친환경적 추출법을 통해 기능성 천연물의 유효성분 함량을 크게 증진시킬 수 있는 가능성을 시사한다.
2. Tanshinone IIA의 세포독성 평가
3T3-L1 전지방세포에서 Tan IIA의 세포독성을 평가하기 위하여 MTT assay를 실시하였다. Tan IIA 단독 처리와 Tan IIA와 MDI 배지 (3-isobutyl-methylxanthine, dexamethasone, insulin) 병용 처리 조건 모두에서 2.5 μM 이하 농도에서는 유의한 세포독성이 나타나지 않았다. 그러나 Tan IIA 5 μM 이상 처리 시 분화 전·후, 모두에서 세포 생존율이 각각 78.35%와 70.61%로 유의하게 감소하여 세포독성을 나타내었다 (Fig. 3A-B).
Tan IIA의 독성 농도로 확인된 5 μM (약 1.47 ㎍/㎖)의 농도는 786-O 인간 신장암 세포주에서 Tan IIA를 세포 생존율이 50% 저해되는 최대 농도 (IC50) 값이 2 ㎍/㎖ (6.8 μM)로 보고된 결과 (Wei et al., 2012)와 유사하였으며 이는 Tan IIA의 세포 독성이 농도 의존적임을 뒷받침함과 동시에 본 연구에서 제시된 독성 범위가 기존 다른 문헌에서 제시된 농도 범위 안에 위치한다는 점에서 타당성을 확인할 수 있었다.
한편, MDI 배지만 단독 처리한 경우 세포 생존율에는 변화가 없었고, MDI 배지 + Tan IIA 병용 처리군에서도 Tan IIA 단독 처리와 유사한 독성 반응이 나타났다. 이에 따라, 지방세포 분화 조절 실험에서는 세포 생존율이 90% 이상 유지되는 2.5 μM 이하의 농도를 Tan IIA의 적정 처리 농도로 설정하였다. (Fig. 3B).
3. SMW 및 SM-CPE의 세포독성 평가
MTT assay 결과, SMW는 200 ㎍/㎖까지는 세포 생존율이 90% 이상으로 독성을 나타내지 않았으나, 400 ㎍/㎖ 이상에서 유의한 감소가 나타나 1,000 ㎍/㎖ 에서는 47.88%까지 세포 생존율이 감소하였다 (Fig. 3C).
SM-CPE의 경우 100 ㎍/㎖까지는 독성이 없었으나, 200 ㎍/㎖에서 세포 생존율이 54.62%로 급감하였고, 1,000 ㎍/㎖에서는 19.03%로 매우 낮은 생존율을 나타내었다 (Fig. 3D). 동일 농도에서 SM-CPE가 SMW보다 2 배 이상 강한 세포독성을 나타내었다.
Tan IIA의 분자량 (294.3 g/mol)을 기준으로 환산하면, 독성이 확인된 5 μM는 약 1.47 ㎍/㎖에 해당되고 SMW와 SM-CPE 내에 포함된 Tan IIA 함량을 고려하면, SMW 400 ㎍/㎖에는 약 0.044 ㎍/㎖, SM-CPE 200 ㎍/㎖에는 약 1.78 ㎍/㎖의 Tan IIA가 포함되어 있어, SM-CPE의 세포독성이 주로 고함량 Tan IIA에 기인함을 시사한다.
SM-CPE 내 포함된 계면활성제 성분인 l ecithin의 독성 가능성은 낮았다. Kosmerl 등 (2021)의 보고에 따르면, 3T3-L1 세포에서 대두·우유 유래 l ecithin은 최대 0.5 ㎎/㎖까지 80% 이상, 1.5 ㎎/㎖에서도 55% - 72%의 생존율을 유지한다고 보고하였으며, 본 실험에서 사용된 lecithin 농도는 이보다 낮았다.
SMW와 SM-CPE의 지방세포 분화 억제 실험에는 두 시료 모두 200 ㎍/㎖ 이하의 농도를 비독성 농도 범위로 설정하였다.
4. Tanshinone IIA와 단삼 추출물의 3T3-L1 세포 지방분화 억제 효과
Oil Red O 염색 결과, MDI 배지를 처리한 양성 대조군은 무처리군 대비 지방 축적량이 약 3.95 배 증가하였다. Tan IIA는 0.1 μM부터 유의하게 지방세포 분화를 억제하였고, 2.5 μM에서는 약 50.73%, 20 μM에서 최대 64.36%의 분화 억제 효과를 나타냈다 (Fig. 4A-B).
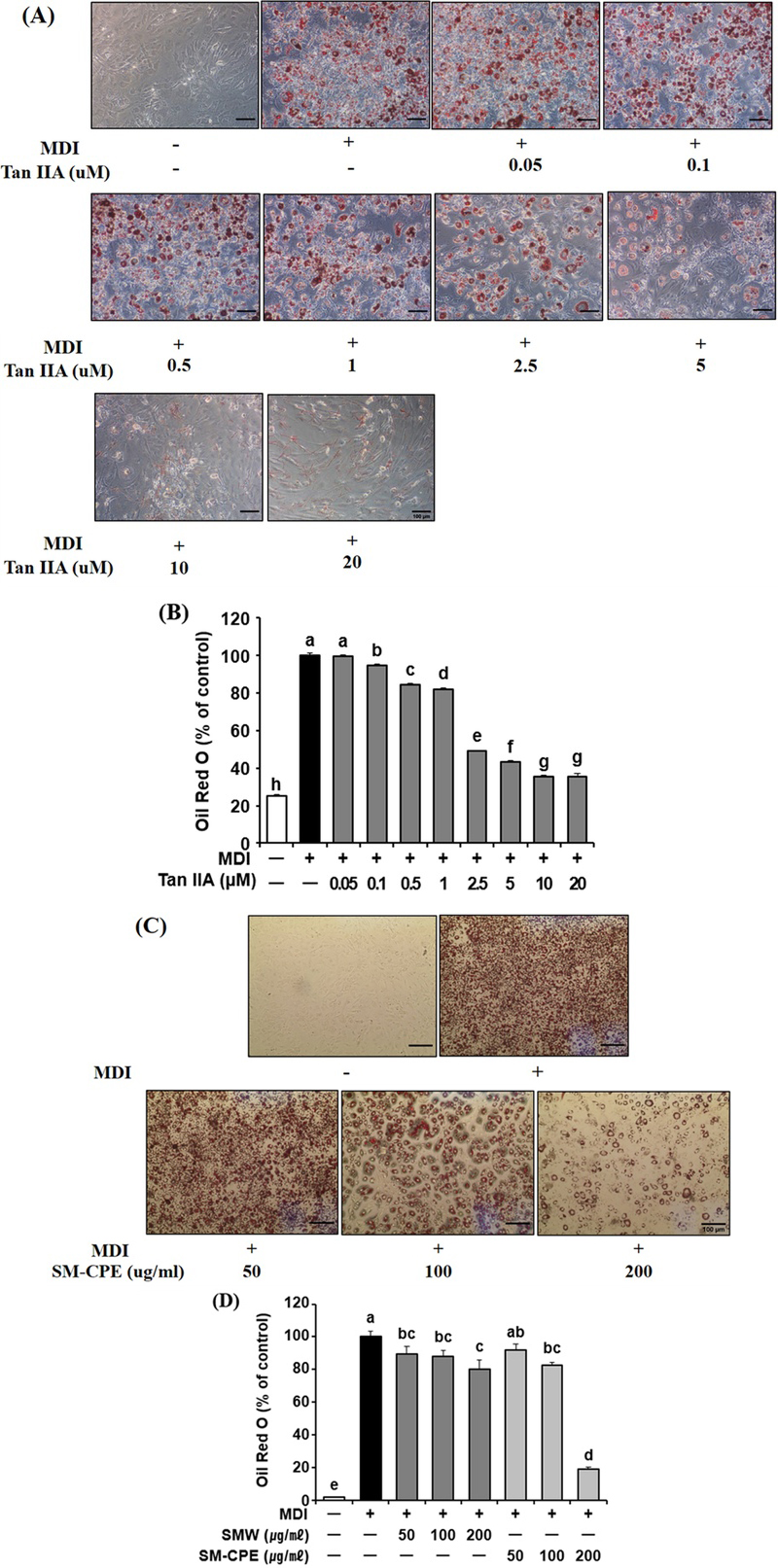
Inhibitory effects of Tan IIA and Salvia miltiorrhiza extracts on lipid accumulation during 3T3-L1 adipocyte differentiation.(A); Representative Oil Red O staining images showing lipid droplet accumulation in 3T3-L1 cells treated with varying concentrations of Tan IIA (0 - 20 μM) during MDI-induced differentiation. (B); Quantification of Oil Red O retention in panel (A). (C); Representative Oil Red O staining images of 3T3-L1 cells treated with either S. miltiorrhiza water extract (SMW) or cloud point extract (SM-CPE) at indicated concentrations (50 ㎍/㎖ - 200 ㎍/㎖). (D); Quantitative analysis of panel (C). Data are presented as the mean ± SD (n = 5). Statistical significance was analyzed by one-way ANOVA followed by Tukey’s HSD test. Bars with different letters indicate significant differences (*p < 0.05). Tan IIA; tanshinone IIA, CON; untreated control, MDI; differentiation cocktail (500 μM IBMX, 1 μM dexamethasone, 5 ㎍/㎖ insulin)
SM-CPE와 SMW의 비교 실험 결과, 두 추출물 모두 지방 세포 분화를 유의하게 억제하였으나 억제 효과의 정도에는 명확한 차이가 나타내었다 (Fig. 4C-D). SM-CPE는 50, 100, 200 ㎍/㎖ 농도에서 각각 8.17%, 17.57%, 81.02%의 지방세포 분화 억제 효과를 보였고, SMW는 동일 농도에서 각각 10.50%, 12.22%, 19.90%의 완만한 억제 효과를 나타내었다 (Fig. 4C-D). SM-CPE의 200 ㎍/㎖에서 나타난 강력한 억제 효과는 MTT assay에서 세포독성이 나타난 농도임을 고려하였을 때 (Fig. 3D), 일부 세포독성 영향이 포함되었을 가능성이 있으나, 고함량 Tan IIA에 의한 직접적 효과도 크다고 판단된다.
이러한 결과는 Tan IIA의 농도 의존적인 특성에 기인한 작용 기전과 관련이 있을 것으로 생각된다. Tan IIA는 세포 내로 쉽게 유입되는 지용성 물질로, parathyroid hormone-related protein (PTHrP) 활성화와 mitogen-activated protein kinases (MAPK) 경로 조절을 통해 (Chan et al., 2011), 지방세포 분화의 핵심 전사인자인 peroxisome proliferator-activated receptor-γ (PPAR-γ)와 CCAAT/enhancer binding protein alpha (C/EBP-α)의 발현을 억제함으로써 지방세포 형성을 저해하는 것으로 알려져 있다 (Wu et al., 2012). 특히 고농도 Tan IIA는 MAPK 경로를 직접 억제하여 전사인자 활성을 강하게 저해함으로써, 지방 분화를 뚜렷하게 억제할 수 있다 (Park et al., 2017).
SMW는 salvianolic acid B (Sal B), salvianolic acid A (Sal A) 등의 수용성 페놀 화합물 성분에 의해 저농도에서는 일부 지방 분화 억제 효과를 나타낸 것으로 확인되는 바, 이러한 결과는 Sal B는 3T3-L1 세포에서 100 μM 농도에서 약 20%의 분화 억제 효과를 보였으며 (Kwon and Jang, 2022), Sal A 또한 고지방 식이 마우스 모델에서 지방 축적 저해 및 간 보호 효과를 나타낸다고 보고한 결과 (Ding et al., 2016)에서도 확인된다. 그러나 이러한 수용성 성분은 농도 증가에 따른 억제 효과의 향상이 크지 않기 때문에, 고농도에서의 효과 차이는 주로 Tan IIA의 함량 차이에 기인한다고 해석된다.
5. P-407 유도 이상지질혈증 마우스의 체중 및 비장 무게 변화
이상지질혈증은 단순한 체중 증가에 국한되지 않고, 다양한 전신성 대사질환과 면역계의 기능 이상을 유발할 수 있는 주요 위험 요인으로 알려져 있다. 특히 중성지방 (TG) 및 저밀도 지단백 (LDL)의 과도한 증가는 동맥경화성 플라크 형성에 기여하며, 관상동맥질환 및 뇌졸중과 같은 심혈관계 합병증의 발병 위험을 높인다 (Fuster, 2016; Carr et al., 2019).
또한, 지질대사의 교란은 면역계에도 영향을 미치는 것으로 알려져 있어, 지방산과 콜레스테롤 수치의 급격한 증가는 비장(spleen)과 같은 면역기관의 기능 변화와 비대 등을 유발할 수 있으며, 콜레스테롤 수치의 상승은 신장 기능 저하와도 관련이 있는 것으로 보고되고 있다 (Scarpioni et al., 2012; Provenzano et al., 2019).
Poloxamer-407 (P-407)로 유도된 이상지질혈증 마우스 모델에서 14 일간의 SMW, SM-CPE 및 Tan IIA 투여 후 체중 변화와 주요 면역 장기인 비장의 무게를 측정한 결과 (Tabl e 2), 양성 대조군인 fenofibrate 처리군에서만 체중이 유의하게 감소한 반면, SMW, SM-CPE 및 Tan IIA 투여군에서는 체중 감소 효과가 통계적으로 유의한 수준으로 관찰되지 않았다 (*p < 0.05).
이러한 결과는 고콜레스테롤혈증 및 이상지질혈증의 치료제로 fenofibrate를 주성분으로 하는 LIPIDIL™을 생쥐에 복강 투여한 결과 체중이 감소하였으며 이는 fenofibrate가 PPAR-α를 활성화하여 지방 산화를 촉진하고, 지방 축적을 억제하는 작용기전을 가지고 있기 때문이라는 보고와 유사하였으나 (Carmona et al., 2005), 고지방 식이 모델에서 Tan IIA가 PPAR-γ에 대한 길항작용을 통해 지방 축적을 억제하고, 음식 섭취량을 변화시키지 않으면서 체중을 감소시킨다고 보고 (Gong et al., 2008)와 단삼 추출물이 장기간 고지방 식이를 한 마우스의 체중 감소를 유도하였다고 보고 (Ai et al., 2022)와는 상이하였다.
본 연구의 SMW, SM-CPE 및 Tan IIA 투여군에서 유의한 체중 감소 효과가 관찰되지 않은 것은 고지방 식이 모델과 P-407 유도 모델 간의 대사적 차이에서 기인하는 것으로 판단된다.
Johnston (2004)의 연구에 따르면 P-407 유도 모델은 LPL (lipoprotein lipase)과 hepatic lipase를 억제하여 단기간에 고지혈증을 유발하는 특징이 있다. 고지방 식이 모델은 장기적인 지방 축적을 통해 대사에 영향을 미치지만 P-407 유도 모델은 단기적인 혈중 지질 급등 및 lipase 억제를 유도하는 급성 모델로, 지방 조직 내 축적 변화보다는 혈중 지질 수치에 대한 영향이 크기 때문에 Tan IIA나 단삼 추출물이 체중 감소에 미치는 효과는 제한되었을 가능성이 있다.
비장 무게 측정을 체중 (g)에 대한 상대값으로 계산한 결과에서도 SMW, SM-CPE, Tan IIA 투여군 간의 spleen/BW 값은 실험군 간 다소 차이를 보였으나, 통계 분석 결과 모든 그룹 간 통계적으로 유의한 차이는 관찰되지 않았다 (*p < 0.05, Table 2). 일부 선행 연구에서는 P-407을 복강 투여한 후 비장의 무게 증가가 보고되었으나 (Goncharova et al., 2015), 본 연구에서는 동일한 처리 수준임에도 불구하고 통계적으로 유의한 비대 또는 위축은 확인되지 않았다. 이는 P-407에 의한 면역기관 영향이 실험 조건 (투여 횟수, 관찰 기간 등)에 따라 상이하게 나타날 수 있음을 나타내며, 향후 다기관 및 장기 평가를 통한 조직학적 분석이 필요함을 나타낸다고 하겠다.
7. SM-CPE와 SMW 및 Tan IIA의 혈중 지질 프로파일 변화
지방세포 분화 (adipogenesis)를 억제하는 생리활성은 체내 지방 축적을 감소시킬 뿐 아니라, 전신적 지질대사 (lipid metabolism)에 긍정적 영향을 미쳐 총콜레스테롤 (TC), 중성지방 (TG), 저밀도 지단백 (LDL)의 감소 및 고밀도 지단백 (HDL)의 증가로 이어질 수 있다 (Jia et al., 2016).
P-407 유도 이상지질혈증 동물 모델에서 SM-CPE와 SMW 및 Tan IIA의 혈중 지질 지표 개선 효과를 확인한 결과 Fig. 5에 제시하였다.
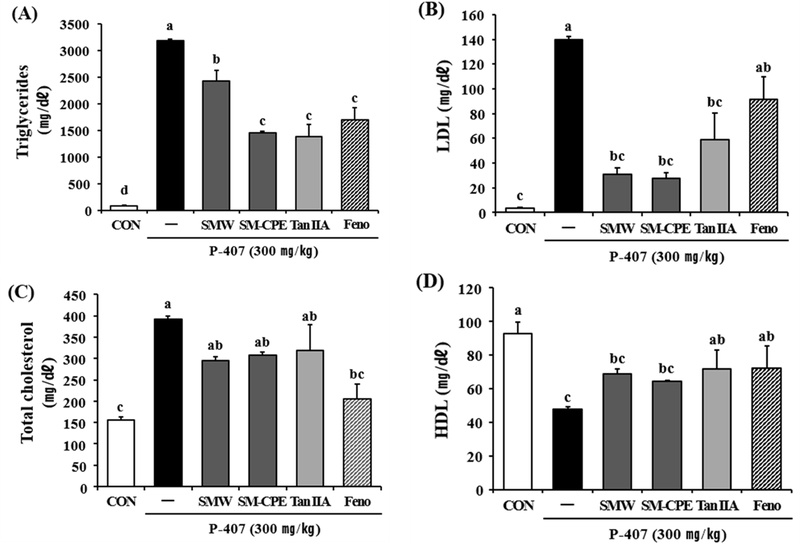
Effects of tanshinone IIA, SMW, and SM-CPE on serum lipid profiles in P-407-induced dyslipidemic mice.(A); Triglycerides levels, (B); low-density lipoprotein (LDL) levels, (C); total cholesterol levels, (D): high-density lipoprotein (HDL) levels. Data represent serum lipid levels after 14 days of oral administration of SMW (200 ㎎/㎏), SM-CPE (200 ㎎/㎏), or tanshinone IIA (10 ㎎/㎏) in mice with dyslipidemia induced by intraperitoneal injection of P-407 (300 ㎎/㎏). Fenofibrate (3.3 ㎎/㎏, p.o.) was used as a positive control. Results are expressed as mean ± SD (n = 5). Statistical significance was determined using one-way ANOVA followed by Tukey’s HSD test. Columns with different superscript letters (a–d) are significantly different (*p < 0.05). CON; untreated control, Veh; vehicle control (P-407 only), SMW; S. miltiorrhiza water extract, SM-CPE; S. miltiorrhiza cloud point extract, Tan IIA; Tanshinone IIA, Feno; fenofibrate; P-407; Poloxamer-407, TG; triglyceride, TC; total cholesterol, HDL; high-density lipoprotein, LDL; low-density lipoprotein.
P-407을 투여군은 정상 대조군 대비 혈중 TG는 97.33%, LDL은 97.64%, TC는 60.05% 증가하였으며, HDL은 48.82% 이 수준으로 감소하여 급성 이상지질혈증 모델이 성공적으로 유도되었음을 확인하였다. 14 일간 SMW, SM-CPE, Tan IIA를 각각 투여한 결과, TG는 양성 대조군인 fenofibrate의 경우, P-407 유도군 대비 69.43%의 감소 효과를 보였으며, Tan IIA (65.61%), SM-CPE (54.22%), SMW (23.86%) 순으로 감소하였다 (Fig. 5A). Fenofibrate와 Tan IIA의 TG 저하 효과는 유사한 수준이었고, SM-CPE 역시 Tan IIA와 통계적으로 유사한 억제 효과를 나타내어 SM-CPE 처리에 의해 유도되는 TG 값의 감소가 Tan IIA의 효과가 반영되었음을 확인할 수 있었으며 이러한 효과는 SMW (23.86%)에 비해 약 2배 이상 강한 효과를 나타냄을 확인하였다 (p< 0.05),
LDL 수치 또한 SMW, SM-CPE, Tan IIA 모두에서 P-407 유도군 대비 유의하게 감소했으며, 세 그룹 간 통계적 유의성은 없었으나 전반적으로 개선 경향이 일관되게 관찰되었다 (Fig. 5B). TC 수치 역시 SMW은 24.94%, SM-CPE의 경우 21.63%, Tan IIA은 18.83% 감소로, 모든 처리군에서 지질 수치가 안정적으로 개선됨을 확인하였다 (Fig. 5C).
한편, P-407에 의해 약 48.82% 감소한 HDL 농도는 Tan IIA을 처리한 경우 50.63%까지 회복되어 fenofibrate보다 우수한 HDL 증가 효과를 나타내었으나 (*p < 0.05), SMW와 SM-CPE 투여군에서도 HDL 수치가 회복되는 경향은 보였으나 통계적으로 유의한 수준은 아니었다 (Fig. 5D). 이는 Tan IIA가 HDL 회복과 관련된 작용 기전을 갖고 있음을 시사한다.
이러한 SM-CPE의 우수한 지질 개선 효과는 SM-CPE에 고함유된 Tan IIA의 다중 생리활성 기전에 의한 것으로 해석된다. Tan IIA는 ApoE 결핍 마우스 모델에서 Omentin-1/ABCA1 경로를 통해 콜레스테롤 배출을 촉진하고, miR-33a/SREBP-2/Pcsk9 경로를 조절하여 간 내 지방 축적을 억제함으로써 지질 프로파일을 개선하는 것으로 보고된 바 있고 (Jia et al., 2016; Tan et al., 2019). 이러한 기전은 Tan IIA가 지질 대사 조절에 있어 중요한 성분임을 뜻한다.
또한, SM-CPE가 특히 TG 수치를 유의미하게 감소시킨 효과는 Tan IIA의 지질 대사 조절 작용과 함께 추출 공정에 사용된 lecithin 역시 지질대사 개선에 기여했을 가능성이 있는 것으로 생각된다. 레시틴은 인지질의 일종으로 세포막의 주요 구성 성분이며, 지질 대사와 밀접한 관련이 있는 바, 특히 대두 유래 lecithin은 간 보호, 콜레스테롤 저하, 지질 흡수 조절 효과가 보고되어 있으며 (Scholfield, 1981; Onaolapo et al., 2024), Yang 등 (2007)의 연구에 따르면, 대두 lecithin 섭취가 고지방 식이를 한 쥐에서 TG와 TC 수치를 유의미하게 감소시키며, 간 내 지질 배출을 촉진하는 것으로 나타났으며 Mourad 등 (2010)은 고콜레스테롤 환자에게 대두 lecithin 캡슐 1 개 (500 ㎎)을 투여한 결과 TC는 각각 40.66%와 42.00%, LDL은 각각 42.05%와 56.15% 감소했다고 보고한 바 있다. 이러한 기전적 시너지 작용은 SM-CPE가 단일 성분보다 복합 효과를 나타내는 기반이 될 수 있음을 나타낸다고 하겠다.
이상의 연구 결과는 SMW, SM-CPE, 그리고 Tan IIA가 모두 지질 프로파일 개선에 긍정적인 영향을 미친다는 점을 보여준다. 특히, Tan IIA 함량을 높인 SM-CPE는 혈중 TG 및 LDL 수치를 효과적으로 조절할 가능성을 제시하며, 분리 정제된 단일 물질인 Tan IIA과 유사하거나 더 우수한 효능을 나타내었다. 이는 CPE 기술이 Tan IIA와 같은 지용성 생리활성 성분의 수득률을 크게 높임으로써, 기능성 성분의 농축과 생리활성 증진이라는 두 가지 측면에서 효과적인 전략임을 시사한다고 하겠다. 또한 CPE 기술은 향후 천연물 기반 기능성 소재 개발에서 유효성분의 효능을 극대화할 수 있는 효과적인 추출 전략으로 활용될 수 있음을 나타낸다.
References
-
Addisu B, Bekele S, Wube TB, Hirigo AT and Cheneke W. (2023). Dyslipidemia and its associated factors among adult cardiac patients at Ambo university referral hospital, Oromia region, west Ethiopia. BMC Cardiovascular Disorders. 23:321. https://link.springer.com/article/10.1186/s12872-023-03348-y, (cited by 2024 Dec. 13).
[https://doi.org/10.1186/s12872-023-03348-y]

-
Ai ZL, Zhang X, Ge W, Zhong YB, Wang HY, Zuo ZY and Liu DY. (2022). Salvia miltiorrhiza extract may exert an anti-obesity effect in rats with high-fat diet-induced obesity by modulating gut microbiome and lipid metabolism. World Journal of Gastroenterology. 28:6131-6156.
[https://doi.org/10.3748/wjg.v28.i43.6131]

-
Alessi MC, Lijnen HR, Bastelica D and Juhan-Vague I. (2003). Adipose tissue and atherothrombosis. Pathophysiology of Haemostasis and Thrombosis. 33:290-297.
[https://doi.org/10.1159/000083816]

-
An SM, Cho SH and Yoon JC. (2023). Adipose tissue and metabolic health. Diabetes and Metabolism Journal. 47:595-611.
[https://doi.org/10.4093/dmj.2023.0011]

-
Carmona MC, Louche K, Nibbelink M, Prunet B, Bross A, Desbazeille M, Dacquet C, Renard P, Casteilla L and Pénicaud L. (2005). Fenofibrate prevents rosiglitazone-induced body weight gain in ob/ob mice. International Journal of Obesity. 29:864-871.
[https://doi.org/10.1038/sj.ijo.0802943]

-
Carr SS, Hooper AJ, Sullivan DR and Burnett JR. (2019) Non-HDL-cholesterol and apolipoprotein B compared with LDL-cholesterol in atherosclerotic cardiovascular disease risk assessment. Pathology. 51:148-154.
[https://doi.org/10.1016/j.pathol.2018.11.006]

-
Chan P, Liu IM, Li YX, Yu WJ and Cheng JT. (2011). Antihypertension Induced by tanshinone IIA Isolated from the Roots of Salvia miltiorrhiza. Evidence-based Complementary and Alternative Medicine. 2011:392627. https://onlinelibrary.wiley.com/doi/full/10.1093/ecam/nep056, (cited by 2024 Dec. 15)
[https://doi.org/10.1093/ecam/nep056]

-
Chen X, Deng Y, Xue Y and Liang J. (2012). Screening of bioactive compounds in Radix Salviae miltiorrhizae with liposomes and cell membranes using HPLC. Journal of Pharmaceutical and Biomedical Analysis. 70:194-201.
[https://doi.org/10.1016/j.jpba.2012.06.030]

-
Chen YC, Zeng XY, He Y, Liu H, Wang B, Zhou H, Chen JW, Liu PQ, Gu LQ, Ye JM and Huang ZS. (2013). Rutaecarpine analogues reduce lipid accumulation in adipocytes via inhibiting adipogenesis/lipogenesis with AMPK activation and UPR suppression. ACS Chemical Biology. 8:2301-2311.
[https://doi.org/10.1021/cb4003893]

-
Chowdhury SA, Vijayaraghavan R and MacFarlane DR. (2010). Distillable ionic liquid extraction of tannins from plant materials. Green Chemistry. 12:1023-1028.
[https://doi.org/10.1039/b923248f]

-
Ding C, Zhao Y, Shi X, Zhang N, Zu G, Li Z, Zhou J, Gao D, Lv L, Tian X and Yao J. (2016). New insights into salvianolic acid A action: Regulation of the TXNIP/NLRP3 and TXNIP/ChREBP pathways ameliorates HFD-induced NAFLD in rats. Scientific Reports. 6:28734. https://www.nature.com/articles/srep28734, (cited by 2024 Dec. 21)
[https://doi.org/10.1038/srep28734]

-
Ferrari CK. (2004). Functional foods, herbs and nutraceuticals: Towards biochemical mechanisms of healthy aging. Biogerontology. 5:275-289.
[https://doi.org/10.1007/s10522-004-2566-z]

- Fuster VP. (2016). Pharmacological management of dyslipidemia in high and very high cardiovascular risk patients. Revista Española de Sanidad Penitenciaria. 18:95-108.
-
Giovanoudis I, Athanasiadis V, Chatzimitakos T, Kalompatsios D, Bozinou E, Gortzi O, Nanos GD and Lalas SI. (2023). Isolation of polyphenols from two waste streams of clingstone peach canneries utilizing the cloud point extraction method. Biomass. 3:291-305.
[https://doi.org/10.3390/biomass3030018]

-
Goncharova NV, Shurlygina AV, Mel’nikova EV, Karmatskikh OL, Avrorov PA, Loktev KV and Korolenko TA. (2015). Cellular composition of the spleen and changes in splenic lysosomes in the dynamics of dyslipidemia in mice caused by repeated administration of poloxamer 407. Bulletin of Experimental Biology and Medicine. 160:28-31.
[https://doi.org/10.1007/s10517-015-3090-7]

-
Gong Z, Huang C, Sheng X, Zhang Y, Li Q, Wang MW, Peng L and Zang YQ. (2008). The role of tanshinone IIA in the treatment of Obesity through peroxisome proliferator-activated receptor γ antagonism. Endocrinology. 150:104-113.
[https://doi.org/10.1210/en.2008-0322]

-
Guo R, Li L, Su J, Li S, Duncan, SE, Liu Z and Fan G. (2020). Pharmacological activity and mechanism of tanshinone IIA in related diseases. Drug Design, Development and Therapy. 2020:4735-4748.
[https://doi.org/10.2147/DDDT.S266911]

-
Jia L, Song N, Yang G, Ma Y, Li X, Lu R, Cao H, Zhang N, Zhu M, Wang J, Leng X, Cao Y, Du Y and Xu Y. (2016). Effects of tanshinone IIA on the modulation of miR-33a and the SREBP-2/Pcsk9 signaling pathway in hyperlipidemic rats. Molecular Medicine Reports. 13:4627-4635.
[https://doi.org/10.3892/mmr.2016.5133]

-
Jia LQ, Zhang N, Xu Y, Chen WN, Zhu ML, Song N, Ren L, Cao HM, Wang JY and Yang GL. (2016). Tanshinone IIA affects the HDL subfractions distribution not serum lipid levels: Involving in intake and efflux of cholesterol. Archives of Biochemistry and Biophysics. 592:50-59.
[https://doi.org/10.1016/j.abb.2016.01.001]

-
Johnston TP and Palmer WK. (1993). Mechanism of poloxamer 407-induced hypertriglyceridemia in the rat. Biochemical Pharmacology. 46:1037-1042.
[https://doi.org/10.1016/0006-2952(93)90668-M]

-
Johnston TP. (2004). The P-407-induced murine model of dosecontrolled hyperlipidemia and atherosclerosis: a review of findings to date. Journal of Cardiovascular Pharmacology. 43:595-606.
[https://doi.org/10.1097/00005344-200404000-00016]

-
Jung HN and Jung CH. (2022). Pharmacologic treatment of obesity. Journal of Korean Medical Association. 65:408-416.
[https://doi.org/10.5124/jkma.2022.65.7.408]

- Korea Disease Control and Prevention Agency(KDCA). (2025). Trends in prevalence of obesity, 2014–2023. Public health weekly report 2025. Korea Disease Control and Prevention Agency. Chungju, Korea. 18:397-398. file:///C:/Users/herba/Downloads/phwr-18-8-397.pdf (cited by 2025 Apr. 5).
-
Kori S. (2021). Cloud point extraction coupled with back extraction: A green methodology in analytical chemistry. Forensic Sciences Research. 6:19-33.
[https://doi.org/10.1080/20961790.2019.1643567]

-
Kosmerl E, García-Cano I, Rocha-Mendoza D and Jiménez-Flores R. (2021). Characterization of milk and soy phospholipid liposomes and inflammation in 3T3-L1 adipocytes. JDS communications. 2:238-242.
[https://doi.org/10.3168/jdsc.2020-0054]

-
Kwon HS and Jang BC. (2022). Anti-adipogenic effect and mechanism in 3T3-L1 preadipocyte differentiation by salvianolic acid B. Kyemyeong Mdical Journal. 41:67-75.
[https://doi.org/10.46308/kmj.2022.00213]

-
Mourad AM, De Carvalho Pincinato E, Mazzola PG, Sabha M and Moriel P. (2010). Influence of soy lecithin administration on hypercholesterolemia. Cholesterol. 2010:824813. https://onlinelibrary.wiley.com/doi/full/10.1155/2010/824813, (cited by 2024 Nov. 11).
[https://doi.org/10.1155/2010/824813]

-
Onaolapo MC, Alabi OD, Akano OP, Olateju BS, Okeleji LO, Adeyemi WJ and Ajayi AF. (2024). Lecithin and cardiovascular health: A comprehensive review. The Egyptian Heart Journal. 76:92. https://link.springer.com/article/10.1186/s43044-024-00523-0, (cited by 2024 Nov. 7).
[https://doi.org/10.1186/s43044-024-00523-0]

-
Park YK, Obiang-Obounou B, Lee J, Lee TY, Bae MA, Hwang KS, Lee KB, Choi JS and Jang BC. (2017). Anti-adipogenic effects on 3T3-L1 cells and zebrafish by Tanshinone IIA. International Journal of Molecular Sciences. 18:2065. https://www.mdpi.com/1422-0067/18/10/2065, (cited by 2025 Apr. 11).
[https://doi.org/10.3390/ijms18102065]

-
Provenzano M, Coppolino G, Faga T, Garofalo C, Serra R and Andreucci M. (2019). Epidemiology of cardiovascular risk in chronic kidney disease patients: The real silent killer. Reviews in Cardiovascular Medicine. 20:209-220.
[https://doi.org/10.31083/j.rcm.2019.04.548]

-
Scarpioni R, Ricardi M, Albertazzi V and Melfa L. (2012). Treatment of dyslipidemia in chronic kidney disease: Effectiveness and safety of statins. World Journal of Nephrology. 1:184-194.
[https://doi.org/10.5527/wjn.v1.i6.184]

-
Scholfield CR. (1981). Composition of soybean lecithin. Journal of the American Oil Chemists Society. 58):889-892.
[https://doi.org/10.1007/BF02659652]

-
Shi Z, He J and Chang W. (2004). Micelle-mediated extraction of tanshiones from Salvia miltiorrhiza bunge with analysis by high-performance liquid chromatography. Talanta. 64:401-407.
[https://doi.org/10.1016/j.talanta.2004.03.001]

-
Shin SS and Yoon M. (2017). Korean red ginseng(Panax ginseng) inhibits obesity and improves lipid metabolism in high fat dietfed castrated mice. Journal of Ethnopharmacology. 210:80-87.
[https://doi.org/10.1016/j.jep.2017.08.032]

-
Shin YR, Ryu BR, Kang MJ, Kim MJ, Jeong JT, Han JW, Lee GW and Lim JD. (2024). Pharmaceutical constituents contents and deviations in Korean and Chinese cultivars of Salvia miltiorrhiza root(Danshen) followed by crop years. Korean Journal of Medicinal Crop Science. 32:90-104.
[https://doi.org/10.7783/KJMCS.2024.32.2.90]

-
Tak YJ and Lee SY. (2020). Anti-obesity drugs: Long-term efficacy and safety: An updated review. The World Journal of Men’s Health. 39:208-221. https://pmc.ncbi.nlm.nih.gov/articles/PMC7994651/, (cited by 2025 Apr. 5)
[https://doi.org/10.5534/wjmh.200010]

-
Tan YL, Ou HX, Zhang M, Gong D, Zhao ZW, Chen LY, Xia XD, Mo ZC and Tang CK. (2019). Tanshinone IIA promotes macrophage cholesterol efflux and attenuates atherosclerosis of APOE-/-mice by Omentin-1/ABCA1 pathway. Current Pharmaceutical Biotechnology. 20:422-432.
[https://doi.org/10.2174/1389201020666190404125213]

-
Wei X, Zhou L, Hu L and Huang Y. (2012). Tanshinone IIA arrests cell cycle and induces apoptosis in 786-O human renal cell carcinoma cells. Oncology Letters. 3:1144-1148.
[https://doi.org/10.3892/ol.2012.626]

- World Health Organization(WHO). (2023). Obesity and overweight. World Health Organization. Geneva, Switzerland. https://www.who.int/news-room/fact-sheets/detail/obesity-and-overweight, (cited by 2025 Apr. 9)
-
Wu SJ, Lee SJ, Su CH, Lin DL, Wang SS and Ng LT. (2012). Bioactive constituents and anti-proliferative properties of supercritical carbon dioxide Salvia miltiorrhiza extract in 3T3-L1 adipocytes. Process Biochemistry. 47:216-224.
[https://doi.org/10.1016/j.procbio.2011.10.034]

-
Xie S, Paau MC, Li CF, Xiao D and Choi MM. (2010). Separation and preconcentration of persistent organic pollutants by cloud point extraction. Journal of Chromatography A. 1217:2306-2317.
[https://doi.org/10.1016/j.chroma.2009.11.075]

- Yang SY, Hong SY, Sung MK, Kang MH and Kim MK. (2007). Effect of lecithin intake on lipid metabolism and antioxidative capacity in rats fed high fat diet. Journal of Nutrition and Health. 40:312-319.
-
Zhong C, Lin Z, Ke L, Shi P, Li S, Huang L, Lin X and Yao H. (2021). Recent research progress(2015-2021) and perspectives on the pharmacological effects and mechanisms of Tanshinone IIA. Frontiers in Pharmacology. 12:778847. https://www.frontiersin.org/journals/pharmacology/articles/10.3389/fphar.2021.778847/full, (cited by 2025 Apr. 5).
[https://doi.org/10.3389/fphar.2021.778847]

-
Zhou L, Zuo Z and Chow MSS. (2005). Danshen: An overview of its chemistry, pharmacology, pharmacokinetics, and clinical use. The Jouranl of Clinical Pharmacology. 45:1345-1359.
[https://doi.org/10.1177/0091270005282630]
